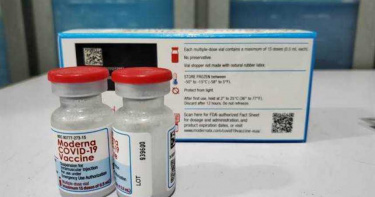
全球疫苗嚴重短缺 莫德納供應商:年底前東南亞訂單滿載
由於Delta變種病毒的因素,世界各國開始討論是否要追打第三劑疫苗,這讓原本數量不足的疫苗,再次發生嚴峻的搶購作戰。而莫德納疫苗在東南亞的供應商裕利醫藥(Zuellig Pharma)則表示,到2021年底前,東南亞的莫德納疫苗訂單幾乎滿載,這也凸顯了世界各國在搶購疫苗方面遇到了重重困難。根據《亞洲新聞台》報導指出,總部位於新加坡的裕利醫藥,負責莫德納疫苗在東南亞、香港、澳門、台灣等地的銷售、監管與批准採購合約,其執行長格雷姆(John Graham)在接受訪問時表示,最近敲定了許多莫德納疫苗的採購訂單,但交貨日幾乎都是放在2022年,因為到2021年底前,莫德納在東南亞的訂單幾乎是滿載狀態。雖說是滿載,但格雷姆也有表示「可能在年底前有機會再釋出一些疫苗,但這也要看當時的供應狀況來決定」。但他還是強調「如果現在才來商討訂購疫苗的事情,很有可能要到2022年才有辦法穩定供應」。而報導中也指出,目前新加坡、菲律賓、泰國與台灣等國家,均與裕利醫藥簽訂購買莫德納疫苗的契約,而格雷姆也透露,目前已經有些國家開始採購更多的疫苗作為追加劑量(第三劑),但交貨期也是設定在2022年至2023年。格雷姆坦言「這是一場爭奪疫苗供應的競賽」。

卡民間疫苗3/雅各臣拉裕利結盟蘇系 陳時中變夾心「問到疫苗就生氣」
外界對「裕利」公司有點陌生,其實裕利是國內最大的冷鏈運輸外商業者。去年十二月二十二日,國民黨立委賴士葆曾在立院質詢陳時中,追問指揮中心不能公開疫苗合約的原因,他當時質詢陳時中,是否因『冷鏈商還未談好』有關?賴追問,衛福部與裕利醫藥、港商雅各臣、信東生技等廠商談過了嗎?由於當時外界盛傳「東洋案」破局與雅各臣介入有關,陳時中尷尬之餘證實,確曾與上述廠商開過會,也令很多人急忙追問「裕利何許人也?」,沒想到短短數月,當時名氣還有限的「裕利」在疫苗案中已成關鍵角色,連國際媒體都點名追捧。全台上千萬劑的常規疫苗,均由裕利醫藥冷鏈物流系統運送。 (圖/報系資料庫)根據裕利官網資料記載,裕利醫藥(Zuellig Pharma)是瑞士的跨國集團,台灣裕利則是瑞士醫藥集團分公司,在台從事醫藥、冷鏈逾二十五年,集團業務規模在亞洲首屈一指,今年三月還在桃園大園區設立全台最大的醫藥物流中心,堪稱亞太地區最大冷鏈倉儲。裕利不僅被指在雅各臣及企業界洽購、捐贈BNT疫苗過程扮演協力商,就連藍營執政的南投、花蓮、雲林和台東等四縣市,向指揮中心遞案進口約二百八十萬劑BNT疫苗,冷鏈協力商也是裕利。不過,四縣市澄清未指定特定冷鏈商,應是委託代購疫苗盛弘集團的決定。雲林縣長張麗善等藍營四縣市首長,聯手向衛福部遞件,爭取進口疫苗。(圖/報系資料庫)國內一位GDP藥廠負責人透露,去年八月東洋著手買BNT疫苗,曾與衛福部、BNT德國原廠及上海復星代表,舉行四方視訊會議,當時與東洋合作的GDP台灣冷鏈業者曾奉命到場報告,獲得高度重視冷鏈運送細節的德國BNT認可,「但據悉該冷鏈業者不是『裕利』,日前國內媒體指稱裕利集團才是德國BNT屬意合作對象的說法,真偽難辨,不能排除是有人刻意放話帶風向。」。東洋採購BNT疫苗破局後,美麗島電子報董事長吳子嘉在今年2月22日質疑,指揮中心掩蓋與雅各臣談判內容,遭指揮中心指揮官陳時中駁斥。媒體人朱凱翔日前獨家披露,指揮中心專家諮詢小組召集人張上淳與德國藥廠BNT視訊探討購買疫苗事宜的會議中,東洋製藥合作的冷鏈商也有參加。(圖/翻攝自網路)陳時中指雅各臣是在去年9月18日『透過1922、部長信箱』表達與指揮中心洽談意願,這番說法卻再度引發在野黨不滿,指控雅各臣結合綠營內「新蘇系」勢力,出手阻撓東洋買BNT疫苗。北市議員游淑慧就說,奉蔡總統之命,指揮中心現在要處理民間企業捐贈BNT疫苗案,陳時中夾在蔡、蘇二人間,一下子說要全力幫忙,一下又改口要求原廠授權書,搞得快精神錯亂,難怪只要有立委質詢他買疫苗的事,陳時中就會顯得很不耐煩。
全球首款乾眼症鼻噴劑 年底可望在台取證
台灣目前約有300萬的民眾受乾眼症所苦,乾眼症是一種由多種因素導致的眼表疾病,以淚膜受損為特徵。健康的淚膜能保護和潤滑眼睛、沖走異物,然而台灣現行的治療藥物卻尚未能滿足病患需求。東生華(TW-8432)引進全球第一個乾眼症治療鼻腔噴霧劑,其中的活性成分Varenicline,通過結合菸鹼型乙醯膽鹼(nACh)受體而發揮作用。當受體活化後,三叉神經副交感神經通路被激活,導致天然淚液分泌增加,從而達到治療乾眼症的目的。透過新的給藥途徑,藉此增加天然淚液分泌,適用於輕度至重度的乾眼症患者,提供更簡便、安全的用藥選擇。此款鼻腔噴霧劑已獲美國FDA批准作為多劑量包裝,治療乾眼症徵候及症狀, 東生華去年7月宣布在台的查驗登記和商業化權利,已於今年初接獲食藥署新藥查驗登記的續審通知,若審查順利有望於年底取證。東生華總經理楊思源表示,此款噴鼻劑是由美國製藥公司 Oyster Point Pharma 開發的新藥,並於2021年在美國獲得FDA新藥許可證並成功上市。東生華透過與箕星藥業合作,並進行台灣的查驗登記及商業化。根據兩項臨床試驗共940名乾眼症患者使用資料顯示,患者平均在僅使用一劑噴鼻液就有淚液分泌增加的改善,在使用2週期間,患者的乾眼症症狀和癥兆有明顯治療反應,使用4週後平均產生的天然淚液量仍然顯著增加,大幅改善患者生活品質。楊思源指出,乾眼症全球醫藥市場規模龐大,且呈現迅速增長。根據Global Data的「Dry Eye Syndrome: Global Drug Forecast and Market Analysis to 2028報告」,顯示自2018年到2028年,乾眼症的年複合成長率高達10.6%,預估至2028年全球市值最高可達111億美元。

印度眼藥水工廠偽造檢查報告、放任員工打赤腳 美國FDA下令全面回收
美國於2023年發生多起非處方眼藥水遭受汙染的事情,美國食品與藥物管理局(FDA)更是在11月初一口氣公布27款問題眼藥水、人工淚液等產品。之後循線調查,發現這些眼藥水、人工淚液均是印度新孟買的公司「基利奇」(Kilitch Healthcare India)所生產。基利奇不僅偽造產品檢查報告,更放任員工在廠區內打赤腳。目前FDA已經下令禁止進口基利奇的產品,同時也要求基利奇回收問題產品,但目前基利奇尚未執行。根據《紐約郵報》報導指出,近期FDA公布27款市面上可以買到的非處方眼藥水、人工淚液,其中包含沃爾瑪、CVS Health、Target Up & Up和Velocity Pharma等品牌的產品。這些問題產品被FDA檢驗出細菌檢測陽性反應,FDA也在第一時間下令回收這些產品。之後FDA的工作人員發現,這些問題產品多是由印度新孟買的一家公司所生產,FDA也曾於10月派員調查該工廠,發現該工廠的微生物學家涉嫌撰寫假報告,以此來保證產品是無菌狀態。同時也發現,該工廠無菌區的工人上班時並沒有穿戴適合的防護設備,甚至有人打赤腳,直接在機器面前梳理自己的儀容。FDA的工作人員也發現,廠區內所生產的眼藥水區域,有明顯的細菌汙染。之後FDA對該工廠發出警告,並指稱使用該工廠的產品有可能會導致失明、視力喪失的可能。但FDA的報告中,第一時間並未透露印度工廠的名稱,而是被媒體透過拼湊的方式確定,FDA所指的問題工廠,就是印度的基利奇。目前基利奇尚未針對此事件進行回應,而面對FDA所要求的回收產品一事,目前基利奇也尚未執行。

高端流感疫苗讓家長恐慌 鄭麗文質疑:會不會又重演銷毀事件?
公費流感疫苗昨日開打,由於今年公費疫苗名單有「高端」在列,讓許多家長擔心小孩會打到高端疫苗,要求政府提出解套方式;立委鄭麗文今(3)日進一步揭露,相較於其他公費疫苗廠商採原裝進口,高端反而是向韓國進口原液到台灣,再分裝填充成為「國產疫苗」,還能藉此在政府採購過程中加分,引發外界疑慮,未來若沒有人要施打高端疫苗,會不會又重演銷毀事件?鄭麗文表示,去年covid-19疫情盛行,高端疫苗的採購資料封存30年,爭議到現在無解,導致人民不信任的廠商,為何這次卻出現在公費疫苗名單中?她說,提供給老人小孩施打的公費疫苗,並不能選擇廠牌,讓不少收到疫苗接種通知單的家長紛紛表示,寧可棄權也不願意貿然接種。鄭麗文指出,疾管署今年4月公布本年度公費四價流感疫苗得標廠商,有國光、賽諾菲、台灣東洋及高端,今年更是從過去的最低標,改採最有利標方式辦理,疾管署還說這次改採最有利標方式,是為確保廠商履約品質,並順利供貨保障國人健康。但她質疑,疾管署為何要在今年更改公費四價流感疫苗的投標規則,難道以前都不用保障國人健康?鄭麗文揭露,在今年新的投標遊戲規則中,其中一項評分項目「供貨的穩定」,也讓高端得以「加分」,該項指標認為若能「在台灣生產」,供貨就會相對穩定。然而她也指出,相較於其他公費疫苗廠商採原裝進口,高端反而是向韓國進口原液到台灣,再分裝填充成為「國產疫苗」,跟雞蛋之亂的「實質轉型」一模一樣,這樣卻能加分? 依據高端公司官網,高端2018年10月宣布取得韓國跨國藥廠GC Pharma四價流感疫苗的獨家代理權進入台灣市場,並取得衛福部核准,在台灣進行四價季節流感疫苗的三期臨床試驗;而由韓國原裝進口的四價流感疫苗也在台灣完成三期臨床試驗,高端並依此三期臨床試驗結果向台灣食藥署申請藥證。意外的是,2020年4月23日,高端公司發布重訊,主動向食藥署撤回進口韓國流感疫苗藥證查驗登記申請案,改採自有品牌模式,由韓國GC Pharma生產原液,高端進行充填分裝與品管放行。目前在台灣上市的流感疫苗,分為原裝進口如賽諾菲、GSK和東洋代理的流感疫苗,以及純國產疫苗,只有高端流感疫苗是分段生產製造,在韓國生產原液、台灣充填包裝。台灣食藥署今年3月通過高端流感疫苗的藥證,正是韓國進口原液、台灣充填包裝的產品。雖然根據食藥署說法,高端有提供在台灣執行第三期臨床試驗、收案對象為20至50歲健康成人的臨床試驗資料,但根據公開資料,這是指韓國原裝進口流感疫苗的數據,而這種分段拼裝生產的疫苗,並未提供台灣三期臨床試驗數據。高端流感疫苗仿單也載明,在兒童(3至18歲)和65歲以上的年長者族群,其免疫生成性資料來自在韓國執行且全程韓國製造的流感疫苗第三期臨床試驗,而非現在台灣上市的特殊拼裝版高端流感疫苗。因此原裝進口韓國流感疫苗的三期臨床數據,能否等同於特殊拼裝版高端流感疫苗,引發外界疑慮。鄭麗文表示,高端不只第一次參與就成功得標,甚至一舉拿下佔比高達10.1%的訂單,超過70萬劑,這是不是在護航?打在人體的疫苗,能這麼輕易修改規則的嗎?她說,民眾無法選擇公費疫苗,現在家長都不知道自己的孩子會不會打到高端流感疫苗,政府難道可以這樣毫無作為,任由疑慮持續擴大嗎?若沒有人要施打高端流感疫苗,那麼到時候會不會又重演銷毀事件?此外,立委王鴻薇今年4月時就曾質疑,高端過往從未涉足公費流感疫苗領域,且已連續3個月營收掛零,政府此次採購也與過往慣例不同,讓高端可以「原液」而非原裝進口,並改採最有利標,這是不是為高端量身定做標準,就為幫高端做業績不倒閉。

大咖生技ETF3/蔡明興新藥股買最多! 開發金超車國泰富邦這二檔
富邦金(2881)董座蔡明興這十年來相挺生技業,成為鑽石生技(6901)創始股東,還投資發起人路孔明創辦的中天(4128)與合一生技(4743)(原投資泉盛,後與合一合併)兩家公司,近20年來,金控與蔡明興本人都積極參與生醫產業策略性投資支持新創公司育成與培植,旗下人壽、富邦金控創投等,至少已投入逾160億元。2014年蔡明興以個人名義與鑽石生技投資公司捐贈共1.5億元,成立永續經營之「臺大鑽石種子基金」,扶植新創鼓勵研發,亦是台灣生技醫藥發展基金會(TBF)的捐資者,2021年起擔任國家生技醫療產業策進會(生策會)的顧問。CTWANT調查,從中天到鑽石投資的欣耀生醫、合一生技、醣基生醫等,蔡明興可說是一網打盡家家都有投資,以這些公司的前十大股東資料來看,蔡明興家族各持股為1.22%、9.38%、7.36%、1.83%;蔡明忠與蔡明興相同,除了個人投資鑽石之外,對中天、合一則各持股1.21%、1.51%。合一股價在2020年曾從25元飆漲到7月最高點476.5元,主要是因宣布與丹麥國際大藥廠利奧製藥LEO Pharma A/S共同簽署「異位性皮膚炎、過敏性氣喘新藥FB825」合作研發,以5.3億美元全球獨家授權協議,以及ON101(WH-1)糖尿病足慢性傷口潰瘍新藥三期臨床試驗第二次期間分析結果達標等因素所致;目前股價來到186元。進一步觀察多家生技股的前十大股東,富邦金子公司富邦人壽名列其中知名企業者,有持股中天3.8%、合一2.02%,還有保瑞(6472)的2.60%、葡萄王(1707)的7.05%、大江(8436)的4.40%、東洋(4105)的3.67%,從開發癌症新藥股、保健保養品、醫美到CDMO(委託開發暨製造服務)大廠都涵括。昱展新藥為美時化學前董事長林東和於2016年所創,富邦金、開發金皆有投資。(圖/翻攝自昱展新藥官網)富邦金控創投除了鑽石生技,還有投資昱展新藥(6785)的6.18%,為特殊學名藥廠美時化學(1795)前董事長林東和於2016年所創,以美國FDA 505 (b)(2)法規路徑,開發含鴉片類成癮症、難治型憂鬱症、慢性癌痛及帕金森氏症等長效藥物。台新金董事長吳東亮則與蔡明興都是十年前同時投資鑽石,2021年同年受聘為生策會顧問之外,還邀請他的外甥女婿、「生技界併購王」之稱的保瑞(6472)董座盛保熙為台新金子公司分享生技產業脈動,台新金並與保瑞共同成立規模約30億元健康基金與保瑞生技,鎖焦併購創新生產製造(CDMO)事業佈局;旗下的健檢中心與盛弘集團以換股策略結盟,跨足精準醫療業。吳東亮今年還選進生策會理事,並於其擔任理事長的工商協進會中提案成立「生技醫療產業研究委員會」,力推該產業,另外也投資研發抗癌新藥的生華科(6492),該公司共同創辦人之一即為親家胡定吾。國泰金控旗下的國泰人壽除了投資隱形眼鏡晶碩(6491)2.60%之外,國泰創投對漢達(6620)也曾持股達1.14%,係以藥物劑型及處方設計為基礎之研發型特色專業製藥,聚焦於505(b)(2)新藥以及高技術門檻之利基型學名藥的公司,已有胃食道逆流學名藥、多發性硬化症用藥等在美國上市銷售。中信金控子公司台灣人壽也曾投資美時達0.54%、中國信託創投對台康生技持股1.47%;開發金控子公司中華開發資本轉投資的「中華開發生醫創業投資」則與富邦金創投同樣看中昱展新藥,投資更高達12.08%,與國泰創投都有投資過的漢達也曾多達4.94%,就連中華開發創投也曾投資漢達有2.13%。另外,大江生醫集團旗下的大江基因(6879),主攻基因檢測與幹細胞、免疫細胞等產品研發製造等,在2022年私募普通股案,佳世達(2352)即投資5.45億元參與。

中華生技醫藥行業協會 越南訪拓團點石成金
CBIA越南醫藥參訪團 開拓亞洲市場的重要一步中華生技醫藥行業協會(CBIA) 理事長陳建州藥師八月帶領CBIA越南醫藥投資訪拓團,進行六項投資訪拓任務 : 1、參加Vietnam Medi-Pharma製藥暨醫療器械展,並投資越南市場。2、醫療器材經銷商合作:與胡志明市醫療設備協會簽訂MOU。3、協助台灣廠商取證困境:提昇醫療器材與食品業者取證能力。4、打進越南醫療服務市場:建立台灣頂尖抗衰老名醫與胡志明市三家醫療院所進行越南換證與執業計畫。5、醫療產業供銷一體:與越南Life Gift集團簽訂MOU,台灣原料製造+越南包裝取證,同時擁有GMP、ISO與US FDA認證,借以拓展東協與美國市場。6、越南落地解決方案:協助設立胡志明公司/代表處、越南投資設立、引進AI營銷平台,增進營銷能力。帶領台商醫藥及食品海外落地 建立企業國際競爭力王冠斌副理事長表示,由於個人長期經營國際醫療及食品投資計劃,故此次台越醫藥合作計劃的進展,已達成企業落地合作的目標,未來將進一步增進台灣與越南的落地合作計劃推展。另外,我國醫療及食品業者,對於東協市場,如馬來西亞、印尼及新加坡,因現行政治上的地緣風險考量,已是企業不得不的選擇區域,因此如何提供台灣業者在投資計劃、法規要求、稅務規劃及勞動人權等議題,都是所有企業主應事先了解及藉由訪拓的過程中,才有機會找到最適合自身條件的海外佈局,其注意之相關條件,不可不慎。CBIA越南分會長黃振綱先生(現任亞太搜尋引擎產業協會理事長)為深耕越南的台灣企業家,本次安排與越南台灣商會聯合總會的交流,分享寶貴經驗,強調在初期進軍市場時,台商定會遇到『金流、物流、文化差異』等問題。解決金流是第一步,要先有在地的銀行帳戶作為開始,其次就是越南網頁進行行銷等...利用Google大數據技術,可以加快進入市場!▲ CBIA協會拜會越南台灣商會聯合總會醫師越南執業符合南向政策 台灣醫療具備優勢台灣整合醫學推廣協會劉士銘理事長,也是台北卓越健康診所抗衰老權威醫師,在活動後表示:台灣醫療量能充沛,醫療專業知識及技術堪稱全亞洲第一,當越南市場經濟增長趨勢加速的時刻,台灣應該善用醫療專業,結合在地經營台商的高度優勢,發展台灣-越南雙向連續性照護的國際醫療模式,包括再生醫療..等各式整合醫學的優質醫療模式導入,營造追求兩地全民健康的大健康醫療產業發展。台灣生技醫藥之光 揮軍東協澄交生技(創櫃7627) 鍾齊賢總監提到腸道菌篩菌養菌平台及獨家包埋技術運用於「癌症輔助治療新藥開發」及「功能性保健食品的研發與銷售」,越南市場的模式係台灣原料研發,胡志明GMP廠生產取證,經越南本地電視購物銷售並銷往美國及星馬。此次參加Medi-Pharma醫療展,深度了解越南當地醫療市場,更與當地大醫聯合診所交流,進一步增進醫療產業合作契機。後續將著手進行醫師合作搭配電商系統的布建及精準關鍵字行銷,以深耕越南市場。成富生物科技公司大陸區林大翔總經理表示公司致力於生物科技領域研發、生產和銷售,長期在兩岸三地深耕當地市場,產品廣受市場好評。感謝CBIA參訪團對接越南企業商務考察和落地深耕事宜,讓台灣業者對越南市場有更進一步了解。杏福醫藥李昆錦總經理表示協會持續推動台灣醫藥產業的國際化腳步,不僅在亞洲地區,更將拓展全球範疇的對外交流合作活動,為台灣生技醫藥行業的全球影響力增添新的光彩。▲CBIA協會參訪LIFT GIFT GMP廠並簽訂MOU台灣智慧健康技術 發表Face AI技術日康科技潘宗賢總經理開發的Face AI技術,利用人工智慧臉部辨識無接觸式技術偵測生理數據如血壓、血氧、心率、心率變異及壓力指數,在2023越南醫療展收穫滿滿,除開拓印尼及馬來西亞經銷市場,另將與越南大醫連鎖診所合作開發遠距醫療平台,導入日康Face AI服務,另與越南Life Gift集團合作,結合Face AI服務銷售健康食品(台灣澄交生技委託生產)。藥師全聯會簡明龍常務理事表示越南是東協新興市場,龐大的人口基數和迅速增長的經濟實力,對台灣醫藥產業來說,帶來無限吸引力的發展機會,晶準生技陳意安總經理也感謝本次CBIA參訪團與當地政府、企業界等多方進行深入交流與對接,希望能夠建立起長遠穩固的合作關係,實現雙贏的局面。三年磨成劍,帶領我國醫療及食品產業跨海新模式中華生技醫療行業協會,成立至今除為政府機關認可之計劃單位外,並舉辦多次國際外交投資論壇,因此更奠定產、官、學、訓及外交新視野,故更受國內業者所倚重。國際競爭這幾年更是地緣政治下,各企業的重中之重,醫療及食品行業更是國力呈現的指標,張意良秘書長表示近日印度及越南政府的產業媒合會議邀約,指定CBIA列為首選的醫療產業訪拓對象,協會更積極提供國際投資及訪拓機會,以強化我國醫療及食品之國際競爭力,以不負會員之期許。
全球首見!鼻腔噴劑激活副交感神經分泌淚液 乾眼症治療新選擇
東生華製藥總經理楊思源今(11)日宣布,將開拓新治療科別進軍眼科治療領域。根據調查發現,目前台灣約有300萬的民眾受乾眼症所苦,看準目標市場,東生華在眼科的首發產品是由美國Oyster Point Pharma所開發用於治療乾眼症的新藥。乾眼症是一種以淚膜受損為特徵的眼睛表面多因素疾病,須持續治療與保養。而人類天然淚膜則能保護和滋潤眼睛,洗去異物,含有生長因子和抗菌成分,形成光滑的表面,形成眼睛的主要屈光面。現行治療選擇卻無法完全滿足患者需求,因此東生華引進全球第一個乾眼症治療鼻腔噴霧劑,其中的活性成分Varenicline,通過結合菸鹼型乙醯膽鹼(nACh)受體而發揮作用。當受體活化後,三叉神經副交感神經通路被激活,導致天然淚液分泌增加,從而達到治療乾眼症的目的。透過新的給藥途徑,藉此增加天然淚液分泌,適用於輕度至重度的乾眼症患者,提供更簡便、安全的用藥選擇。根據2項臨床試驗共940名乾眼症患者使用資料顯示,患者平均在僅使用一劑後就有淚液分泌的增加,在使用2週期間,患者的乾眼症症狀和癥兆有明顯改善,使用4週後平均產生的天然淚液量仍然顯著增加。透過乾眼症治療鼻腔噴霧劑來增加天然淚液分泌,為乾眼症患者帶來更好的治療反應與感受,目前已在2021年取得美國FDA新藥許可證並上市,東生華與箕星今年正式簽約並啟動在台灣的查驗登記及後續的銷售準備。

4家中企涉嫌販運芬太尼原料!遭美司法部起訴 北京:為鴉片危機找代罪羔羊
美國司法部長賈蘭德(Merrick Garland)於美東時間23日宣布,美國政府依販運用於製造芬太尼(fentanyl)的化學原料為名,起訴4家中國公司和8名隸屬這些公司的中國主管及員工。對此,北京當局也指出,華府正在透過此舉轉嫁國內的鴉片成癮危機。據《半島電視台》的報導,其中2名中國人已遭逮捕。美國司法部擴大打擊這種合成鴉片類藥物,這類藥物過去10年已導致數十萬人服藥過量而死亡。這標誌著美國首次在境內起訴販運芬太尼先驅化學品至美國和墨西哥的中國公司及個人。賈蘭德指出:「司法部永遠不會忘記那些被芬太尼荼毒的受害者,我們永遠不會停止追究那些該負起責任的相關人士」。他還指控這些公司及員工故意合謀生產致命的芬太尼,並在美國進行分銷,「僅其中1家中國化學公司已運送200多公斤的芬太尼相關先驅化學原料至美國,目的是為製造50公斤的芬太尼,如此的芬太尼致命劑量足以殺死2500萬美國人。」報導指出,美國國內的毒品問題已持續數十年,根據美國疾病控制與預防中心(CDC)的數據,光是在1999年至2020年期間,就有超過56.4萬美國人因服藥過量而死,近年來逐漸流行的芬太尼更是加劇了這場危機,例如2021年,美國因服藥過量而死的人口竟來到了驚人的10.7萬人,其中有超過7萬是死於芬太尼和其他合成鴉片類藥物。《半島電視台》則表示,實際上,美國藥品生產商積極推銷「奧施康定」(OxyContin)等高度成癮的止痛藥,也是引發這場鴉片危機的罪魁禍首之一。普度製藥(Purdue Pharma)持有者薩克勒(Sackler)家族成員就曾在2020年底於國會視訊聽證會上作證時承認,強力處方止痛藥「奧施康定」確實助長了美國的鴉片類藥物氾濫危機。對此,中國駐美大使館發言人劉鵬宇也在美東時間23日駁斥華府的指控,並諷刺華盛頓正在為國內的毒品危機尋找代罪羔羊,同時他也譴責美國司法部門的措施是違反國際法的「長臂管轄」、是美方精心策劃的陷害行動,嚴重侵犯了相關企業和個人的合法權益,「中方對此予以強烈譴責。」

綠膿桿菌汙染人工淚液持續延燒 81人受害14人失明4人死亡「活摘眼球求保命」
美國疾病控制與預防中心(CDC)19日表示,今年稍早傳出的人工淚液遭到綠膿桿菌污染的事件持續延燒,目前又添增1名死亡病例,目前整體受害人數達到81人,其中4人死亡、14人失明,其中有4人為了保全性命,不得不接受眼球摘除手術。根據《NBC》報導指出,整起事件從3月份爆發,當時就傳出有68人受害。而截至目前為止,受害人數更是擴大到81人,近期又更是添增了1名死者。CDC相關小組負責人沃爾特斯(Maroya Spalding Walters)受訪時表示「這是一場堪稱災難性、嚴重改變生活的感染事件」。報導中也指出,目前問題產品已經被證實有印度Global Pharma Healthcare製造的EzriCare人工淚液、Delsam Pharma人工淚液和 Delsam Pharma的軟膏。雖然廠商已經早在2月份就開始召回問題產品,病例也有所放緩,但CDC推測,未來的相關病例數應該會持續增加。目前在美國18個州已經出現相關病例,其中包含加利福尼亞州、科羅拉多州、康涅狄格州、特拉華州、佛羅里達州、伊利諾伊州、北卡羅來納州、新澤西州、新墨西哥州、內華達州、紐約州、俄亥俄州、賓夕法尼亞州、南達科他州、德克薩斯州、猶他州、華盛頓州和威斯康星州。

疫苗又惹議2/食藥署護稱藥品具關鍵製程 高端卻打臉自承分裝充填
立委王鴻薇、李德維與中華民國防疫學會榮譽理事長王任賢日前質疑,蔡政府為了拯救營收歸零的高端公司,對該公司的四價流感疫苗大開後門。高端對此聲明表示,高端疫苗代理的GC Biopharma 四價流感疫苗已完成臨床試驗,以「成品銷售」或「分裝充填」方式供應市場,並揚言提告;但衛福部食藥署發新聞稿替高端辯護時卻指稱,此疫苗是高端在「國內進行藥品關鍵製程製造」。對於高端的聲明,王鴻薇反問,國內4家四價流感疫苗供應中「除了國光是本土疫苗外,其他引用國外的疫苗,大家都是原裝進口,為什麼只有高端是原液到台灣填充分裝,且可以順利取得藥證,高端是不是破例了?」她質疑,高端從去年營收一路下滑,到今年一月、二月掛零,衛福部為了要救高端,才開方便之門,讓高端分裝韓國疫苗,並以自有品牌的國產疫苗之姿參與公費疫苗競標。高端公司在29日的聲明中指出,高端與韓國疫苗大廠GC Biopharma於2018年4月簽約啟動,由高端疫苗代理GC Biopharma四價流感疫苗,以成品銷售或分裝充填方式供應市場。而食藥署則在同日發布新聞說,「高端四價流感疫苗」為高端疫苗生物製劑股份有限公司與韓國GC Pharma 合作,於國內進行藥品關鍵製程製造之國產疫苗。高端說自己「成品銷售或分裝充填」,但食藥署則說高端做了「關鍵製程」,相當耐人尋味。高端公司聲明指出,高端與GC Biopharma的合作並非只是產品進口代理,而疫苗產品最終成品的無菌製程分裝,也是十分常見的產業鏈專業分工事項。(圖/翻攝自高端疫苗生物製劑公司官網)王任賢指出,高端從原本要進口成品,後來又改成進口原液填充,質疑是要「洗產地」,用「假國產」來搶占比例最高的真國產市場。一位疫苗界人士同意這種推論,但他認為高端當初送衛福部食藥署審核的,是韓國GC Biopharma的「GC FLU Quadrivalent原廠進口疫苗,在台進行第三期臨床試驗的也是進口產品,但日前取得藥證的卻是「高端四價流感疫苗」(MVC FLU Quadrivalent),很難說得通,況且,若按食藥署所說,高端進行了「關鍵製程」,新的「國產疫苗」豈不是更應該重新做試驗?這位人士指出,高端應該也知道這個漏洞,因此僅管想自我包裝成「國產疫苗」,卻聲明指出是以「分裝充填方式供應市場」,強調所推出的疫苗與已通過三期臨床試驗的韓國GC Biopharma的製品是相同一款;但食藥署官員護高端心切,卻指「高端四價流感疫苗」是高端疫苗生物製劑股份有限公司與韓國公司合作,於國內進行藥品關鍵製程製造之國產疫苗,還說「高端四價流感疫苗」已通過一、二、三期試驗。「去查一下當初在韓國做一、二期試驗的疫苗名稱,以及在台灣做第三期的疫苗名稱,看是不是『高端四價流感疫苗』,就知道官員有沒有護航、衛福部是不是開後門了。」這位人士酸說,食藥署官員是想護航,硬把分裝充填說成關鍵製程。王任賢指出,高端進口韓國流感疫苗廠的原液,並以韓國的臨床實驗結果取得台灣流感疫苗的藥證,雖然不能說有錯,但審核過程並不完全完美,並可能造成國內疫苗削價競爭。圖為桃園民眾接種流感疫苗。(圖/報系資料照)

人工淚液遭汙染!美國已3人「點入眼喪命」 出現6症狀要小心
今年2月初才傳出,一款由美商醫藥公司「EzriCare」生產的非處方人工淚液,出現汙染問題,被強制回收下架後,美國陸續傳出,有多款人工淚液感染綠膿桿菌的通報。根據美國疾管中心(CDC)本月21日所發布的最新聲明稿指出,目前全美共有16州、68人因使用汙染的眼藥水而受感染、並有3人因此喪命,呼籲使用EzriCare與Delsam Pharma兩家人工淚液相關產品的民眾,要注意眼睛是否出現不正常的分泌物。根據美國疾病管制暨預防中心(CDC)截至本月21日的統計,全美已有16州,累計68例的個案,因使用上述兩家業者出品的人工淚液,感染了綠膿桿菌,死亡個案累計已3例,另有8人失明、4人須接受手術摘除眼球。美國CDC指出,感染病例使用的人工淚液品牌數至少超過10種,但發現使用EzriCare人工淚液而被感染的患者占最多。CDC提出示警呼籲,手邊若有這些出問題人工淚液的民眾,最好立即停用。CDC提醒,如果曾用過EzriCare與Delsam Pharma出品人工淚液的民眾,務必注意眼睛是否出現像是黃、綠或無色分泌物,眼睛疼痛,眼睛或眼皮發紅,眼睛有異物感,眼睛變畏光,視野變模糊等變化,若有上述情形者,應儘速就醫。
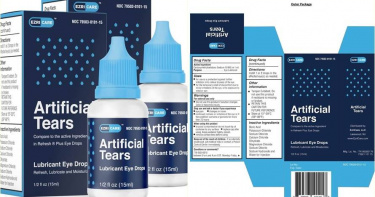
美國知名人工淚液細菌感染釀1死 食藥署回應這樣說
美國食品暨藥物管理局(FDA)近日發出公告,表示由印度藥廠Global Pharma Healthcare推出的人工淚液品牌EzriCare,發現高度抗藥性的綠膿桿菌(Pseudomonas aeruginosa)感染,已影響12州並有55名病患感染,甚至出現首起死亡案例,如今台灣食藥署也對這款人工淚液做出回應。綜合外媒報導,人工淚液品牌EzriCare發現受到細菌感染,當中發現有高度抗藥性的綠膿桿菌(Pseudomonas aeruginosa),雖然還沒有證明細菌感染跟產品有所關聯,但已在美國12州有1死55感染,FDA也以「缺乏測試和適當包裝」為由下架禁售。衛福部食藥署今(4)日也表示,經清查後發現這項產品,並沒有核准輸入台灣,會持續注意國際間警訊。而振興醫院感染科主任兼任感染管制室主任李明政表示,綠膿桿菌是「很惡毒的細菌」,這種細菌擴散快速,一旦感染必須使用特殊抗綠膿桿菌的抗生素才能治療,因此在臨床間常發生延誤就醫,治療的關鍵時間是3日內。

這款「人工淚液」含綠膿桿菌!全美12州爆大規模感染 造成1死、5失明
俗話說眼睛是靈魂之窗,不少愛美女性習慣戴隱形眼鏡,若是感覺乾澀便會使用人工淚液舒緩,不過恐怕會有失明風險。美國疾病管制與預防中心(CDC)周四(2日)表示,一款名叫「EzriCare」的人工淚液,在全美12個州爆發感染,造成1人死亡、5人永久失明。綜合外媒報導,由印度藥廠Global Pharma Healthcare製造的人工淚液「EzriCare」,被驗出內容物含有極高抗藥性、可存活在42℃環境下的「綠膿桿菌」(Pseudomonas aeruginosa),目前CDC已勒令下架、回收問題產品,並要求所有醫療機構及病患都應立即停止使用。報導指出,包括加州、科羅拉多、康州、佛州、新澤西、新墨西哥、紐約、內華達、德州、猶他、華盛頓及威斯康辛等12個州,至少55人遭到感染,其中1人不幸病逝,另有5人永久喪失視力,多數患者的血液、尿液和肺部均出現感染現象,且在感染前都曾使用過「EzriCare」的人工淚液。對此,負責在美國經銷該產品的EzriCare公司則表示,目前尚未有證據顯示,該波群聚感染與人工淚液有直接相關,但已停止銷售該款人工淚液。

甘比亞66名兒童死於急性腎衰竭 恐與印度製造咳嗽糖漿有關…世衛展開調查
甘比亞近日有數十名幼兒死於急性腎衰竭,世界衛生組織(WHO)透露,這可能與印度製藥商生產的受污染的咳嗽糖漿和感冒糖漿有關,目前聯合國機構已展開調查。此外,世衛組織也要求監管機構將Maiden Pharma產品從市場上撤出。根據路透社報導,在對幾種藥用糖漿進行測試後,世界衛生組織總幹事譚德塞(Tedros Adhanom Ghebreyesus)表示,這些藥用糖漿被懷疑在這個西非小國造成66名兒童死亡。譚德塞提及,聯合國機構正在與印度監管機構對總部位於印度首都新德里的Maiden Pharmaceuticals Ltd. 展開調查。而針對此事,Maiden Pharma拒絕回應,目前印度衛生部也沒有回應。世衛組織5日發布醫療產品警報,要求監管機構將Maiden Pharma產品從市場上撤出。世衛組織指出,這些產品可能已通過非正規市場在其他地方分銷,但迄今為止僅在甘比亞被發現。警報涵蓋4種產品,包括異丙嗪糖漿、Kofexmalin嬰兒止咳糖漿、Makoff嬰兒止咳糖漿以及Magrip N感冒止咳糖漿。世衛組織表示,實驗室分析證實,二甘醇和乙二醇的含量「不可接受」,它們可能有毒並導致急性腎衰竭。在數十名兒童開始出現腎臟問題後,甘比亞醫務人員於7月發出警告。在出現一種模式之前,這些死亡讓醫務人員感到困惑,數十名5歲以下的患者在服用當地銷售的撲熱息痛(Paracetamol,乙醯胺酚)糖漿後,3至5天開始出現狀況。甘比亞衛生服務主任Mustapha Bittaye直言,在其他糖漿中也發現了類似的問題,但衛生部正在等待結果的確認。他說,「最近幾周死亡人數逐漸減少,並且禁止銷售Maiden Pharmaceuticals生產的產品。然而,直到最近,一些糖漿仍在私人診所和醫院出售。」