仁新醫藥
」
新藥股大漲跌1/這二檔營收利多股價亮眼 「它」納入中國目錄成亮點
台股力拼站回28K,AI概念股仍是主旋律,大數據分析等科技導入生技醫療產業也加速新藥研發進程,臨床試驗數據一翻兩瞪眼好壞在眼前,CTWANT調查2025年股價亮眼上漲與慘跌共四檔新藥股,2026年展望是個個有希望,最關鍵的還是營收財報給證據。 先來看看最新一例,2025年12月7日中國國家醫保局公布首版《商業健康保險創新藥品目錄》,納入18家企業19款高值創新藥,聚焦CAR-T、雙抗、罕見病及阿茲海默症等超出基本醫保範圍的產品,研發PTS肺癌新藥的共信-KY(6617)子公司天津紅日健達康醫藥科技公告「治療中央型氣道阻塞產品-PTS302」,成為台股唯一上榜個股,消息曝光,股價從78.8元上漲到86.6元,旋即又短暫下跌86.4元,再逐步漲到15日收盤價90.5元,到這周連四跌、周五收盤價85元。 CTWANT調查,共信12月3日公布11月合併營收259.1萬元,年減12.5%,累計雖年增11.42%,但投資人擔憂目錄效應需時間轉化實際訂單。 至2025年12月15日止,觀察仁新醫藥(6696)、藥華藥(6446)個股股價變化,其均以創新藥為核心,近期受臨床進展、營運利多驅動,股價有所表現。仁新醫藥近一月從270元上漲到最高442元,近三月則從162元漲到周五收盤407元;藥華藥近一月從453元漲到最高519元,近三月則最高漲到559元。仁新醫藥專注罕見疾病新藥,子公司Belite Bio(美國納斯達克BLTE)Tinlarebant三期臨床於2025年12月1日公布,針對青少年斯特格病變臨床三期試驗(DRAGON)解盲之關鍵性數據亮眼,共收案104位青少年受試者,並成功達成主要療效指標。Belite董事長暨執行長林雨新醫學博士表示,「DRAGON最終試驗結果讓斯特格病變疾病治療迎來了歷史性突破,Tinlarebant將成為首個治療這種具威脅性疾病的潛在新藥,期盼藉此帶給無藥可醫的患者及其家屬治療新希望。」BLTE股價從今年初低點62.09美元,漲到近期的最高點156美元,「三期解盲成最大催化劑。」證券分析師表示。Belite規劃於2026年上半年與各國監管機構討論Tinlarebant的潛在後續計畫與新藥查驗登記申請(NDA)送件事宜,並向美國FDA遞交新藥查驗登記申請(NDA)。Belite宣布Tinlarebant抑制視網膜萎縮進展達預期,股價飆至新高,仁新持股 43.94%間接受惠,募資126億元不折價增資當日完成。仁新2026年關鍵為Tinlarebant FDA核准,預計上半年送NDA。藥華藥向美國FDA申請Ropeg新適應症「原發性血小板過多症(ET)」,目標2026上半年取證。圖左起為執行長林國鐘、董事長詹青柳、總經理黃正谷。(圖/CTWANT資料照)藥華藥旗下真性紅血球增多症(PV)新藥Ropeginterferon alfa-2b(Ropeg,P1101)用於新適應症罕病血癌藥銷售勁揚,股價高檔震盪,10月底完成向美國FDA申請Ropeg新適應症「原發性血小板過多症(ET)」送件,若順利獲准,最快有望於2026年上半年取得美國ET藥證,成為公司啟動第二成長曲線的重要動能。藥華藥11月營收15.5億元,月增10.63%,年增53.02%,已連續3個月刷新單月歷史新高;累計前11個月達137.11億元,較去年同期的86.02億元,成長59.38%;前三季獲利達35.69億元,年增翻倍,每股盈餘9.66元,賺近一個股本。根據CTWANT調查,藥華藥也正同時研發新款癌症藥物。此外,Ropeg筆型注射劑的補充性生物製劑查驗登記申請(sBLA)審查亦同步進行中。FDA已通知審查目標完成日(PDUFA date)為2026年2月14日。

仁新白血病新藥獲FDA快速審查認定 董座:加速推進具潛力療法
仁新醫藥(6696)27日公告,旗下治療急性骨髓性白血病之新藥LBS-007獲美國食品藥物管理局(FDA)授予快速審查認定(Fast Track Designation),這是目前台灣第一家新藥公司取得的急性白血病快速審查認定,董事長林雨新博士表示,此認定為推進LBS-007具潛力的療法提供了加速途徑。仁新今天收盤價140.00元,下跌12.17元,跌幅達8.00%。仁新醫藥於2022年4月底由子公司Belite Bio(那斯達克股票交易代碼:BLTE)以每一單位發行價位6美元在那斯達克掛牌,目前股價來到64.02美元,下跌11.32美元,跌幅達15.03%。仁新指出,根據此項認定,LBS-007可獲得與美國FDA更頻繁的會議與書面溝通諮詢,在符合美國FDA相關條件下,將可再獲得加速核准(Accelerated Approval)與優先審查(Priority Review),並可在執行臨床三期試驗期間,透過滾動式審查(Rolling Review),先行提交新藥查驗登記申請(NDA)所需相關文件供審,除有助於加速未來美國藥證申請與審查之時程,亦有利於藥物及早上市。仁新總經理王正琪博士表示,在LBS-007臨床一期劑量遞增試驗中,目前所有劑量給藥的受試者都並未發生確定或極有可能相關的不良反應(Definitely or Probably Related Adverse Effects),這顯示出LBS-007的安全性及耐受性良好,將為急性白血病患者帶來治療的新希望。LBS-007先前已取得FDA授予急性淋巴性白血病(Acute Lymphocytic Leukemia, ALL)與急性骨髓性白血病(Acute Myeloid Leukemia, AML)孤兒藥資格認證,仁新也將藉由法規優勢為全球急性白血病病患加速藥物的開發及上市。

太強了!這家公司7年前轉投資電動車 SPAC上市大賺11倍
俗稱「空殼公司」的SPAC近兩年在美國股市成主流,現在更因電動機車一哥Gogoro宣布採取SPAC方式在美國上市,蔚為市場熱門話題。其實,兩個月前上櫃公司淳紳(4529)就已是SPAC受惠公司之一,收割7年前投資電動車產業Atieva,進而持有美股「Lucid Group,Inc.(LCID)」,較原始投資獲益達近11倍。SPAC這股風潮也吹進台灣!根據公開資訊關測站,國內上市櫃等公司陸續傳出正研議透過SPAC讓子公司在海外市場籌募資金上市。今年5月,牛仔褲代工大廠如興(4414)董事會決議為提升投資效益,進行集團旗下9家公司組織重組案,尋求子公司分項打包赴美掛牌上市機會,並已在9月中成立申請海外掛牌審議特別委員會,如興發言人陳怡如即說,「已經有美國的SPAC向如興詢問子公司掛牌相關事宜」。興櫃的仁新醫藥(6696)則於今年9月初公告,為了籌募資金,研議子公司Belite採取SPAC在海外掛牌上市案。兩周後的9月16日,Gogoro更是宣布將與SPAC的Poema達成併購協議,預計明年第一季在納斯達克以股票代碼「GGR」上市,估值上看23.5億美元(約新台幣650.5億元)。俗稱空殼公司的SPAC(Special Purpose Acquisition Company),是一種「特殊目的收購公司),近兩年新創公司受到疫情衝擊不僅在成本大增,也增加上市難度,因此國外法規允許的一種「沒有業務,無虧損而言的乾淨新殼SPAC」,可縮減上市時間等,成為許多新創科技上市的選項,包括Grab、WeWork等都以此模式順利掛牌。(圖/翻攝官網)淳紳(4529)董事長沈瑋也提到,過去讓很多人不了解的SPAC,現在也讓淳紳有機會在2013~2014年的一項轉投資計畫中,成為SPAC間接受惠者。沈瑋是在美國取得會計碩士,曾任國際四大會計師事務所之一、安侯建業會計事務所(KPMG)的全球合夥人,2011年入主淳紳投入電動車產業至今,研發與建立產線等過程中亟需龐大資金與人才等,同時也踏足歐美、中國大陸等與建立發展電動車公司合作,其中就還包括投資電動車產業Atieva的轉投資計畫。沈瑋指出,他很早就嗅到「電動車」產業前景看好,2014年3月,Atieva是一家量產第一部電動車的公司,他認為Atieva擁有開發技術能力,就在Atieva啟動海外募資計畫中,他參考其他投資者的方式,以淳紳與淳紳子公司明洧透過投資私募基金Sino-JP Fund發行的CLASS D型股票5萬股,約美金322萬多元,間接持有Atieva 50萬特別股。Atieva後更名為Lucid Motors,在今年獲得美國上市公司Churchill Capital Corp.IV投資(即為SPAC公司),7月23日兩家公司合併後的美股代碼為LCID,間接投資的股票市值以6月29日收盤價計算,約達3,415萬多美金,較原始投資322多萬美金獲益近11倍。淳紳目前卡在增資進度受阻,面臨營運資金不足也還未做到生產階段,加上財務操作深陷檢方指控的掏空案疑雲,「淳紳尊重司法調查,深信司法終究會還經營團隊的清白,也希望能體會淳紳發展電動車的努力」沈瑋說。7年前淳紳轉投資Atieva計畫,如今SPAC上市手法而有了撥雲見日的突破,對淳紳來說,總算有個好消息。(圖/翻攝官網)
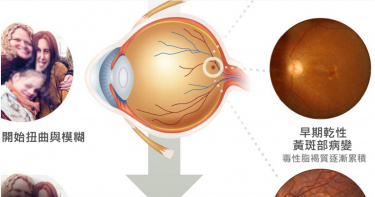
剛撤件就轉往海外上市 仁新醫藥急籌資
仁新醫藥(6696)才自證交所撤件創新板上市申請案受到投資人關注,今天(1日)召開董事會,董事長暨執行長林雨新晚間宣布,正考慮以子公司Belite於日本、香港、美國、澳洲等地上市,作為募集資金、擴展融資管道及業務,推進臨床試驗、增強公司全球競爭力與知名度。仁新醫藥晚間近9時發布重訊,說明今日董事會決議通過以子公司Belite Bio Inc考慮海外上市之案,若Belite特別股股東全數行使轉換為普通股,仁新醫藥持有Belite80.10%。若再假設該子公司給與之認股權全數經執行轉換為普通股,仁新醫藥對Belite之持股比例將稀釋為66.88%。仁新醫藥今天罕見地以4千多字說明Belite上市案的緣由與規劃,董事長暨執行長林雨新表示,本次提請股東會表決Belite赴海外上市案,主要係因日前撤件台灣創新板上市申請案,預期短期內要在台灣資本市場取得較大規模之融資以支持子公司Belite推進其他,例如乾性黃斑部病變之臨床試驗有所難度。林雨新指出,若因無法及時籌措所需資金,導致開發延宕或是中斷,將可能錯過關鍵市場機會,因此擬啟動Belite赴海外上市之計畫以創造多元籌資管道,並根據上市櫃公司標準,提請股東會表決。若可於短期內獲得股東或特定人提供後續較大規模之臨床試驗資金,則Belite亦有可能不需啟動海外上市。林雨新也進一步說明,仁新目前研發進度最快之新藥LBS-008相關授權技術及臨床試驗資料均由Belite所擁有,先前Belite發行權益證券已致仁新對其持股比率最大可能降至66.88%。由於新藥開發之臨床試驗一旦啟動,若無資金完成則會前功盡棄,仁新目前僅LBS-008之研發進度較快,便是受限於集團之融資能力無法同時開展多個臨床試驗。仁新本次擬啟動Belite海外上市,亦是希望可以藉此減輕仁新對Belite之財務支持,讓仁新得以啟動,例如透過全癌症技術平台CDC7(Cell Division Cycle 7, 細胞分裂週期7)所開發的癌症新藥LBS-007之臨床試驗,CDC7是新一代的抗癌標靶,預計除急性白血病,亦可能應用於多種難以治癒的實質腫瘤,創造股東價值同時亦分散臨床試驗風險。