注射部位
」 疫苗 BNT 莫德納 副作用 新冠疫苗
酒店業掀「瘦瘦針」風潮!3成小姐冒副作用求速瘦
台灣醫美市場近期掀起1波「瘦瘦針」熱潮,主打快速減重效果,吸引大批追求身材管理的女性投入,其中以需長時間維持外型的族群最為顯著。南部1名酒店業幹部直言,即便明知施打或服用後可能出現強烈副作用,包括喝酒容易嘔吐、長期甚至掉髮,仍有至少3成酒店小姐持續施打瘦瘦針或服用相關瘦身藥物,可見這股風潮已深入特定行業。對此,台南市衛生局提醒,瘦瘦針屬於處方用藥,必須經醫師評估並開立處方後使用,民眾切勿自行購買或忽視潛在風險。據《中時新聞網》報導,所謂瘦瘦針,原本用於治療糖尿病患者,近年被延伸應用至體重控制領域,並迅速在醫美市場擴散。市面上品牌眾多、價格差距不小,甚至出現以口服方式取代注射的瘦瘦藥。由於取得管道相對容易,網路上也能見到價格低廉的販售訊息,但這些藥品來源不明,品質與安全性難以保障,卻仍吸引不少人鋌而走險購買。除了肥胖族群外,許多需要在短時間內維持纖細體態的女性也成為主要使用者,尤其在8大行業內更形成1股風潮。有酒店小姐透露,工作型態需徹夜陪酒應酬,作息顛倒且飲食不規律,身材容易走樣,而能快速抑制食慾、降低體重的藥物,正好符合職業需求。南部1名酒店業幹部坦承,店內超過一半女性幹部都有施打經驗,近百名酒店小姐中約3成長期使用體重控制藥物,有人選擇打針,也有人改採口服方式。1名A酒店小姐表示,施打後食慾被大幅抑制,原本能吃完的便當如今不到1/3就飽,連酒都難以入口,1罐都喝不完,多喝1口甚至會立刻嘔吐。她指出,第1個月體重就減少5、6公斤,效果相當明顯。不過為了不影響陪酒工作,有些女同事會選擇在休長假期間施打,待體重下降後再回到職場,或改服效果較弱的瘦瘦藥,以免在工作時頻繁嘔吐。另1名長期施打的酒店女幹部體重已減少約10公斤,但也持續承受副作用折磨,包括反覆嘔吐與掉髮問題。她坦言,為了維持工作表現只能繼續施打,只是將原本1週1針的頻率延長為2週1針,以減緩身體負擔。她也無奈表示,一旦停打食慾就會迅速恢復,「吃了還是會變胖」,彷彿陷入難以抽身的循環。根據衛生福利部食品藥物管理署統計,近3年台施打瘦瘦針後通報的疑似藥物不良反應案件共21件,症狀包含腸胃不適、低血糖、噁心、嘔吐及注射部位不適等。食藥署指出,目前尚未觀察到整體安全性出現異常或新增風險趨勢,但仍提醒民眾使用前應充分了解可能的副作用,並在專業醫療監督下進行。衛生局強調,瘦瘦針屬處方用藥,必須經醫師醫療評估後開立處方,再由藥師調劑給藥,多數產品仍限成人使用,並須符合身體質量指數(BMI)等適應條件。民眾切勿透過來路不明的網路或私人管道購買,以免取得偽劣藥品,或在不符適應症的情況下使用,對健康造成不可逆的傷害。

瘦瘦針國內21件不良反應通報 食藥署示警4事:誤用傷身
全球近年掀起瘦瘦針減重風潮,也引發相關安全性討論。衛生福利部食品藥物管理署今(7)日說明,國內近三年共接獲21件瘦瘦針疑似不良反應通報,包含腸胃疾病、低血糖、噁心、嘔吐及注射部位不適等,尚未觀測到藥品整體安全性異常趨勢。不過食藥署示警,該藥品須經專業醫療評估後開立處方,也須符合BMI等使用條件,民眾不可從非正規管道自行購買使用。近期國際新聞報導,美國有數千名GLP-1受體促效劑類藥品(俗稱瘦瘦針)使用者因嚴重副作用提起大規模訴訟,而英國藥物及保健產品管理局亦於近期發布安全警訊,提醒該類藥品可能有引發嚴重急性胰臟炎的風險,包含罕見的壞死性和致死性胰臟炎案例。食藥署強調,瘦瘦針屬處方用藥,須經醫師專業醫療評估開立處方,並經藥師調劑後給藥,民眾切勿透過網路或來路不明管道購買,以免因買到假藥或劣藥及不當使用,減重不成反而危害自身健康。食藥署進一步說明,目前我國核准用於「體重控制」之GLP-1受體促效劑類藥品共3種成分,包括tirzepatide、semaglutide及liraglutide。統計自全國藥物不良反應通報系統,自2023年1月1日至2025年12月31日止,共接獲21件疑似不良反應通報,症狀包含腸胃疾病、低血糖、噁心、嘔吐及注射部位不適等,目前尚未觀測到藥品整體安全性出現異常或新增風險趨勢,但民眾使用瘦瘦針仍應留意可能的副作用風險。食藥署提醒,部分瘦瘦針經醫師評估可用於12歲以上青少年,但多數仍限成人使用,且須符合BMI等使用條件。使用前應與醫師充分討論並接受評估,使用期間如出現疑似不良反應,應儘速就醫。食藥署亦將持續掌握國內外安全警訊,必要時啟動安全性再評估,以確保民眾用藥安全。食藥署提醒,瘦瘦針勿網購、須醫師開立並留意不良反應。(圖/食藥署提供)

愛刺青要知道!墨水源自工業塗料 研究發現恐影響免疫反應
從手腕上的極簡線條或是整隻手臂的彩色刺青,這種人體藝術早已成為現代社會的日常風景。然而國外科學家提醒,刺青帶來的不只是外在風格,刺青顏料進入體內後,可能與免疫系統產生複雜交互作用,也會在體內累積,恐怕對長期健康狀況有影響。根據外媒《ScienceAlert》報導,近期一項研究指出,刺青時注入皮膚真皮層的顏料,會被人體視為外來物質;免疫細胞嘗試清除這些顆粒,但由於顏料顆粒過大,無法完全代謝,只能被「困」在皮膚細胞內,這也正是刺青能永久留存的原因。不僅如此,部分顏料顆粒還會隨著淋巴系統移動,累積在淋巴結中,引發外界對免疫健康的疑慮。刺青顏料並非單一成分,而是由多種化學物質混合而成,包括色素、溶劑、防腐劑及微量雜質。其中,不少色素原本是為工業用途開發,例如汽車烤漆、塑膠或印表機碳粉,並非設計用來注射進人體。部分刺青墨水還含有鎳、鉻、鈷,甚至鉛等重金屬,這些物質在特定濃度下具有毒性,也容易誘發過敏或免疫反應。此外,部分顏料含有偶氮染料與多環芳香烴(PAHs),研究顯示,偶氮染料在長時間日曬或雷射除刺青時,可能分解為芳香胺類化合物,實驗中已被證實與致癌及基因損傷有關;而常見於黑色墨水的多環芳香烴,部分也被列為致癌物。近期一項研究更指出,常用刺青顏料可能影響免疫活性,導致局部或淋巴結發炎,甚至在特定情況下干擾疫苗免疫反應。研究發現,當刺青顏料存在於疫苗注射部位附近時,可能降低新冠疫苗的免疫反應效果;不過,專家強調,這並不代表刺青會讓疫苗變得不安全,而是顯示顏料可能影響免疫細胞之間的訊號傳遞。目前尚無明確流行病學證據證實刺青會直接導致人類罹癌,但實驗室與動物研究顯示潛在風險。由於癌症往往需數十年才會發展,加上刺青盛行時間相對不長,使得長期風險更難評估。報導中,有醫界人士提醒,刺青最常見的健康問題仍是過敏與慢性發炎反應,尤其紅色顏料最容易引發長期搔癢、腫脹,甚至形成肉芽腫。這類反應可能在刺青完成數月甚至數年後才出現,日曬或免疫狀態改變都可能成為誘因。不僅如此,如同所有侵入性行為,刺青也存在感染風險,若衛生管理不佳,可能引發金黃色葡萄球菌、B型或C型肝炎,甚至罕見的非典型分枝桿菌感染。專家指出,目前全球對刺青墨水的管理仍不一致,許多國家對其規範遠不如化妝品或醫療產品嚴格。隨著刺青風潮持續擴大,呼籲加強成分透明度、法規管理與長期研究的聲音也日益高漲。刺青雖是自我表達的象徵,卻同時意味著終身的化學暴露,其潛在影響,仍值得社會與科學界持續關注。

告別巨痛針!免疫功坊TE-8214:從「麥芽糖」到「水溶液」的長效藥物革命
長效型胜肽藥物的發展,是現代醫學的一大福音,它顯著改善了病患的生活品質。然而,對於「生長激素分泌異常的相關徵兆」的病患來說,儘管現有治療藥物奧曲肽(Octreotide)已能緩解病徵,但長效型製劑的注射疼痛卻是難以言喻的夢魘。在【生活講堂】節目中,主持人—高葳(Stacey) 專訪了台灣免疫功坊(Immunwork)董事長、被譽為「台灣抗體之父」的張子文博士。張博士在訪談中深入揭示,他們正在研發的創新藥物TE-8214,目標就是要徹底解決這個困擾病患數十年的痛點。舊藥之痛:麥芽糖般的黏稠與結節為了將奧曲肽從原本只有1.5小時的短暫半衰期,延長到能數週注射一次的長效療程,現行市場上的長效緩釋劑(如 Sandostatin LAR)必須採用 Depot(儲藏物)的概念。張博士在節目中生動地形容,這種緩釋劑的劑型,在調製出來後,會變成一種「很黏稠的東西,看起來有點像麥芽糖」。這種極端的黏稠度帶來了災難性的後果:1. 粗針深層注射: 由於藥物黏稠難推,病患必須使用極粗的針頭(例如 18G 或 19G),並深層推入臀部肌肉中。張博士提及,有醫師反應,光是看到這種粗針,有的病患就可能害怕得想跑掉。2. 痛苦結節: 藥物在肌肉內釋放時,會在注射部位形成難以消散的硬塊或結節。這類硬塊可能需要數個月甚至一年才能緩慢消退,嚴重影響病患的日常活動和生活品質。新藥突破:脂肪酸束與白蛋白攜帶的長效機制免疫功坊的TE-8214代表了新一代長效藥物在技術與人文關懷上的雙重突破。張博士指出,TE-8214 運用公司獨有的「脂肪酸束的技術」對奧曲肽進行了全新的修飾,創造出獨步全球的創新藥物。最大的突破,在於劑型的徹底改變:TE-8214不再依賴聚合物形成的網狀結構來緩釋藥物,它本身就是水溶液型態。由於是水溶液,TE-8214可以使用極細的針頭(例如 30G,如同疫苗針般細)進行皮下注射,不再需要痛苦的肌肉深層注射,徹底減輕病患的疼痛。長效機制也更為精妙:TE-8214在被皮下注射後會迅速進入血液系統,並與血液中的白蛋白(Albumin)結合。白蛋白作為體內的攜帶者,將藥物攜帶在血液中,使半衰期延長。這種機制既達到了長效的目的,同時也完全避免了肌肉結節的產生。在專訪的最後,張子文博士強調,他的新藥研發不僅追求有效性,更追求人性化。TE-8214目前正在人體臨床試驗階段,一旦成功上市,將為病患提供一個「無痛、細針、不結節」的治療新選擇,讓病患能夠更積極、更有尊嚴地配合治療。
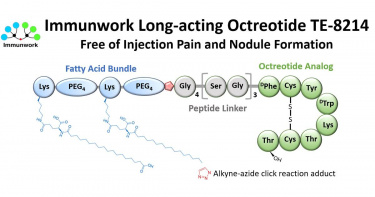
T-E Pharma旗下免疫功坊長效型奧曲肽新藥TE-8214 第一期臨床試驗證實有效改善注射不適、抑制發病生化指標IGF-1
T-E Pharma旗下之免疫功坊 (Immunwork, Inc.) 今日宣布,其自主研發的長效型奧曲肽新藥TE-8214已於澳洲順利完成第一期臨床試驗。結果顯示TE-8214具備良好的安全性與耐受性、可達成預期藥理機制,且皮下注射輕易,不產生施打部位副作用。TE-8214為免疫功坊運用專利平台技術開發之長效型奧曲肽 (octreotide) 類似物,經由在奧曲肽分子上連結含有兩條脂肪酸鏈的脂肪酸束,達成延長藥物半衰期,可應用於治療肢端肥大症與多種神經內分泌腫瘤所引致的病徵。上述兩類疾病常伴隨嚴重的內分泌失調,導致消化性潰瘍、嚴重腹瀉、氣喘、組織異常生長、關節疼痛與高血壓等症狀,若未妥善治療,將大幅影響患者的生活品質與壽命。(圖/免疫功坊提供。)隨著全球對奧曲肽藥物需求的增長,近年來相關市場規模持續擴大,預估2030年將達100億美元。現有市售與研發中的相關產品,多為高黏稠度微粒或凝膠狀緩釋劑型,須使用19G或20G的粗針頭進行肌肉 (如Octreotide LAR) 或深層皮下注射 (如Lanreotide Autogel),不僅施打困難,更易引發注射部位疼痛及結節等副作用,造成病患對治療的接受度與依從性明顯下降。(圖/免疫功坊提供。)免疫功坊創辦人兼執行長,先前發明多項創新藥物的免疫學家張子文表示:「TE-8214 完成第一期臨床試驗是免疫功坊的重要里程碑,也為肢端肥大症與神經內分泌腫瘤患者帶來新希望。TE-8214具備高水溶性,可透過30G細針頭進行皮下注射,大幅減輕患者注射時的疼痛與恐懼感。未來我們將憑藉此關鍵優勢,積極拓展全球奧曲肽市場,為患者提供更安全、更舒適的治療選擇。」TE-8214的第一期臨床試驗採雙盲、單劑量遞增設計,設有四個劑量組別 (0.6 mg、1.2 mg、2 mg及4 mg),每組納入8名健康受試者,其中6人接受TE-8214,2人接受安慰劑(生理食鹽水)。整體結果顯示TE-8214耐受性良好,僅出現輕微不良反應,未觀察到任何嚴重不良事件。常見的奧曲肽副作用為消化道不良反應,本試驗24位TE-8214受試者中,僅3人出現極輕微的消化道不適,證實TE-8214的安全性與耐受性表現優異。更重要的是,所有TE-8214受試者均未出現注射部位疼痛或結節情形,結果與安慰劑組的受試者完全相同,顯示TE-8214的劑型設計成功解決緩釋劑型的痛點問題。此外,奧曲肽類藥物主要透過抑制體內類胰島素生長因子 (Insulin-like growth factor 1, IGF-1) 濃度發揮治療效果。在本次試驗的高劑量組別 (2 mg和4 mg) 中,12位TE-8214受試者中有10位 (83%),其IGF-1濃度下降超過20%,顯示TE-8214具備顯著的IGF-1抑制效果,進一步支持其作為治療用藥之優秀潛力。目前,免疫功坊正積極展開第二期臨床試驗的籌備工作,預計於2025年第三季在台灣正式啟動。我們期盼透過未來階段的試驗推進,加速驗證TE-8214的治療潛力,拓展其臨床應用與全球市場佈局,為更多患者帶來突破性的治療方案。TE-8214與市售長效型奧曲肽類藥物的差異化比較(圖/免疫功坊提供。)關於免疫功坊免疫功坊位於國家生技研究園區,專注於開發結合標的 (T) 與效應(E) 結構單元的「T-E型藥物」,以實現兼具療效與安全性的突破性治療。公司運用自主研發的「脂肪酸束平台」技術,目前已有兩項新藥進入臨床階段,並有多項臨床前候選藥物,未來將持續推進創新藥物研發與臨床應用。聯絡資訊若您有合作洽談需求或欲了解更多資訊,歡迎與我們聯繫。電子郵件:bd@immunwork.com公司官網:https://www.immunwork.com/公司影片:https://www.youtube.com/watch?v=1owxqn08HoQT-E Pharma's subsidiary Immunwork Announces Positive Phase I Top-Line Data for TE-8214, a Next-Generation Long-Acting Octreotide, Demonstrating Favorable Safety, Tolerability, and Potent IGF-1 Suppression.·Pioneering Patient Experience: TE-8214, a highly water-soluble aqueous solution, enables pain-free subcutaneous injection with a thin 30G needle, eliminating injection site reactions seen with current therapies.·Strong Pharmacodynamic Activity: Robust, dose-dependent reduction of disease biomarker IGF-1, with 83% of high-dose participants achieving a >20% reduction, confirming therapeutic potential.·Significant Market Potential: Positioned for the US$10 billion long-acting octreotide market by addressing key unmet needs of painful injections and side effects associated with current viscous, thick-needle formulations.·Phase II Initiation and Strategic Partnering: Phase II trial planned for Q3 2025; Immunwork is actively seeking strategic collaborations to accelerate global development and commercialization.Immunwork, Inc., a clinical-stage biotechnology company developing transformative therapies, today announced positive top-line results from its Phase I clinical trial (in Australia) of TE-8214, a novel long-acting octreotide analog for the treatment of acromegaly and neuroendocrine tumors (NETs). The study met its primary objectives: TE-8214 demonstrated good safety, tolerability, and pharmacological activity, with pain-free subcutaneous administration and no injection site reactions.(This photo provided by Immunwork, Inc.)A Next-Generation Therapy for Unmet Patient NeedsTE-8214 was developed using Immunwork's proprietary fatty acid modification platform, which extends the drug's half-life and increases water solubility. TE-8214's water-soluble, low-viscosity formulation allows for subcutaneous administration with a fine 30G needle, offering a dramatically improved patient experience compared to the current standard-of-care, which requires thick, viscous formulations administered with large 19G or 20G needles that often cause significant pain and injection site reactions. This innovation addresses a critical need for safer, more patient-friendly long-acting therapies in a global octreotide market projected to reach US$10 billion by 2030.(This photo provided by Immunwork, Inc.)Phase I Clinical Highlights TE-8214's Differentiated ProfileThe randomized, double-blind, placebo-controlled, single-ascending dose study enrolled 32 healthy subjects (24 receiving TE-8214 and 8 receiving saline) across four dose cohorts (0.6, 1.2, 2, and 4 mg). Exceptional Safety and Tolerability: TE-8214 was well tolerated with no serious adverse events reported. Notably, no TE-8214 recipients experienced injection site pain or nodules—results identical to placebo with saline — demonstrating a clear advantage over existing therapies. Gastrointestinal side effects, often seen with octreotide, were minimal: only 3 of 24 TE-8214 recipients reported very mild gastrointestinal discomfort. Potent and Sustained Pharmacodynamic Activity: Octreotide drugs mainly exert their therapeutic effects by suppressing insulin-like growth factor 1 concentration in the body. In the two highest dose cohorts (2 mg and 4 mg), 10 of 12 participants (83%) achieved a >20% reduction in insulin-like growth factor 1, confirming robust biological activity and validating its therapeutic potential for Phase II studies.“These Phase I clinical trial results confirm TE-8214's differentiated profile: TE-8214 is highly water-soluble, can be administered subcutaneously using a fine needle, significantly reducing injection pain and side effects for patients,” said Dr. Tse-Wen Chang, founder and CEO of Immunwork and a pioneer of anti-CD3 (OKT3) and the inventor of anti-IgE (Xolair) for asthma and allergy. “By solving the fundamental formulation and administration challenges of current treatments, we have created a product with the potential to become the new standard of care. TE-8214's profile—combining ease of administration, superior tolerability, and strong efficacy—positions it to capture a significant share of the market and, most importantly, vastly improve the quality of life for patients.”Strategic Outlook: Advancing to Phase II and Seeking Partnerships Immunwork is preparing for a Phase II trial of TE-8214 in Taiwan, planned to start in Q3 2025, to further evaluate the efficacy and safety of TE-8214 in patients. The company is actively pursuing strategic partnerships with pharmaceutical leaders to accelerate late-stage clinical development, navigate global regulatory pathways, and maximize the commercial potential of TE-8214.TE-8214: A Differentiated Profile vs. Marketed Long-acting Octreotide Analogs.(This photo provided by Immunwork, Inc.)About ImmunworkImmunwork, based in the National Biotechnology Research Park in Taipei, develops "T-E type drugs" that combine targeting (T) and efficacy (E) moieties for transformative therapies with enhanced efficacy and safety. Leveraging proprietary fatty acid bundle technologies, Immunwork has two clinical-stage candidates and a robust preclinical pipeline, and is committed to advancing innovative medicines for global unmet needs.Contact InformationFor partnership inquiries and further information:E-mail:bd@immunwork.comWebsite:https://www.immunwork.com/Video: https://www.youtube.com/watch?v=1owxqn08HoQ

陸女自稱「22年不卸妝」出代誌了? 臉部爆紅熱燙又發硬:像硬殼一樣
近日,中國一名37歲女子,因為紅彤彤的「關公臉」引起媒體注意。事實上,這名女子自述,自己的膚色可不是天生,而是她自15歲學會化妝後,20多年來基本就不曾卸妝,頂多睡前用清水沖洗了事,近日終於爆發了嚴重的紅腫現象。據陸媒《都市頻道》報導,中國吉林省一位37歲高姓女子宣稱,自己從15歲學會化妝起,至今化妝已經20多年,基本上不太卸妝,頂多睡前用清水沖洗了事。然而在今年,不知怎麼回事,臉部肌膚突然開始紅腫、發燙、發癢。然而,她不僅沒有向皮膚科醫師求助,甚至又跑去醫美診所打了一劑「水光針」。不打還好,高女女子控訴,在注射了水光針後不僅臉上的皮膚變得僵硬,就連皮膚變色也變得更加深重,從發紅轉向發紫,發燙、發癢的狀況也變得更加嚴重。她告訴媒體,現在自己臉上的皮膚:「就像個硬殼一樣,又硬、又癢、又紅!」還表示現在自己天天躲在家裡,不敢出去見人。資料指出,長期不卸妝的後果可說是十分嚴重。由於化妝品中常常含有油性成分與顏料,長期不卸妝時,這些成分與汗水、皮膚油脂混合,產生活性酵素,進而變成稱為「過氧化脂質」的汙垢,並堵塞毛孔,使皮脂、汗水和污垢無法正常排出,進而形成粉刺、痘痘。此外,殘留的化妝品和污垢會刺激皮膚,引起紅腫、發癢等不適症狀,甚至誘發過敏反應,引起局部紅腫、發癢,甚至出現水泡現象。而化妝品中的化學成分長期停留在皮膚上,也可能損害皮膚組織,加速老化,導致細紋、皺紋的出現。事件曝光,掀起網友紛紛留言討論,不少人認為高女宣稱「22年不曾卸妝」未免太過誇張,認為她的臉又不少整容手術痕跡,在手術前不可能允許她不卸妝。還有人指出,她臉部的狀況似乎有些類似水光針注射後出現的病毒感染或是過敏反應。據了解,在水光針注射過程中,若未嚴格遵守衛生標準,使用不潔的針頭或器具,就可能將細菌或病毒帶入皮膚引發感染,導致紅腫、疼痛、發熱等現象,嚴重時甚至可能導致化膿、潰瘍,甚至引發蜂窩性組織炎,或擴散到全身造成敗血症。此外,當對水光針中使用的玻尿酸或其他成分產生過敏反應,也可能在注射部位出現紅疹、搔癢甚至腫脹的狀況,更嚴重的過免反應可能導致血管栓塞,影響視力,甚至危及生命。

突破舊框架!新一代生物製劑健保給付,嚴重氣喘控制再升級
氣喘的臨床表現多樣化,為治療帶來諸多挑戰。然而,隨著醫療科技的進步,現代醫學已成功開發出精準治療的生物製劑。由於不同患者的體質與誘發因子差異顯著,加上環境變遷的影響,氣喘的臨床表現變得愈加複雜。台大醫院雲林分院胸腔內科主治醫師陳彥甫指出,過去的生物製劑治療主要針對第二型發炎(Type 2 inflammation)患者,雖然取得了一定的成效,但對於非第二型氣喘(Non-type 2 inflammation)患者的效果相對有限。隨著新一代生物製劑的問世,不僅能有效控制第二型及非第二型氣喘,甚至對於具有複雜混合型氣喘的患者,也展現出卓越的治療效果,為患者帶來更多希望。治療合併肥胖、鼻瘜肉及混合型複雜的氣喘患者 新一代生物製劑展現療效目前臨床上,透過生物標記已能為嚴重氣喘(Severe asthma)患者選擇合適的生物製劑治療方案。然而,由於氣喘的複雜性,例如患者抽菸、合併肥胖、鼻瘜肉、皮膚過敏或黏液栓塞(mucus plugging)等因素,生物製劑的治療效果在某些情況下仍然面臨挑戰。陳彥甫醫師指出,有些嚴重氣喘患者的生物標記指數並非每項都特別高,甚至可能所有指數都不顯著升高。然而,新一代生物製劑的問世,為非第二型氣喘及混合型氣喘患者提供了全新的治療選擇。陳醫師進一步說明,特別是合併肥胖的嚴重型氣喘患者,其病情難以控制通常與嗜中性球發炎密切相關。新一代生物製劑能有效控制非第二型氣喘,對於合併肥胖的氣喘患者也能展現療效,為這類患者帶來全新的治療希望。年輕媽因氣喘發作常跑急診 新一代生物製劑助控制氣喘台大醫院雲林分院胸腔內科主治醫師陳彥甫分享,臨床上曾遇到一名30多歲的年輕媽媽,體重約90公斤,屬於第二型嚴重氣喘患者。她幾乎每個月都因氣喘急性惡化頻繁前往急診室,主要症狀包括不斷咳嗽、痰多、喘息以及嚴重胸悶。特別是在生完孩子後,因孩子經常感染感冒,她也經常被傳染,進一步加重了氣喘症狀。治療過程中,她甚至一度需要依賴全身性類固醇來控制病情。考量到這名患者合併肥胖、鼻瘜肉,以及影像學檢查顯示多處黏液栓塞(mucus plugging)的情況,陳醫師為她申請了新一代生物製劑的健保給付。在接受治療一個多月後,患者的類固醇使用量逐漸減少,氣喘症狀也得到了顯著控制,不僅緩解了不適,還大幅提升了生活品質。陳醫師進一步指出,目前市場上的嚴重氣喘生物製劑均已通過嚴格的臨床試驗,證實其療效與安全性,並經由政府機構審核取得藥品許可證。然而,患者在接受治療時仍需留意可能出現的不良反應,例如注射部位的腫脹或疼痛。若發生疑似藥物副作用,應儘速尋求專業醫師的協助。新一代生物製劑擴增給付條件 嚴重型氣喘患者新福音目前健保對於嚴重氣喘生物製劑治療的給付條件仍存在一些限制,在臨床運用上可能帶來挑戰。台大醫院雲林分院胸腔內科主治醫師陳彥甫指出,有些生物製劑其健保給付規定要求患者必須使用半年以上的口服類固醇才能申請。然而,類固醇治療對部分患者可能引發不適的副作用,例如肥胖、水腫、血糖難以控制、骨質疏鬆,甚至增加感染風險,對患者的身心健康造成一定影響。為了幫助更多嚴重型氣喘患者,健保今年進一步擴增了對新一代生物製劑的給付條件,為患者提供了更多治療選擇。陳醫師強調,透過早期使用生物製劑來有效控制氣喘症狀,不僅能減少口服類固醇副作用的累積,也能顯著提升患者的生活品質。這樣的治療策略更加貼近臨床需求,為患者帶來更大的希望。控制氣喘不二法門 遵循醫師指示規律用藥「近幾年隨著更多新型生物製劑的問世,醫師在臨床治療上多了強有力的武器,能更有效地控制嚴重型氣喘。」陳彥甫醫師表示,生物製劑的進步,確實為不同嚴重型氣喘患者的治療帶來了顯著突破。然而,想要真正有效控制氣喘,關鍵仍在於患者是否能遵循醫師指示規律用藥,並結合戒菸、適當減重、規律運動,以及減少暴露於過敏原的環境,才能有效預防不可逆的肺部損傷。陳醫師進一步指出,生物製劑作為過去10年來嚴重氣喘的新型治療選擇,已有大量研究證實其對疾病控制的效果。然而,若患者中斷治療,氣喘相關的生物標記指數可能逐漸回升,並增加症狀惡化的風險。因此,他建議尚未完全控制氣喘的患者,應每3~6個月由醫師評估治療反應,根據病情調整氣喘藥物及生物製劑的使用方案,以確保疾病穩定。「氣喘雖然無法完全痊癒,但只要規律用藥,就有機會達到臨床緩解,並有效避免疾病進一步惡化。」陳彥甫醫師強調,規律用藥與持續治療是氣喘管理的核心,患者應積極配合醫師的治療建議,進而改善症狀,提升生活品質,重回正常生活。

新藥解盲兩樣情!康霈跳空漲停重登股后 順藥大股東砸錢救火止跌回升
台股12日收在23,046.80點,上漲了143.17點,漲幅達0.63%;其中,友華漲幅達10%居本日排行榜之冠,緊跟在後的是昨晚公布局部降脂新藥CBL-514美澳臨床二期試驗解盲達標的康霈,股價飛漲了52元、高達9.98%,跳空漲停573元,重登生技新藥股股后。相對順藥在11月29日宣布治療急性缺血性腦中風新藥LT3001,第二期臨床試驗結果數據達初步療效的訊息,卻未受投資人買單,股價大跌40%多,讓大股東晟德製藥宣布10日起砸10億元買回順藥股票,股價雖止跌回升,今天股價收在193.5元,上漲了3.00元,漲幅達1.57%。二家新藥股解盲消息公布之後,投資人給予兩極化反應,市場熱議其一關鍵是在於所公布的「P值」,是否有清楚揭露受試者、安慰組的療效差異的數據,以及療效效果的說明。康霈生技11日晚間正式公布其505(b)(1)全新小分子新藥CBL-514注射劑用於局部減脂之Phase 2b臨床試驗(CBL-0204 Phase 2b)最終統計結果。康霈也將於後續召開線上法說會,詳細說明該試驗臨床試驗數據與成果。其中,在具有治療前與至少一次治療後數據的受試者(FAS)中,臨床試驗主持醫師以腹部脂肪堆積等級量表(CR-AFRS, Clinician Reported -Abdominal Fat Rating Scale)評估,76.7%的受試者經CBL-514治療後可顯著改善至少1個等級,對比安慰劑組之18.9%,療效達統計上顯著差異(p=0.00004),本試驗主要療效指標成功達標,且整體藥物安全性與耐受度表現良好。(符合試驗規範之受試者Per-Protocol:81.8%的CBL-514用藥受試者改善至少一個等級之CR-AFRS。)在此試驗告捷後,CBL-514可望於2025年進入全球多國多中心三期樞紐臨床試驗(Pivotal Phase 3 Study),將有機會成為全球第一個可用於大範圍局部減脂的新藥。該試驗次要療效指標之FAS統計結果顯示,最後一次治療後12週,試驗主持醫師評估中,32.0%的CBL-514用藥受試者改善至少二個等級之CR-AFRS,顯著高於安慰劑組的 0%(p=0.00122)。最後一次治療後12週,受試者自我評估中,76.7%的CBL-514用藥受試者改善至少一個等級之PR-AFRS,顯著高於安慰劑組的19.4%(p=0.00004)。(符合試驗規範之受試者Per-Protocol:81.8%的CBL-514用藥受試者改善至少一個等級之PR-AFRS。最後一次治療後4週,50%的CBL-514用藥受試者腹部皮下脂肪體積減少至少20%,顯著高於安慰劑組的 0%(p< 0.00001)。最後一次治療後4週,與安慰劑組相比,CBL-514組腹部皮下脂肪厚度可減少27.1%(95% CI: -32.3%, -21.8%, p< 0.00001),療效達到統計上顯著差異。58.8% 的CBL-514組受試者僅需接受一次治療,即可達到至少一個CR-AFRS等級的改善。安全性方面,受試者完成至多4次CBL-514療程後的整體安全性與耐受度良好,主要不良事件為常見的輕度和中度的注射部位反應(injection site reaction)。

被低估的新冠3/「左流右新」疫苗一起打安全嗎?研究曝「最大副作用是它」
中秋節過後,疾管署打出「左流右新」口號,10/1新冠、流感疫苗首度同步開打,,左手打流感疫苗、右手打新冠疫苗,由於一次接種2疫苗,引起民眾擔心副作用將更嚴重。疾管署副署長羅一鈞表示,根據國際研究顯示,同時打新冠、流感疫苗者,半數都會在注射部位出現局部疼痛,其他則會頭痛、疲倦,但症狀都不超過48小時。「根據國健署統計,台灣近5成長者患有3種以上慢性疾病,當慢性病越多、新冠死亡風險就越高,若患有2~5種慢性疾病會提升死亡風險達2.6倍。」成大醫院家庭醫學部吳至行主任表示,如果本身有心血管疾病,新冠死亡風險更提升4倍,若為透析患者,死亡風險最高更飆至430倍。再觀察疾管署資料,無論是疫情初期或現在,可以發現新冠重症、死亡案例中9成是65歲以上的長輩,雖然風險如此高,65歲以上長輩的新冠疫苗接種率卻僅有1~2成,因此疾管署今年首度讓流感、新冠疫苗一起打,期盼能提升長輩接種新冠疫苗的意願。為何長輩不肯打疫苗?最常見的原因是認為不出門何必打疫苗。「這是錯誤觀念,新冠病毒會在家庭成員間傳播,所以不出門也會感染。」台灣家庭醫學醫學會理事長黃振國說,研究顯示7成指標病例是學齡孩童,許多孩子會從學校將病毒一起帶回家,這也是學童列為第一波新冠疫苗接種對象的原因之一。疾管署規劃新冠、流感疫苗於10/1同步開打,第1階段開放接種對象包括65歲以上長者、學齡前幼兒、醫事及衛生防疫相關人員等11類對象。第2階段則是從11/1日開始開放施打,新冠疫苗接種對象為出生滿6個月以上未列於第一階段者,流感疫苗接種對象為50~64歲無高風險慢性病成人。65歲以上長者是新冠重症、死亡的危險族群,若是有多種慢性共病,死亡風險更會大為增加。(示意圖/非當事人/記者黃耀徵攝)新冠和流感疫苗同時打,許多民眾害怕副作用太強,「根據以色列團隊針對醫護人員在2022-2023年接種流感和新冠疫苗的分析研究結果,發現同時打新冠和流感疫苗者,與只打新冠疫苗者的身體反應相似。」疾管署副署長羅一鈞表示,副作用並沒有增強,同樣都有約一半出現注射部位的局部症狀,也都有約四分之一出現頭痛、肌肉酸痛、疲倦等全身性症狀,且症狀絕大多數不超過48小時。該以色列研究也發現同時打兩種疫苗不會影響新冠疫苗的免疫反應。吳至行說,依照過往新冠疫情的趨勢來看,下一波高峰應該會落在12月,現在病毒株正在轉換,本來是JN.1,但現在KP.3正在慢慢上升,而11、12月氣候越來越冷,群聚機會也越來越多,疫情就會慢慢升溫,加上10月有國慶假期,一路到12月就會爆發。建議規律施打新冠疫苗,除了可以降低重複感染的風險,若是真的不幸染疫,也能有效減緩症狀、副作用。
「流感+新冠疫苗」下月開打 大賣場設接種站「還有健康禮可拿」
衛生福利部疾病管制署近期公布2024年度新冠和流感疫苗的接種計劃,這項接種計畫自10月1日起分階段接種。其中北榮(台北榮民總醫院)宣布,將於27日上午9時開放網路預約掛號服務,但僅限公費成人流感和新冠肺炎疫苗。根據媒體報導指出,這次全台共有3843家醫療機構成為新冠和流感疫苗的合約院所。其中,2914家提供兩種疫苗,882家僅提供流感疫苗,47家僅提供新冠疫苗。而為了方便民眾識別,疾管署製作4款不同顏色的布條,分別是藍色(兩種疫苗都有)、紫色(只有流感疫苗)、綠色(只有新冠疫苗)來方便民眾辨識,而橘色的布條則用於宣導疫苗接種開始。對於要同時接種兩種疫苗一事,疾管署推出「左流右新,健康安心」的口號,建議民眾左手接種流感疫苗,右手接種新冠疫苗,一次完成兩種疫苗的接種。不僅方便記憶,也能讓民眾獲得雙重保護。針對同時接種兩種疫苗的安全性,疾管署引用以色列一項研究結果,該研究分析2022至2023年醫療人員接種情況,發現同時接種兩種疫苗與只接種新冠疫苗相比,身體反應其實很相似。其中約52.1%的同時接種者和49.4%的單獨接種新冠疫苗者出現注射部位局部症狀,而27.4%的同時接種者和27.6%的單獨接種新冠疫苗者出現全身性症狀,如頭痛、肌肉酸痛和疲倦。大多數症狀不超過48小時。研究還顯示,兩組的新冠抗體效價相似,證明同時接種不會影響新冠疫苗的免疫反應。目前接種計劃分為兩個階段,第一階段從10月1日開始,主要針對65歲以上長者、學齡前幼兒、醫事及衛生防疫相關人員等11類對象。第二階段從11月1日開始,新冠疫苗對象擴大到出生滿6個月以上的人(未列於第一階段者),而流感疫苗則針對50至64歲無高風險慢性病的成人。而為了提高接種便利性,疾管署也全聯、大潤發、家樂福等大型連鎖超市合作設立接種站點。約74家全聯和2家大潤發將參與此計劃。而前往接種站前100位接種的民眾,將可獲得健康禮品,包括礦泉水和季節水果(具體內容依現場提供為準)。疾管署表示,按時接種疫苗是預防新冠肺炎和流感最有效的方法之一。他們鼓勵符合資格的民眾在開放接種後儘快預約,並強調「左流右新」的接種方式既不會增加身體負擔,也不會影響疫苗效果,可以讓民眾一次獲得雙重保護,安心度過秋冬季節。
新冠、流感疫苗十月開打 疾管署籲民眾儘速預約接種
疾病管制署今(18)日表示,今年度新冠、流感疫苗將同步於10月1日起分階段開打。第1階段自10月1日開始,對象包括65歲以上長者、學齡前幼兒、醫事及衛生防疫相關人員等11類對象;第2階段自11月1日開始,新冠疫苗為出生滿6個月以上對象(未列於第一階段者),流感疫苗對象為50至64歲無高風險慢性病成人。呼籲符合公費接種資格民眾開打後儘速預約接種,2種疫苗同時接種,獲得雙重保護。疾管署說明,為配合今年新冠、流感疫苗首度同時開打,特別於宣導主視覺中呈顯雙重保護的意象,代表2種疫苗的防護罩保護著接種民眾,抵擋新冠、流感病毒侵襲;而搭配「左流右新,健康安心」口號,也讓民眾易於記憶,左手接種流感疫苗,右手接種新冠疫苗,一次完成2種接種疫苗,保護自己免於新冠、流感威脅,健康、安心過秋冬。另外,因應今年有3,843家新冠、流感疫苗合約院所,為避免民眾選擇接種院所時混淆,疾管署亦製作4款布條提供地方衛生局及疫苗合約院所使用,除用於宣導新冠、流感疫苗開打的「橘色款」外,還有針對不同合約院所製作3款布條,2,914家提供新冠及流感疫苗院所為「藍色款」、882家僅提供流感疫苗院所為「紫色款」、47家僅提供新冠疫苗院所為「綠色款」,各院所可將布條刊掛門口,方便民眾一眼辨識。疾管署補充,除合約院所可接種外,為讓民眾接種疫苗更便利,疾管署持續與全聯實業股份有限公司合作,今年亦於全聯福利中心門市設立接種站,同時再增加大潤發賣場,並同樣提供前100位接種民眾健康禮(礦泉水及季節水果1份,依現場提供為準),全臺共有約74家全聯/2家大潤發設站點,供民眾有更多接種選擇,詳細接種資訊可參考各門市公告。對於今年雙疫苗一起接種,有民眾擔心:「同時打新冠和流感疫苗,副作用會不會太強烈?」,疾管署說明,根據以色列團隊針對醫學中心醫療照護人員在2022-2023年接種流感和新冠疫苗的分析研究結果:「發生局部和全身症狀的比例,同時打兩種疫苗跟只打新冠疫苗相似」。分析顯示,同時打新冠和流感疫苗者,與只打新冠疫苗者的身體反應相似,都有約一半出現注射部位的局部症狀(兩組發生率分別為52.1%和49.4%),也都有約四分之一出現頭痛、肌肉酸痛、疲倦等全身性症狀(兩組發生率分別為27.4%和27.6%),且症狀絕大多數不超過48小時。該以色列研究也發現兩組的新冠抗體力價相似,顯示同時打兩種疫苗不會影響新冠疫苗的免疫反應。疾管署呼籲,按時接種疫苗為預防新冠肺炎及流感最有效的方法之一,請符合資格民眾於開打時踴躍前往接種,且同時施打「左流右新」,一次輕鬆獲得兩種保護力,既不會增加身體負擔、也不會影響疫苗效果。

1歲女童發燒、流鼻水!就醫檢查竟是「川崎症」 醫曝「關鍵徵兆」家長多加注意
三軍總醫院收治一名一歲女童近日因發燒、流鼻水及嘔吐等症狀入院,而在經過一系列診療後,最終被確診為川崎病。該女童在住院前並無特殊病史。在入院四天前,女童開始出現發燒、流鼻水和嘔吐症狀。兩天後,家長帶她至診所就醫,並開始服用症狀控制藥物。然而,病情未見好轉,仍然有持續高燒和嘔吐狀況,家長隨即帶她至本院兒科急診就醫。川崎病導致冠狀動脈擴大病變 須預防血栓小兒心臟專科醫師徐萬夫說明,女童於急診就醫,嘴唇發紅乾裂、雙側眼結膜充血、手腳掌紅腫,軀幹部位出現紅疹,並且卡介苗注射部位皮膚也有發紅現象。因為此時已經符合診斷川崎病的臨床要件,入院後隨即給予川崎病第一線藥物免疫球蛋白治療及阿斯匹靈後,病童隨即退燒且上述臨床症狀改善,在持續觀察經過36小時沒有再次發燒後讓病童出院。然而在經過一週後,病童再次出現有發燒嘔吐情況,眼皮發紅浮腫,經過超音波檢查發現心臟冠狀動脈已經有擴大,故判斷為頑固性川崎病,於是立即再次住院,期間接受了川崎病第二線與第三線藥物的治療。雖然第一時間會退燒且抽血顯示發炎指數改善,但在多日後又會再次發燒,後來在使用第四線的藥物後,病童的狀況終於獲得控制,然而由於冠狀動脈擴大病變的關係,需要使用抗凝血藥物預防血栓形成,在經過一年的追蹤治療下,病童的冠狀動脈狀況控制良好,沒有發生狹窄與血栓導致血管阻塞的事件。發燒超過五天、伴隨四種以上症狀 早期川崎病徵兆徐萬夫醫師提到,上述一歲女童是一個較為特殊的川崎病案例,以下提供一些早期識別川崎病的關鍵徵兆,若患兒持續發燒超過五天,並伴隨下列四種以上的外觀症狀,即應提高警覺:口腔黏膜變化(嘴唇發紅乾裂、舌頭發紅等)雙眼結膜充血(通常沒有合併分泌物)頸部淋巴結腫大(通常為單側)手腳腫脹發紅多形性紅疹(通常在軀幹及四肢)若符合川崎病的診斷,臨床醫師可能會進一步安排抽血檢驗以評估病童的發炎狀況以及心臟超音波檢查以評估冠狀動脈是否受到影響。治療第一線藥物為免疫球蛋白及阿斯匹靈,大部分的川崎病童都會在24小時內明顯退燒且臨床症狀改善;出院後醫師會再安排定期於門診進行心臟超音波追蹤評估是否出現冠狀動脈病變的情形。第一線藥物治療仍發燒 恐是頑固性川崎病然而,如果在經過第一線的藥物治療後,病童仍然持續有發燒,或是有發生以下狀況時,就要懷疑是頑固性川崎病:持續發燒:如果病童在接受靜脈注射免疫球蛋白後,24至36小時後仍然持續發燒退燒後再次發燒:若病童在治療後的兩週內再次出現發燒,在排除其它引起發燒的原因後,需進一步評估是否為頑固性川崎病持續的川崎病相關表現:包括皮膚與黏膜的持續發炎,以及冠狀動脈的擴大等冠狀動脈病變風險高 識辨評估、醫病合作最重要徐萬夫醫師提醒,由於頑固性川崎病童發生冠狀動脈病變的風險更高,且目前研究對於頑固性川崎病的最佳治療方式也有待更多的研究提供臨床證據,所以對於臨床醫師來說,即時的識辨評估病童是否可能發生頑固性川崎病、依據病童的狀況制定個人化的評估與診療方式、與家長和照顧者充分說明解釋及提供支持等,都是很重要的議題。

全面了解子宮頸癌:從定期抹片檢查到HPV子宮頸疫苗
子宮頸癌在女性健康議題中佔有不容忽視的重要位置,子宮頸癌通常是由人類乳突病毒(Human Papillomavirus,HPV)所引起,是一種常見的性傳染病。一般情況下,人體免疫系統可清除HPV,但某些型別可能會導致細胞變異,最終導致子宮頸癌的發生。子宮頸癌是女性生殖系統中常見的癌症之一,通常發生在子宮與陰道相連的子宮頸,早期可能無症狀,但隨病情惡化,可能出現異常陰道出血、不規則月經、性交疼痛、出血症狀等等,若不及早發現並治療,子宮頸癌對女性健康可能會造成嚴重的影響。性行為開始後女性每年應進行一次子宮頸抹片檢查台北市立聯合醫院陽明院區婦產科主治醫師徐靖指出,子宮頸抹片檢查是種早期發現異常細胞、透過輕柔刮取子宮頸細胞樣本進行的細胞學檢查,如發現異常,醫生將進一步評估並提供適當治療。衛福部建議,性行為開始後女性每年應至少進行一次子宮頸抹片檢查,若前三次檢查結果皆為正常,30至65歲女性可延長為每三年檢查一次,及早發現異常細胞會有助於預防子宮頸癌的發生。青春期前或初期接觸HPV前施打子宮頸疫苗除定期抹片檢查外,子宮頸HPV疫苗也是保護女性健康的重要方式,此疫苗可預防特定型別的HPV感染,降低子宮頸癌的風險,疫苗分為預防型(bivalent、quadrivalent、nonavalent)和治療型,建議在青春期前或初期接觸HPV前施打,即使已接觸HPV疫苗仍有一定的保護效果。根據衛福部建議,9至45歲女性可施打疫苗,最佳施打年齡為性行為開始前,但已有性行為者亦可考慮;部分國家也開始推薦男性施打HPV疫苗,因其可能成為HPV攜帶者和傳播者。目前市面上有幾種不同型別的HPV疫苗,包括二價(Cervarix)、四價(Gardasil)和九價(Gardasil 9),能預防不同數量的HPV型別,其中九價疫苗提供最廣泛的保護,可預防引起大多數HPV相關癌症的型別。大多數施打HPV疫苗者無嚴重的副作用,僅有輕微如注射部位疼痛、紅腫等局部反應和例如發燒、頭痛等全身反應,經過廣泛的臨床試驗證實,HPV疫苗被證明是安全有效的、是預防HPV感染和相關癌症的重要工具。徐靖醫師提醒,預防子宮頸癌是全社會共同的努力目標,透過定期的抹片檢查和子宮頸HPV疫苗施打,可有效保護女性的健康,帶來更健康、更安全的生活。

誤認鼻子長粉刺!男友媽好心幫處理「擠出隆鼻假體」 正妹氣炸怒告
北市一名游姓女子先前曾動刀隆鼻,2020年與前男友交往期間,由於男方的孫姓母親對醫美有些研究,因此放心讓孫婦在臉上注射不明物,孫婦甚至將游女的隆鼻假體「誤認成粉刺」擠出,導致游女傷口感染險毀容,氣到提告男友媽,經士林地院審理,依《過失傷害罪》判處孫婦拘役30日。據判決書指出,有過美容經驗的孫婦,得知兒子的游姓女友喜歡醫美,便向游女提議注射膠原蛋白微整,包括眉心、鼻頭及下巴都有施針,怎料游女分手後卻發現,注射部位經常傳來刺痛感,因此向孫婦反應,2人則相約在家處理皮膚狀況。孫婦在檢查臉部問題時,以為游女鼻子上的假體是粉刺,竟用針頭直接挑擠,意外將植入的隆鼻假體擠出,接著再用小剪刀剪下,由於孫婦施作過程並未確實消毒,也沒有戴上醫用手套,害得她鼻子患處傷口感染,進而引起蜂窩性組織炎,讓游女一氣之下怒提告。法官審理認為,孫婦並非醫事相關從業人員,卻草率處理游女的臉部問題,且過程中未做好相關消毒措施,導致傷口發生感染,漠視他人健康權益,考量孫婦已坦承犯行,但未與游女達成和解,故依《過失傷害罪》判處孫婦拘役30日,可易科罰金。

就怕新冠疫情狂燒!新冠XBB疫苗有新選擇 Novavax首批預計1月開打
新冠疫情還沒結束!為因應目前流行的變異株,國內提供莫德納XBB疫苗接種,而食品藥物管理署今天宣布核准Novavax XBB疫苗專案輸入,未來民眾將多一項新冠疫苗選擇。疾病管制署表示,Novavax XBB疫苗預計12月底抵台,最快1月中旬開打。食藥署今天(13)召開專家會議,經審查Novavax XBB疫苗所附資料證據,與先前已核准的Novavax疫苗採用相同的技術平台製造,具有相似的特性。動物試驗結果顯示,施打Novavax XBB疫苗,可針對XBB.1.5變異株病毒產生相當的中和抗體免疫反應;安全性方面,最常見的不良反應為注射部位壓痛、注射部位疼痛、疲倦、頭痛、肌痛和全身無力,發生的局部/全身性不良反應以輕中度為主,與先前已核准的Novavax疫苗相似。食藥署表示,考量國內目前流行的變異株以XBB變異株病毒為主,世界衛生組織亦建議使用單價XBB.1衍生譜系(如XBB.1.5)作為新疫苗抗原成分,經專家會議整體評估其臨床風險效益,同意核准Novavax XBB疫苗專案輸入,適用於12歲以上青少年及成人主動免疫接種。疾管署發言人羅一鈞說明,根據衛福部傳染病防治諮詢會預防接種組(ACIP)11月22日決議,建議未曾接種新冠疫苗者,應接種2劑Novavax XBB疫苗,兩劑間隔4周以上;曾接種新冠疫苗者,需與前一劑間隔至少3個月,接種1劑Novavax XBB疫苗。羅一鈞表示,已接洽自COVAX機制進口Novavax XBB疫苗,共46萬劑,預計12月底抵台、最快1月中旬開打。國內目前提供2種廠牌的XBB疫苗,ACIP建議,選擇其中一種疫苗接種即可。
馬斯克大讚減肥神藥Ozempic 小摩:2030年銷售額逾千億美元
特斯拉和SpaceX的創始人兼執行長馬斯克(Elon Musk),近日在X上發表了一則頗具爭議的言論,聲稱肥胖相關的健康風險幾乎肯定大於使用胰高血糖素樣勝肽-1(GLP-1)受體激動劑的風險,這是一類可以降低血糖並促進減重的藥物。近期在社交媒體上引起熱議無非是諾和諾德藥廠的Ozempic、Wegovy,兩者皆是GLP-1受體激動劑藥物,它能夠刺激胰島素分泌,減少食慾,減緩胃排空。主要用於治療第2型糖尿病,但美國食品藥物管理局(FDA)已批准其中一些用於肥胖治療。而GLP-1類藥物現在已經成爲諾和諾德和禮來這兩家醫藥巨頭的金礦,並使諾和諾德超過LV集團成爲了歐洲市值最高的公司。馬斯克在X上的推文內容稱:「減肥藥Ozempic實際上影響了沃爾瑪的食品銷售,肥胖是導致全球死亡和疾病的主要原因。GLP- 1受體激動劑已被證明有助於減重和治療糖尿病。與好處相比,副作用微乎其微。不要讓恐懼阻止你過上更健康的生活。」據統計,全球超過五分之二的人口超重或肥胖。世界肥胖聯合會預測到2035年,這一數字將增加到超過40億,超過一半的人口將面臨超重或肥胖問題。肥胖症是一種疾病,GLP-1類型藥物是當前科學有效的治療方法。據稱,只需堅持每週注射一次即可使體重下降15%,而這些新型減肥藥物並非僅是一種美容產品,它們將使全球數十億受肥胖困擾的普通人受益。值得注意的是,GLP-1是目前減重領域主流研究靶點,存在超過1000億美元的藍海市場,全球GLP-1RA市場規模現已突破200億美元。摩根大通預計到2030年,將有大約1500萬肥胖症患者使用GLP-1類藥物,年銷售額將遠遠超過1000億美元。其中,美國市場的銷售額將接近500億美元。而禮來製藥和諾和諾德將有望繼續在GLP-1市場佔據絕大部分份額,並均分這一市場。然而,GLP-1受體激動劑並不是沒有風險的。一些常見的副作用包括噁心嘔吐、腹瀉便秘、注射部位反應和低血糖;較嚴重但罕見的併發症包括膽囊疾病、腎臟問題、甲狀腺腫瘤和過敏反應。馬斯克的推文引發了他的追隨者和民眾間的激烈爭論。有些人讚揚他提高了人們對肥胖問題的認識,並鼓勵人們尋求醫療協助;其他人則批評他過於簡化了一個複雜的問題,並在沒有足夠證據或醫學專業知識的情況下推廣藥物。

打完針後要揉嗎? 食藥署揭:若錯誤處理易瘀青
打完針後到底要不要揉一揉?食藥署說明,打針時根據施打的位置和用途不同,後續的處理方式也不一樣!針後錯誤處理容易瘀青,建議民眾打針時,可詢問護理師或專業醫事人員後續的處理方式,注射藥品後最好在原處休息30分鐘,無不適或過敏反應後再離開。解答:並非所有的針打完都需要揉並非所有的針打完都需要揉,有些針劑打完不適合揉,如果揉了,反而會有反效果。一般而言,打針後需不需要揉,依注射的藥品種類或注射方式而定。通常打胰島素(皮下注射),或打血管針(靜脈注射),如打點滴、抽血及一些小量的藥物注射等,這類的針劑打完後,不需揉,只需輕壓傷口,直到不再出血即可,如果揉的話,可能會使血管遭到拉扯,而導致皮下出血或淤青。部分肌肉注射的藥品,會建議輕揉注射部位,以加速藥品的吸收或使藥品快速產生藥效。而部分疫苗,雖然也是肌肉注射,但因疫苗是在注射後,讓藥品緩慢被身體吸收,慢慢誘導身體產生抗體。因此,打完疫苗後,不建議搓揉注射部位,若注射藥品24小時後有產生局部硬塊,可透過熱敷的方式改善。食藥署建議,目前注射的藥品種類繁多,建議民眾打針時,可詢問護理師或專業醫事人員後續的處理方式,並且注射藥品後,最好在原處休息30分鐘,如無任何不適或過敏反應後再離開。原文出處:聽說打完針後,一定要揉一揉,隔天傷口才不會瘀青?

幼兒追加劑5月初開打 僅莫德納基礎劑幼兒可打
幼兒施打完COVID-19基礎劑後,若想接種追加劑,過去國內無相關疫苗可以提供接種。不過,指揮中心在4月13日宣布,未來幼兒可接種莫德納次世代疫苗作為追加劑,對此也公布了新的建議指引。指揮中心發言人羅一鈞表示,目前洽購的莫德納次世代疫苗將於4月16日到貨,經過食藥署封緘檢驗流程後,預計最快5月初可以提供幼兒接種追加劑疫苗。追加劑不開放混打 僅莫德納基礎劑幼兒可打衛生福利部傳染病防治諮詢會預防接種組(ACIP)已於今(2023)年3月22日專家會議,先行針對「幼兒是否可接種莫德納COVID-19雙價BA.4/5次世代疫苗作為追加劑」進行討論。指揮中心於4月13日公布討論結果,並依據目前臨床試驗結果及國際間使用情形,針對幼兒莫德納COVID-19雙價BA.4/5次世代疫苗追加劑接種作出接種建議。羅一鈞說明,由於現在幼兒混打的安全性證據不是很充分,專家檢視現有資料後認為現在不適合建議幼兒族群進行混打,所以建議施打疫苗仍需同一廠牌延續使用,不建議混打。因此,幼兒莫德納COVID-19雙價BA.4/5次世代疫苗追加劑接種建議,滿6個月至未滿6歲且以「莫德納疫苗」成基礎劑接種的幼兒,可接種莫德納次世代苗作為追加劑,接種時間須與前一劑間隔至少3個月。關於莫德納次世代疫苗接種效益與安全性,羅一鈞指出,根據臨床試驗,幼兒輕症保護效果約有50.6%,也就是說染疫後產生輕症的情況大約可以減少一半。另外,副作用大部分都是輕微且短暫的過渡性症狀,主要有注射部位疼痛、疲倦、頭痛等,少部分接種後會有肌肉、關節疼痛以及發燒的情形,不過症狀都較輕微。BNT基礎劑幼兒 無追加劑接種怎麼辦?由於,已接種BNT疫苗作為基礎劑的幼兒,不適用莫德納次世代疫苗作為追加劑,許多民眾就好奇未來是否會採購BNT幼兒型次世代疫苗,提供給幼兒作為追加劑接種呢?羅一鈞表示,目前沒有更多的證據顯示這群幼兒需要再提供第四劑疫苗,包含次世代疫苗在內進行接種,而美國也還沒有開放BNT次世代疫苗讓已接種3劑BNT疫苗的幼兒作為追加劑使用,所以還須檢視更多資料評估。已接種BNT疫苗的幼兒,依現行建議完成3劑基礎劑施打就可以了。不過,羅一鈞強調,由於現有資料專家建議不進行混打,但之後針對幼兒混打若有新的資料、結果,也不排除會進行調整。

康霈首創脂肪標靶新藥引注目 今登興櫃直衝160元
全台唯一投入醫美新藥研發的康霈生技(6919)今(26日)攜核心產品局部減脂新藥CBL-514優異的臨床成果登錄興櫃,參考價為122元。市場看好其全球首創脂肪標靶新藥吸睛,未來上市將搶攻千億局部減脂市場,早盤大漲三成衝上160元。根據Grand View Research 2021年調查,2030年全球醫美市場預估為3321億美元,而根據Deloitte中國身體塑形市場行業發展白皮書指出,中國局部減脂市場在2020年超過15億美元,在2030年將成長至154億美元,推估全球市局部減脂市場將超過1,025億美元。由於身體局部的皮下脂肪,包含腹部、大腿或手臂的皮下脂肪很難透過飲食、運動或藥物減重的方式來減少,因此,若要減少身體局部脂肪,且不影響其他部位,就必須透過手術或非手術的局部減脂產品來減少局部脂肪。而與減重藥物或縮胃手術不同,局部減脂產品的主要用途為減少治療部位的皮下脂肪而非減輕體重。美國整型醫學會指出,目前仍有超過60%的人因為不滿意現行的治療方式或害怕副作用而卻步,顯示局部減脂市場仍有大量未被滿足的醫療需求。康霈生技經過10年的研究,開發了全世界第一個也是目前唯一以脂肪細胞凋亡來減少脂防細胞的注射劑藥物CBL-514,目前已進入臨床二期。康霈指出,CBL-514是一種全新小分子新藥505(b)(1)注射劑,能誘導脂肪細胞凋亡,可經由注射方式精準減少治療部位脂肪,且不會造成其他組織細胞壞死或損傷,也不會對神經系統、心血管或呼吸中樞造成副作用。簡單來說CBL-514就是脂肪細胞的標靶治療,能減少注射部位皮下脂肪,能安全又有效地想瘦哪裡就瘦哪裡,實現安全有效且安心無創的局部減脂。CBL-514在醫美-非手術局部減脂適應症,已於澳洲及美國完成Phase I、Phase IIa、Phase II-stage1以及最大劑量代謝物鑑定Phase II MetID臨床試驗,且藥物安全性與耐受度良好。除了原本的局部減脂適應症,CBL-514其他適應症範圍,包含罕見疾病-竇根氏症與橘皮組織治療皆已通過美國FDA核准進入臨床二期試驗,鎖定全球2030年233億美元與61億美元市場。康霈另有三個新藥在臨床前階段,CBA-539適應症為色素沉著、美白及抗衰老,CBO-012適應症為退化性關節炎,CBF-520適應症為治療中心型肥胖與非酒精性脂肪肝等相關疾病。

莫德納次世代疫苗通過EUA 18歲以上可追加接種
衛生福利部食品藥物管理署(以下簡稱食藥署)為因應新型冠狀病毒疾病(以下簡稱COVID-19)變異株防疫之需求,於111年9月2日召開專家會議,討論莫德納雙價疫苗作為18歲以上成人主動免疫之追加接種。食藥署表示,莫德納雙價疫苗為次世代疫苗,每劑0.5 mL含有25微克原型株mRNA及25微克Omicron BA.1變異株mRNA。經審查莫德納雙價疫苗的一項第二/三期臨床試驗結果顯示,以雙價疫苗作為追加劑,相較於以原型株疫苗作為追加劑,能夠誘發較優的對抗Omicron BA.1變異株的中和抗體免疫反應;而探索性分析數據顯示,雙價疫苗也能夠誘發對抗Omicron BA.4/BA.5變異株的中和抗體免疫反應。在安全性資料方面,雙價疫苗追加劑發生的局部/全身性不良反應頻率與原型株疫苗相似,並以輕中度為主,常見的不良反應主要是注射部位疼痛及腫脹、疲倦、頭痛和肌肉痠痛等,沒有發現新的安全疑慮。食藥署表示,經整體評估其有效性及安全性,並考量國內緊急公共衛生需求,同意核准莫德納雙價疫苗可適用於18歲以上成人主動免疫之追加接種,其用法用量為在國內已授權的COVID-19疫苗之基礎接種或追加劑後,間隔至少3個月施打。未來食藥署將持續監控國內外接種COVID-19疫苗的安全警訊,分析評估疫苗不良事件通報資料,執行安全監視機制,保障民眾接種疫苗之安全。