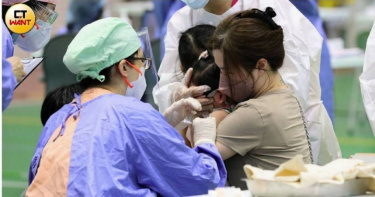
6歲以下幼兒莫德納次世代接種 下周二開打!需間隔12周以上
疾病管制署今(12)日表示,有關幼兒追加劑型莫德納雙價BA.4/5次世代疫苗,將於今)年5月16日起納入提供接種。依衛生福利部傳染病防治諮詢會預防接種組(ACIP)於今年3月22日專家會議,接種對象及間隔建議如下:一、接種對象:(一)可提供滿6個月至未滿6歲以莫德納疫苗完成基礎劑接種之幼兒,接種追加劑使用。(二)不適用於滿6個月至未滿5歲以Pfizer-BioNTech幼兒劑型疫苗完成基礎劑接種之幼兒,該些對象仍以Pfizer-BioNTech幼兒劑型疫苗完成3劑基礎劑接種。二、接種間隔:需與最後一劑基礎劑或前一劑追加劑間隔12周(84天)以上。另疾病管制署說明,針對滿5歲至未滿6歲兒童,亦提供本疫苗作為追加劑選擇。包括:已接種Pfizer-BioNTech兒童疫苗追加劑之幼兒,以及已年滿5歲未滿6歲,前以Pfizer-BioNTech幼兒疫苗完成3劑基礎劑之幼兒,皆可以選擇本疫苗接種追加劑,接種間隔亦為需與最後一劑基礎劑或前一劑追加劑間隔12週(84天)以上。疾病管制署呼籲,本次為首次提供國內滿6個月至未滿6歲幼兒雙價追加劑接種,提醒接種後,家長可透過接種單位提供的須知或海報上的QR code掃描加入「Taiwan V-Watch」疫苗接種-健康回報系統(https://gov.tw/CFL),藉由家長關注子女接種後狀況觀察,提醒就醫並瞭解接種後常見不適。另亦請尚未完成接種基礎劑者,儘速完成接種。並請各地方政府衛生局妥為安排/指定合約醫療院所,相關接種資訊請參閱各縣市官網公布資訊。

批蔡政府堅持「獨立台灣」買疫苗 鄭麗文告發蔡英文內亂、殺人
鴻海集團創辦人郭台銘日前爆出BNT大股東於2021年6月寄給他信件,內容提及民進黨政府堅持與BNT協議對外公告時必須寫『獨立的台灣政府』(Independent Government of Taiwan)而導致買不到疫苗。國民黨立委鄭麗文等人於今(10)日赴台北地檢署告發總統蔡英文、前行政院長蘇貞昌、前衛福部長陳時中以及外交部長吳釗燮涉嫌內亂、瀆職、殺人罪。郭台銘辦公室指出,該信件坐實了政府卡BNT疫苗,為了意識形態而犧牲人民生命安全的證據。信件內容也表明民進黨堅持與BioNTech的協議對外公告時必須寫『獨立的台灣政府』(Independent Government of Taiwan),因代理商Fosun(中國大陸上海復星製藥)無法接受,導致交易被迫取消。郭辦表示,顯見合約取消是因民進黨政府堅持將政治置於人民的生命安全之上。而由永齡、鴻海、台積電所組成的疫苗談判小組,簽約的名稱則是『Republic of China(Taiwan)』。鄭麗文表示,蔡政府在購買疫苗時堅持以『獨立的台灣政府』(Independent Government of Taiwan)名義,涉嫌叛國,且因阻擋疫苗購買造成800人死亡,涉嫌廢弛職務釀成災害、殺人罪等,才在今天提出告發。

監院疫情調查報告出爐 監委要求衛福部「公開完整疫苗決策資訊」
監察院社會福利及衛生環境委員會於2月22日通過監察委員林郁容、王麗珍、蘇麗瓊、蕭自佑所提調查報告,要求行政院督促衛生福利部對於新冠肺炎疫苗的整備與採購決策及作業程序未臻周妥之處,進行檢討改善。4位監察委員表示,國內於2021年5月中旬爆發本土疫情,社會瀰漫恐慌不安,國人對於疫苗之施打有急切需求,部分輿論認為中央流行疫情指揮中心對於疫苗整備及採購政策似有不周,且決策過程未見完備。為究明實情,調查過程諮詢國內專家學者及約詢時任衛福部陳時中部長、疾管署周志浩署長及食藥署吳秀梅署長等人後提出調查報告。監委指出,全球COVID-19疫情爆發後,國內尚未發生大規模社區感染前,即開始整備COVID-19疫苗。因臺灣管制措施得宜,疫情發展慢於其他國家,但當時全球疫情擴展迅速,其他國家一開始就進入社區感染,死亡病例遽增,因此先進國家較早於疫苗尚未研發成功或取得EUA時,即投入大量資金,以投資方式超額採購疫苗,疫苗初期產能有限,供不應求,採購條件由賣方主導,加以國內疫情平穩,民眾接種疫苗意願不高,故我國向國際疫苗廠採購及簽約之當時,時程較其他國家為晚,而且採購數量相對較少,致非屬國際疫苗廠優先供貨之國家,包括COVAX平台在內;另2021年5月疫情艱難時刻,疫苗到貨數量僅87萬餘劑,迄同年7月底前,到貨數量約951萬餘劑,其中586萬餘劑係國際友人捐贈。因此指揮中心雖緊急應變,透過外交部協助爭取國際捐贈,確為不得不然之舉,允應確實檢討此次新冠疫苗無法滿足國人接種需求之各項因素,作為日後因應新興傳染病流行之疫苗政策決策及執行採購時程之參考。監委指出,行政院於2020年7月確定我國疫苗來源包括「自研自製」的管道,食藥署即規劃視疫情急迫情形及緊急公衛需求,必要時給予EUA,並曾邀集高端、國光及聯亞等3家研發COVID-19疫苗業者參與,同年10月14日召開專家討論會議決議「COVID-19疫苗申請EUA所需的療效資料,得以免疫原性做科學上合理的連結或推估」;2021年5月28日之專家會議同意以「比較國產疫苗與AZ疫苗之免疫原性(不劣性比較)」,作為國產疫苗緊急使用授權之療效評估標準,以及食藥署於2021年7月18日及8月15日分別召開會議審查高端疫苗及聯亞疫苗申請EUA案,將中和抗體效價作為替代性療效指標與決定是否發給高端及聯亞EUA所為之決定,有其決策依據。惟迄今國際間承認高端疫苗之國家僅有10國,主要原因應係未有傳統第三期臨床試驗之結果證明其療效,國際認證之進展相當有限,部分國人因此對其保護力有所質疑,已不利國內疫苗產業之發展。未來倘有類似情況,衛福部應以本次疫情經驗為鑑,研酌於契約中擬訂業者取得相關國際認證等適當條件,以促使國內業者盡最大努力,提升民眾信心。監委另表示,政府採購法第105條第1項第2款規定雖授權公務員應依專業判斷進行緊急採購,但執行者在實務上因授權範圍未具體明確,仍可能多所顧慮。此次疾管署以預採購方式向COVAX平台、AstraZenca公司、Moderna公司採購未完成第三期臨床實驗之疫苗,各界並未質疑其合法性,但於高端及聯亞尚未取得EUA即簽訂採購合約,卻使辦理採購之疾管署迭遭責難;又2021年發生社區感染時,迭有批評購買數量太少,甚至認為第一要務是取得疫苗,即使價格再貴,亦應於國際間不計成本,搶購疫苗。惟疫情難以預料,指揮中心增加採購之數量,來不及在效期前全數接種,部分疫苗必須銷毀,再被質疑購買數量過多;再以COVID-19疫苗之交易為賣方市場,各廠商於合約中約定雙方權利義務有利於賣方,而採購數量、時機,以及各國國民之所得情形,均可能影響疫苗採購之單價,且廠商並未公布其訂價依據之成本分析,疾管署亦難以取得各國購買之價格進行比價。因此衛福部及工程會允應就此次COVID-19疫苗之採購經驗,通盤檢討緊急採購之相關規範,其授權範圍應具體明確,採購程序及機制容許相當之彈性,完備緊急採購之法令規範及辦理程序,俾使公務員不致進退失據,得及時依專業判斷為適當之採購;另衛福部允應培養國內具備國際採購專業之人員,研酌如何結合各部門專業人力,共同協助處理,提升緊急採購之專業能力。監委表示,指揮中心為規劃疫苗接種部署,在民間企業及慈善團體申請輸入疫苗時,要求需檢附原廠授權書,有其確保疫苗安全有效及供應數量穩定之考量;鴻海及永齡基金會於2021年6月1日委託台康公司檢附相關文件向食藥署申請500萬劑BNT疫苗專案輸入, 6月10日補件,當時並未取得BioNTech公司同意供貨之證明文件,但食藥署仍於6月12日許可有條件專案進口,其但書包括BioNTech公司出具同意供貨之證明書等,永齡提供疾管署擬向疫苗廠表達國家願意支持之草案資料;台積電亦於2021年6月10日主動至疾管署拜會,表達捐贈疫苗意願,並將申請之文件提供疾管署之律師進行檢視與修改。疾管署即持續與相關企業檢視及研修採購前置作業所需法律文件,俾使捐贈單位能進行後續疫苗採購事宜。惟在當時國人對疫苗有急切需求之氛圍下,衛福部於2021年7月11日晚間完成簽署程序,與國人對加速取得疫苗之期待有所落差,甚至引起外界之質疑與抨擊。衛福部允應檢討此次民間企業、團體捐贈疫苗之行政流程及證明疫苗來源及品質之相關文件,建立捐贈疫苗與藥品之處理機制。除此之外,監委另提出下列調查意見,並請行政院督促所屬檢討改進:一、我國與國際間疫苗受害救濟之審查制度相較,民眾申請時無須付費及負舉證責任,且由中央協助資料蒐集,申請之門檻較低,相對審理所需行政負擔較重。惟新冠疫苗多採用緊急授權方式上市,在安全性及有效性存有風險,民眾於接種疫苗後發生不良反應,因有時序上之關聯,難免懷疑與接種疫苗有關,疾管署允應加速新冠疫苗預防接種受害救濟審查進度,釐清個案傷病或死亡與施打疫苗之關聯性,使受害民眾迅速獲得合理之補償,維持對接種疫苗之信心,以利防疫政策之推動。二、指揮中心依據ACIP專家會議結論,依職業、年齡、疾病等風險別排定優先順序,但公布之相關會議記錄,對於疫苗接種政策之討論,僅記錄討論後之決議,民眾難以瞭解接種順序之考量,引發各種疑慮,應予檢討以作為未來疫苗接種政策之參考。三、部分縣市對於預約接種疫苗方式及場地動線規劃不周,甚至發生非高風險者未依接種順位提早接種疫苗之情事,衛福部允應通盤檢討此次縣市政府規劃及執行疫苗接種所發生之各項問題,作為日後進行大規模疫苗接種計畫之參考,避免類此情事之發生。四、疫苗政策為攸關全體國民重要權益之事項,衛福部已公開部分疫苗採購、核予高端疫苗EUA、通過高端疫苗效益評估報告等重要決策之內容,相關政策亦經專家會議討論形成政策決定,但公布之資訊尚不足以使民眾對疫苗政策之諸多質疑獲得釐清,允應公開更完整之疫苗決策資訊,對民眾疑慮事項善加說明澄清,並檢討目前將相關簽稿文書之機密等級設定「密」等之必要性,適當開放予各界檢視,保障人民知的權利,增進對公共事務之瞭解、信賴及監督,並促進民主參與。本案在111年12月21日經本院社會福利及衛生環境委員會進行審查,經與會委員嚴謹討論,認有再予補充論述之需要。為確保調查報告之周全,爰斟酌會中委員提出之各項意見,修正調查報告內容之部分文字後,再行送會審查。至本案之處理進度,符合「監察院辦理調查案件注意事項」相關規定,併予敘明。
中國放寬部分新冠防疫策略 世衛組織主任樂見改變
據香港東網報導,世界衛生組織(WHO)緊急項目執行主任瑞安當地時間2日表示,高興看到中國調整策略,放寬部分新冠防疫限制措施,指當人民處於痛苦時,政府傾聽民意很重要。瑞安表示,疫情下民眾活動受到限制,生活上不得不作出改變,確實令人疲倦。他認為,使用美國輝瑞和德國生物科技公司BioNTech合作研發及美國莫德納的mRNA疫苗,是中國提高免疫覆蓋率的可靠選擇,但使用哪一款疫苗,是主權政府根據人民最大利益所作的選擇。他認為中國未來的防疫策略,應該要在控制病毒、人民生命、生計、福祉及人權之間取得平衡。世衛曾指出中國的清零政策不能持續,認為擁超級傳播力的新冠變種Omicron令清零變得不可能。

第二批採購BNT兒童疫苗今上午抵台 62.4萬劑供6個月至4歲幼兒接種
中央流行疫情指揮中心今(31)日表示,今(2022)年第二批採購Pfizer-BioNTech幼兒劑型疫苗62.4萬劑,於今日上午抵達桃園國際機場,完成通關程序後,直接運送至指定冷儲物流中心進行後續檢驗封緘作業,再提供給6個月至4歲幼兒基礎劑接種使用。本批效期至2023年4月30日,今年採購的幼兒劑型疫苗已全數到貨。
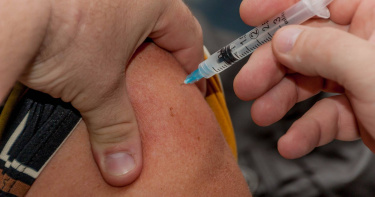
因新冠疫苗使用mRNA技術 科學家預測:癌症疫苗將在8年內上市
德國公司BioNTech的共同創辦人近期受訪時表示,因為新冠疫苗使用到mRNA技術,在研發的過程中積累了不少經驗。目前預測,在這樣的經驗下,癌症疫苗將於8年之內正式上市。根據《BBC》報導指出,與輝瑞(Pfizer)合作開發新冠疫苗的德國BioNTech,其公司創辦人夫婦圖雷齊(Ozlem Tureci)與吳沙忻(Uğur Şahin)夫婦,近期在接受訪問時表示,圖雷齊表示,其實在疫情之前,BioNTech就一直研究mRNA技術的癌症疫苗,但由於研發新冠疫苗的關係,反而更熟悉、加快了mRNA疫苗的製作,同時也更加理解人體免疫系統的反應。目前BioNTech正在針對癌症疫苗進行幾項實驗,其中一項實驗是提供「客製化」的疫苗,透過mRNA疫苗技術,讓患者體內的免疫系統「主動去攻擊」癌症細胞。圖雷齊認為,mRNA技術讓患者的免疫系統能夠識別癌症細胞,同時也可以避免因為使用標靶藥物,結果導致其他細胞也跟著遭受破壞。而被問及mRNA技術的癌症疫苗會何時上市、正式使用在患者身上,圖雷齊則是預測「可能會在2030年之前正式上市」。

日本自由行將解禁!6大重點報你知 這款APP必載
日本11日不但要重新開放自由行與免簽證入境,還要取消每日入境人數上限,再加上日圓今年大幅貶值,都讓許多哈日族早已摩拳擦掌,準備將疫情後第一場國外旅遊獻給日本,據《ETtoday新聞雲》的報導,以下為日本旅遊的最新6大重點與規定。1.下載MySOS APP所有入境日本的旅客都被要求在赴日的2週內下載並安裝MySOS,之後在航班抵達日本的6小時內填寫個人資料,同時再上傳3劑日本認可之疫苗廠牌的接種證明或是PCR陰性報告。2.不再需要隔離日本在10月10日以前,所有外國旅客都是根據各國疫情風險區分成的紅、黃、藍3個類別,來遵照不同的檢疫規定。不過11日將統一採取相同規範,即使是來自在此之前被列為高風險地區的旅客,只要符合規定,就不需要隔離。不過在入境時出現新冠症狀的旅客仍需在機場接受PCR核酸檢測。3.旅客不再需要透過旅行社代訂行程日本自11日起全面開放自由行,旅客不再需要透過旅行社代訂住宿與機票。4.重新開放免簽證旅遊日本11日起將重新開放在疫情期間暫停的免簽證協議,因此由日本外務省指定的68個國家與地區的護照擁有者,將不再需要向日本政府申請旅遊簽證。5.打滿3劑疫苗者不須提供入境前PCR核酸檢測結果日本政府已在9月修改入境規定,免除已接種3劑以上疫苗的旅客入境前的PCR檢測要求,不過未完整接種疫苗或是施打的疫苗廠牌不符合規定的旅客,仍須提交在抵達日本72小時前的PCR檢測報告。6.接種新冠疫苗日本仍在持續擴大新冠疫苗的認可清單,截至目前為止已開放施打滿3劑BNT(Pfizer–BioNTech)、莫德納(Moderna)、AZ(AstraZeneca)、嬌生(Johnson & Johnson)、印度巴拉特生技公司(BharatBiotech)生產的Covaxin、諾瓦瓦克斯(Novavax)、中國製的科興、國藥、康希諾吸入式疫苗,以及印度製藥企業印度血清研究所(SerumInstitute of India)研製生產的Covishield、Covovax疫苗。值得注意的是,日本尚未將高端疫苗列入,不過只要「4劑內有3劑符合日本規定」依然能免PCR入境日本,但如果施打2劑以上的高端就不適用,畢竟現行規定最多只能接種4劑疫苗。
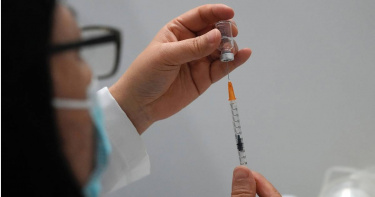
這次又要怪日本做事太慢?日新增5款認可疫苗 科興、國藥入列卻不見高端
日本厚生勞動省4日在入境疫苗認可名單中又新增了5款疫苗,包括中國製的科興、國藥、康希諾吸入式疫苗,以及印度製藥企業印度血清研究所(Serum Institute of India)研製生產的Covishield、Covovax疫苗,不過仍未見台灣的高端疫苗。日本政府現行認可的新冠疫苗為世界衛生組織(WHO)新冠疫苗緊急使用清單中的疫苗,包括BNT(Pfizer–BioNTech)、莫德納(Moderna)、AZ(AstraZeneca)、嬌生(Johnson & Johnson)、印度巴拉特生技公司(Bharat Biotech)生產的Covaxin,以及諾瓦瓦克斯(Novavax)。據厚生勞動省4日更新的疫苗認可清單顯示,10月11日後將新增5款中國和印度製的新冠疫苗,而名單中依然不見台灣製的高端疫苗。日本厚生勞動省4日更新疫苗認可名單。(圖/翻攝自日本厚生勞動省網站)台大兒科醫師李秉穎於9月17日被問到高端為何遲遲無法通過WHO國際認證時,還表示「非學術因素」,甚至怪給世界衛生組織,聲稱「終究會有資料出來,但因為WHO做事太慢」,沒想到近日厚生勞動省又排除了高端進入認可名單之中,似乎打臉了李秉穎的說法。日本11日起開放海外旅客自由行,恢復免簽證措施,入境旅客只要持有接種3劑日本認可疫苗的紀錄,就不需出示PCR陰性證明;相反的,若沒有打滿3劑疫苗,或接種厚生勞動省認可疫苗名單以外的疫苗,則必須出示出發前72小時內做的PCR陰性證明來代替,過程需自費3500元。

中視新聞赴美採訪 獨家進實驗室訪疫苗開發者
中視新聞記者龔邦華、張召朋、王清煜等日前飛往美國及澳洲,專訪今年唐獎得主,團隊先是到美國14天,於紐約採訪今年永續發展獎得主傑佛瑞.薩克斯教授,並到費城採訪生技醫藥獎得主德魯.魏斯曼,接續再至澳洲採訪法治獎得主雪柔.頌德斯。在疫情期間出國採訪,因許多班機取消直飛,導致中視新聞團隊去程必須先飛到美國西岸的舊金山,再轉機前往紐約;回程則須從澳洲墨爾本先飛往新加坡轉機,才能回到台灣,過程幾經波折。一共長達24天的採訪之旅,讓資深記者龔邦華表示:「是記者生涯中出國出差採訪最多天的一次!」受疫情影響,中視記者飛往美國、澳洲訪問歷經波折。(圖/中視提供)此趟行程,受訪者之一的德魯.魏斯曼教授,他與卡塔林·卡里科及彼得·庫利斯,三人對疫苗開發有突破性的發現,並為克服這些問題開發巧妙的方法,成為SARS-CoV-2疫苗能被快速開發的關鍵。這些技術不僅徹底改變了疫苗學,更開創了以RNA為療法的新時代。但受訪時德魯.魏斯曼卻相當謙遜,讓記者龔邦華印象深刻。行程中教授也邀請中視團隊到費城的實驗室觀摩,還能站在放置mRNA疫苗相關研究的實驗室保存箱前,記者當下感受到研究者他們夜以繼日不斷研究,對BioNTech和Moderna疫苗的開發至關重要,幫助人類對抗新冠疫情,這難得的經驗讓龔邦華內心澎湃不已。一行人到澳洲墨爾本採訪時,趁著空檔,看了世界最小的企鵝「小藍企鵝」,看著小企鵝搖搖擺擺覓食,留下一串串腳印,有趣情景讓記者大開眼界。而當天在路程上竟撞到一隻袋鼠,讓一行人心有餘悸,這些都成為此次出差相當「難忘」的回憶!龔邦華之前是中視駐美特派,曾長期居住紐約,因疫情返台,藉由這次專訪行程,讓她相隔一年半,有機會再到紐約,但物價的暴漲讓龔邦華相當驚訝,受通貨膨脹影響,短短1年一碗拉麵從12塊美金,竟變成18塊美金。

60.255萬劑BNT疫苗抵台! 12-17歲青少年將優先接種
中央流行疫情指揮中心今(29)日表示,今(2022)年第二批採購Pfizer-BioNTech成人劑型疫苗60.255萬劑,於今日上午抵達桃園國際機場,完成通關程序後,直接運送至指定冷儲物流中心進行後續檢驗封緘作業,再提供COVID-19接種計畫所列實施對象接種。本批效期至2023年3月21日,將優先提供給12-17歲青少年接種追加劑使用。指揮中心指出,已於今年4月28日及7月21日與香港復星公司及德國BioNTech公司簽署COVID-19疫苗供應協議及第一次修正合約,並與美國Pfizer公司及德國BioNTech公司簽署兒童疫苗補充協議及第一次修正合約,供應330萬劑兒童劑型、190萬劑幼兒劑型及180萬劑成人劑型疫苗,並視需求擴充400萬劑成人劑型疫苗,以因應SARS-CoV-2變異病毒株之威脅。目前共計到貨220.32萬劑兒童劑型、127.2萬劑幼兒劑型、246.051萬劑成人劑型疫苗。
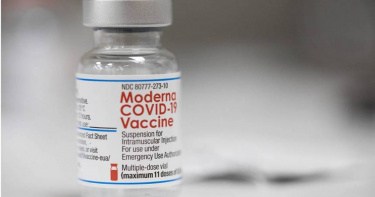
莫德納宣布提告輝瑞、BNT 盜用mRNA專利開發新冠疫苗
美國生物技術公司莫德納,本月26日宣布,要對疫苗競爭對手輝瑞與其德國合作夥伴BioNTech提起告訴,指控他們在開發美國批准的第一批COVID-19疫苗時,侵犯其mRNA基礎技術的專利,莫德納已經向美國和德國地方法院提告,輝瑞和BNT在被提告後,股價隨即下跌。綜合外媒報導,莫德納在聲明中指出:「莫德納認為輝瑞和BNT的COVID-19疫苗,侵犯莫德納於2010年和2016年間申請、涵蓋莫德納mRNA基礎技術的專利。」目前莫德納已向美國麻薩諸塞州聯邦地區法院,以及德國杜塞道夫地方法院提起訴訟,但索賠金額則未定。莫德納,還有輝瑞和BNT兩家合夥公司,是全球最早開發COVID-19疫苗的兩個集團。其中總部設在美國麻州的莫德納,是mRNA技術的創新先驅。過去疫苗的開發,總要耗費許多時間才能完成,但mRNA疫苗技術的突破,加速了COVID-19疫苗開發的效率。對於被莫德納提告,《CNN》報導指出,輝瑞公司發言人表示:「目前無法發表評論」。

今年第一批幼兒BNT疫苗127.68萬劑今上午抵台 適用對象曝
中央流行疫情指揮中心今(19)日表示,今(2022)年第一批採購Pfizer-BioNTech幼兒劑型疫苗127.68萬劑,於今日上午抵達桃園國際機場,完成通關程序後,直接運送至指定冷儲物流中心進行後續檢驗封緘作業,檢驗封緘預估8月26日完成,預計8月27日起配送各縣市政府,再提供給6個月至4歲幼兒基礎劑接種使用。本批效期至2023年4月30日。指揮中心指出,已於今年7月21日與香港復星公司及德國BioNTech公司簽署COVID-19疫苗供應協議第一次修正合約,並與美國Pfizer公司及德國BioNTech公司簽署兒童疫苗補充協議第一次修正合約,預定供應190萬劑幼兒劑型及110萬劑兒童劑型疫苗做為幼兒基礎劑(3劑)及兒童基礎劑(2劑)或追加劑使用。(圖/指揮中心提供)
第四批兒童BNT疫苗到了 59.04萬劑今日抵台
中央流行疫情指揮中心今(4)日表示,今(2022)年第四批採購Pfizer-BioNTech兒童劑型疫苗59.04萬劑,於今日上午抵達桃園國際機場,完成通關程序後,直接運送至指定冷儲物流中心進行後續檢驗封緘作業,再提供給5-11歲兒童接種基礎劑使用(包含第二劑,及尚未接種第一劑者,如確診後已間隔3個月者接種)。本批效期至今年12月30日,今年採購的兒童劑型疫苗已全數到貨,共計220.32萬劑,分別為首批5月16日77.76萬劑、第二批5月30日33.12萬劑、第三批6月20日50.4萬劑及本批59.04萬劑。指揮中心指出,已於今年4月28日與香港復星公司及德國BioNTech公司簽署COVID-19疫苗供應合約,並與美國Pfizer公司及德國BioNTech公司簽署兒童疫苗補充合約,預定供應220萬劑兒童劑型及180萬劑成人劑型疫苗做為基礎劑、基礎加強劑或追加劑使用,並視需求擴充400萬劑成人劑型疫苗,以因應SARS-CoV-2變異病毒株之威脅。(圖/指揮中心提供)
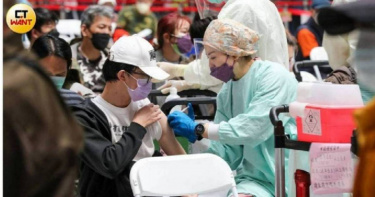
輝瑞、BNT將開始測試冠狀病毒通用疫苗 以提供持久變異保護為目標
美國輝瑞與德國BioNTech是疫苗方面的合作夥伴,2間公司共同宣布,將在下半年展開下一代疫苗測試,以預防多種冠狀病毒。《路透社》報導,他們對超越當前方法的疫苗進行的實驗工作包括T細胞增強疫苗,旨在主要在病毒變得更加危險時預防嚴重疾病,以及預防更廣泛的病毒家族及其突變的泛冠狀病毒疫苗,其目標是提供持久的變異保護。這兩個合作夥伴是西方世界使用最廣泛的COVID-19疫苗的製造商,目前正在與監管機構討論他們已建立的疫苗的增強版本,以更好地防止Omicron變異株及其子譜系。病毒持續變異為更容易逃避疫苗保護的新變種,以及減弱人類免疫記憶,促使公司、政府和衛生機構尋找更可靠保護工具的緊迫性。BioNTech表示,正在獨立研究精準抗生素,以殺死對目前可用的抗感染藥物產生抗藥性的超級細菌。不過BioNTech沒有透露試驗何時開始,這項計畫仰賴於去年10月收購的生物技術公司PhagoMed的技術。由於抗生素過度使用和抗生素生產過程中洩漏到環境中,造成抗藥性感染正在上升。公共衛生研究人員估計,美國和歐盟每年死於抗生素抗藥性感染的總人數接近7萬人。
今年第三批BNT兒童疫苗到了 50.4萬劑上午抵臺
中央流行疫情指揮中心今(20)日表示,今(2022)年第三批採購Pfizer-BioNTech兒童劑型疫苗50.4萬劑,於今日上午抵達桃園國際機場,完成通關程序後,直接運送至指定冷儲物流中心進行後續檢驗封緘作業,再提供給5-11歲兒童接種基礎劑使用。本批效期至今年9月30日,目前共有161.28萬劑到貨,分別為首批5月16日77.76萬劑、第二批5月30日33.12萬劑及本批50.4萬劑。指揮中心指出,已於今年4月28日與香港復星公司及德國BioNTech公司簽署COVID-19疫苗供應合約,並與美國Pfizer公司及德國BioNTech公司簽署兒童疫苗補充合約,預定供應220萬劑兒童劑型及180萬劑成人劑型疫苗做為基礎劑、基礎加強劑或追加劑使用,並視需求擴充400萬劑成人劑型疫苗,以因應SARS-CoV-2變異病毒株之威脅。(圖/疾管署提供)