
AZ公司坦承疫苗「真有血栓風險」 疾管署:有新事證5年內可重提疫苗救濟
英國製藥巨頭阿斯特捷利康(AstraZeneca)疫情期間和英國牛津大學合作研發AZ新冠疫苗,卻爆出多起嚴重副作用,目前累計遭到51位患者集體求償約1億英鎊(約新台幣40.8億元);阿斯特捷利康公司近日首次公開坦承,AZ疫苗的確有可能「在極罕見狀況下」引發血栓合併血小板低下(Thrombosis with Thrombocytopenia Syndrome,TTS),嚴重恐導致死亡。對此,疾管署發言人曾淑慧2日表示,疾管署會與食藥署持續密切關注,一旦有新事證,民眾也可以重新提出疫苗救濟申請。據外媒《每日電訊報》報導,英國男子傑米史考特(Jamie Scott)在2021年4月接種AZ新冠疫苗不久,大腦就發生血栓及腦出血,不僅在住院期間3次被判病危,出院後也無法再工作,被判定已造成永久性腦損傷。史考特2023年對阿斯特捷利康提出告訴,指控疫苗害他平白無故蒙受人身健康和間接財物損失;目前英國高等法院已受理包括史考特在內的51起類似案件,總求償金額達到1億英鎊。過去,面對多起疫苗相關訴訟,阿斯特捷利康始終否認指控。然而在2024年2月一份提交給英國高等法院的法律文件中,阿斯特捷利康首度坦承:「在極端少數的案例下,會造成罕見血栓併血小板低下症候群。」台灣疾管署發言人曾淑慧表示,台灣已密切注意這類國際訴訟案件。疾管署與食藥署正在共同監控疫苗的安全性和效力,同時提醒民眾,在符合條件的情況下,可以重新提出預防接種受害救濟申請(疫苗救濟申請)。此外,政府亦強調,預防接種受害救濟審議過程將會保持獨立及專業,確保公平公正。此事件也引起了立法者的關注,立委廖偉翔與陳昭姿質疑疾管署的受害救濟案件審議過程草率,指出審議過程需更加透明和有條理。對此,曾淑慧強調審議過程是依法進行,合法合理,且確保預防接種受害救濟審議小組獨立行使職權;審議小組則秉持醫學專業並以審慎客觀之態度,全力取得事證方作成結論。

日本正露丸驚爆檢測報告造假30年 製藥商遭勒令停產停售
日本富山縣富山市藥品製造公司極東KYOKUTO(キョクトウ)以腸胃藥正露丸而聞名,但近日卻被爆出,從2021年12月開始就多次造假檢測結果以符合規定標準,該產品目前已自主召回,並已確認不存在健康危害。對此,當局勒令極東藥品公司從4月30日起停產23天及為期22天的停業令。綜合日媒報導,富山市26日發布消息稱,根據《藥品和醫療器材法》,極東藥品公司其主要商品正露丸,從2021年12月後就多次竄改實驗數據,藉此符合規定標準,該產品目前已自主召回,並已確認不存在健康危害。對此,富山縣政府下令極東藥品公司從2024年4月30日至5月22日為期23天的停產令及為期22天的停業令。起初富山縣政府是於2022年7月發覺異樣,極東隨即展開公司內部調查,讀賣新聞報導還指,造假情事已持續至少30年。至於捏造虛假檢測記錄的原因,負責人則表示「負責檢測的人已經退休了,所以我們不知道他為何下令製作虛假檢測記錄。」極東藥品公司表示「我們鄭重對待處罰,並將努力挽回消費者的信任。」

不只軟毛青黴酸 日厚生省再查小林製藥紅麴原料…又檢出2異物
日本小林製藥因其紅麴原料內含「軟毛青黴酸」,證實會影響食用者的腎臟問題,進而引發極為龐大的食安危機。後續日本厚生勞動省再次調查小林製藥的紅麴原料,結果在當中又發現了2種通常不會加入產品的異物。根據《NHK》報導指出,日前日本厚生勞動省和國立衛生研究所再次分析小林製藥在2023年6至8月的原材料後,發現當中除了先前檢出的軟毛青黴酸外,另外還發現2種通常不太會加入產品的異物。但目前官方並未公布2種異物的名稱,同時這2種異物是否影響人體還有待調查。據了解,整起事件源自於3月22日,小林製藥主動在官方網站發文表示,一名顧客從2021年4月至2024年2月期間,連續3年購買、服用小林製藥旗下的紅麴保健品,最終2月時因腎臟疾病而離世。而整起事件曝光至今,已累計有1434人通報,當中有240人因此住院,而有5人則不幸身亡。

台灣人吃小林製薬「紅麴」產品…53人通報不適 食藥署宣布再開專家會議
日本製藥大廠「小林製藥」含紅麴成分的保健食品,造成民眾服用後出現腎臟疾病,目前已累積5人死亡,114人住院治療,而台灣也有業者輸入相關產品,累計53人通報不適。對此,食藥署將於明(19日)2度召開專家會議,協助消費者求償等權益。日本不少民眾服用小林製藥紅麴機能性保健食品後,出現急性腎衰竭死亡,該產品也驗出毒性極強的「軟毛青黴酸」,雖然還沒證實因果關係,但造成死亡和住院案例,引發國際關注。台灣方面,食藥署陸續公佈下架產品名單,截至昨(17日)已累計248件產品,並開放消費者通報非預期反應,民眾必須提供食用批號、效期和病歷等資料。食藥署副署長林金富指出,之前已經召開過「健康食品、特殊營養食品及膠囊錠狀食品非預期反應諮議小組」,但有部分消費者提供的相關資料比較亂,所以上次會議主要是彙整資料,並聯繫消費者補充資料。林金富透露,明天會召開第2次專家會議,參與專家包括醫師、學者以及民間團體代表等,會議上會進行最後評估,討論完就會有決定結果,因為日本方面已經坦承食用對健康有影響,食藥署也會跟消保官一起協助消費者做後續求償等權益。

用餐後嘔吐、腹瀉就是食物中毒? 醫曝這些症狀恐是「過敏發作」
台灣食安問題連環爆,從蘇丹紅辣椒粉、小林製藥紅麴補充品、寶林茶室米酵菌酸中毒案,到王品旗下的初瓦、嚮辣,甚至藏壽司、八方雲集等也出包,導致民眾現在外出用餐後若出現身體不適,直覺都會聯想到是食物中毒。對此,林口長庚風濕過敏免疫科也在臉書粉專發文分享,如何分辨食物過敏與食物中毒,「若發覺症狀持續或惡化,請務必立即就醫。」食物過敏食物過敏是人體免疫系統對某種食物產生抗體,對抗外來物時會釋放組織胺,過多的組織胺造成過敏反應。而常見的食物過敏反應包括:皮膚紅疹發癢、嘔吐、腹瀉、腫脹,嚴重可能引發呼吸困難、低血壓、過敏性休克等症狀。食物中毒食物中毒是食物被細菌或病毒污染後又被吃下肚。根據衛福部食藥署定義,「食品中毒案件指2人或以上攝取相同食品引發相似症狀」。而常見的食物中毒反應包括:腹瀉、噁心、嘔吐、發燒、虛弱、血便等症狀。林口長庚風濕過敏免疫科粉專也提醒,若出現不適現象,應避免再吃下可能導致症狀的食物,並且仔細觀察症狀的變化,若發覺症狀持續或惡化,請務必立即就醫。

小林製藥爭議後…日本消費者廳徹查6795種保健食品 18款爆出健康危害報告
日本製藥大廠「小林製藥」3款含有紅麴成分的保健食品,造成服用者出現腎臟疾病,目前已累積5人死亡,114人住院治療。對此,日本消費者廳12日公布了針對1693家公司的6795種保健食品的緊急檢查結果,報告顯示曾有醫療專業人士對其中18種產品提出至少117件健康危害報告。綜合日本Goo、《每日新聞》的報導,小林製藥事件後,日本消費者廳針對1693間公司是否報告健康危害進行問卷調查。截至11日,當局已收到1395家企業之5551種產品的回覆,約佔整體的80%。在18種被醫療專業人士報告有健康危害的產品中,一半是補充劑,且有11家企業出售了這些產品。雖然目前117件健康危害報告中尚未傳出死亡案例,且大多數為輕症,但仍有幾名患者住院治療,這些輕微症狀包括腹瀉和濕疹,而住院患者人數方面則並未透露。部分案例目前尚未證實與產品有因果關係,且調查結果通篇未透露公司及產品名稱。該行政機關解釋,沒有任何產品需要立即採取下架行動,因為尚不能推論任何產品與特定症狀相關,不過這117件健康危害報告無一申報到政府機關。報導補充,在食品功能標籤制度下,如果公司按照國家指導方針提交申報,便可以在食品中標註其功效及功能等,無需經過國家審查,僅需基於《食品標籤法》的食品標籤標準要求及時報告任何健康危害。不過,小林製藥在事件爆發後2個月才向政府報告此事,導致消費者廳必須主動開始調查其他企業。

食藥署指王品案驗出諾羅病毒 廚師若抱病上班將依食安法開罰
食藥署副署長林金富指出,「王品」集團餐廳爆發疑似中毒案件,到目前為止,疑似出現症狀向衛生機關通報者已經有82人,經過食藥署、疾管署及地方衛生局檢測,已經從完成採檢的20人的人體檢體中檢測出有「諾羅病毒」,地方衛生局也對患者檢體及廚工進行人體採樣,手部及廚具刀具的環境採樣,目前都仍持續檢驗中。由於諾羅病毒常見在腸胃道疾病感染者身上出現,外傳王品疑似有身體症狀的廚師抱病上班才導致此次中毒事件,媒體今日也詢問食藥署。林金富說明,食安法規定,如果廚工或食品從業人員生病,就是應該請假、不得上班,以免發生傳染病傳給消費者,如果稽查確有廚工抱病上班情況,將按食安法開罰,這也是地方衛生局稽查、檢體採樣的重點。林金富說,目前的季節是諾羅病毒好發季節,至於外界一度懷疑的仙人掌桿菌則是好發在炎熱的夏季,例如煮好的飯,容易讓仙人掌桿菌孢子活化,若儲存環境不當或者煮好後很久才食用,被活化的桿菌就容易產生毒素,因此要特別提醒餐飲業者及消費者注意,防治諾羅病毒及細菌性引起的食品中毒,尤其諾羅病毒宿主是人,很容易傳染到即時食品,食品業員工健康管理相當重要。王品集團旗下的韓式料理「初瓦」、和牛麻辣鍋「嚮辣」日前爆出食物中毒事件,截至目前為止已累積82人通報身體不適。此外,針對日本小林製藥紅麴原料致死事件,林金富也表示,到目前為止,日本小林製藥生產的有問題紅麴原料,進入台灣的共有兩批,分別是320-23711R及320-23308R,分別由兩家國內業者引進,目前相關產品已經下架24,205盒。林金富說,目前業者多願意配合食藥署規定,將有問題的產品下架,他也感謝業者的配合。他也說,日本小林已在小林製藥台灣分公司設立聯繫窗口,消費者可以向使用小林紅麴做為原料的生產業者及台灣小林進行諮詢,如果無法得到令消費者滿意的結果,也可以向全國的消保官尋求協助。未來消費者如果要打團體訴訟,行政院消保處會提供必要協助,衛福部食安基金也會提供律師費補助。

日方通知我小林紅麴食安事件 將在台灣小林設聯繫窗口
衛福部食藥署今天舉行記者會,由食藥署副署長林金富主持,針對台灣業者使用日本小林紅麴原料生產的製品,引發消費者身體不適進行說明。食藥署食品組組長鄭維智表示,目前有105家台灣業者通報使用到小林製藥的紅麴,通報案件數有245家。食藥署整理目前累計的非預期反應通報案件有34件,其中健康食品有8件,一般食品有26件。食藥署指出,根據日本IHR國際衛生條例規定,日方已經小林紅麴事件向我方通報,日本小林紅麴事件的聯絡資訊及處理窗口設在台灣小林藥業,消費者如果直接買到日本小林製藥的紅麴產品,或者日本產品含有小林製藥的紅麴原料,可以到台灣小林藥業的官網登記諮詢,受理時間是週一到週五上午九點到下午五點。其次,消費者如果買到的是國內業者的產品,卻含有小林紅麴原料,消費者就必須向該業者洽詢退款等事項,萬一無法得知製造業者,也可以與台灣小林製藥客服專線聯絡,小林製藥台灣分公司在四月底前受理諮詢。食藥署提醒,民眾如果吃到以小林紅麴為原料的保健食品或者健康食品,若覺得有不適,可以同時向食藥署通報,由於日本仍持續調查此案的原委,也提醒國內消費者注意,如果消費者提供的資料越完整,將更有助於未來專家學者評估,是否因為小林紅麴原料導致消費者的「非預期反應,也就是所謂的「相關性」,這可能與後續求償有關。食藥署指出,如果消費者通報當時並沒有身體不適,也仍沒有就醫,也沒有關係,食藥署仍會彙整資料,若未來消費者要打團體訴訟,食藥署會將相關資訊轉介給消保團體及行政院消保單位。日本小林製藥紅麴保健品導致腎臟相關疾病的食安風暴,由於影響範圍不小,引發外界矚目。到目前為止,日本國內已有5起死亡病例,就醫民眾擴大至1120人,日本厚生勞動省9日公布5名死者的重大疾病史,並公開日本腎臟病學會的調查結果。

臨床第一線抗生素驚見「結晶」!食藥署回收問題批號 共5.7萬瓶
衛福部食藥署近日接獲多起通報,南光化學製藥股份有限公司生產的「克力欣注射液150公絲/公撮(克林達黴素)」有結晶情形,疑似品質不良,今(9日)宣布回收同批號共5.7萬瓶。據悉,該藥品是臨床第一線抗生素用藥,主要用於由厭氣菌、鏈球菌等感染症,市占率高達75%,健保年度用量有52萬多瓶。食藥署近日接獲3家醫院通報,指南光化學製藥股份有限公司生產的克力欣注射液150公絲/公撮(克林達黴素)CLINCIN INJ. "N.K." 150MG/ML(CLINDAMYCIN),衛署藥製字第031368號、批號2H3557,有結晶情形,故啟動回收,共 57,471瓶。食藥署說明,該藥品主成分為clindamycin(as phosphate),主要用於由厭氣菌、鏈球菌、葡萄球菌、肺炎雙球菌等具有感染性菌株所引起之感染症。倘對用藥有疑慮者,應儘速回診與醫師討論,處方其他適當藥品。請各醫療院所、藥商、藥局配合辦理回收作業,立即停止調劑、供應。食藥署已要求廠商應於113年4月28日前完成回收作業,並應繳交回收成果報告書及後續預防矯正措施,若逾期未完成,可依法開罰新台幣20萬到500萬元。據悉,該藥品是臨床第一線抗生素用藥,市占率高達75%,健保年度用量有52萬多瓶。由於還有其他批號供應,且國內也有同成份、同劑型、同劑量的多張許可證,因此本次回收不會造成缺藥情形。
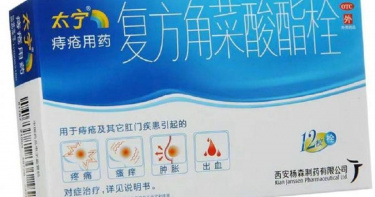
大陸「知名痔瘡藥」全面停產 價格半年飛漲17倍!全網崩潰:沒有它我怎麼活
大陸知名痔瘡用藥「太寧栓」因原料短缺全面停產,如今每盒價位已從22.5元人民幣(約新台幣99元),暴漲至398元人民幣(約新台幣1766元),足足翻倍飆漲了17倍,引起大批患者哀號。綜合陸媒報導,西安楊森製藥有限公司去年發布停產聲明,表示由於「全球已無原料可持續供應生產」,因此自2023年11月起,停止太寧栓劑的生產及市場供應。事實上,太寧栓是一種外用非處方藥,主要用於治療痔瘡及其他肛門疾病,有助緩解疼痛、搔癢、腫脹與出血等不適症狀。據悉,先前「太寧栓」每盒最便宜只要22.5元人民幣(約新台幣99元),不過停產加上市場嚴重缺貨,導致該痔瘡用藥暴漲至398元人民幣(約新台幣1766元),短短5個多月一路飛漲了17倍之多。對此,不少網友紛紛哀號,「我的痔瘡怎麼辦」、「太寧栓,沒有你我怎麼活」、「不要啊!這個真的超級好用啊」、「完蛋了,我以前就只能用這款才能消腫的」,而太寧栓在孕婦群中也廣受好評,「懷孕的時候唯一能用的栓劑就是這個了,不能停呀」、「孕期唯一能用的痔瘡外用藥,一顆見效」、「生完小孩就是用的這個,讓我少受了很多很多罪」、「孕婦沒有這個才難,能用的痔瘡藥基本只有這個。」另外,也有人驚呼漲得太離譜,「去年買兩盒才70多塊」、「這漲價也太狠了吧」、「年初買得價格才25塊,後悔沒有多買點」、「太可怕了,今早已花1190買5盒。」
Fed降息+併購增加 大摩:生技股將反彈有望優於大盤
外媒報導,華爾街投行摩根士丹利(大摩)認為,美股的生物科技股可望反彈,因聯準會即將降息,開始調降利率,加上大型企業併購行動增加,資金面對於生技類股也更為有利,將推動生技股表現優於大盤。大摩最近報告對歷史數據的回顧顯示,生物技術板塊在首次降息前的幾個月裡,表現一直優於大盤,但隨後大約一個月將表現不佳,但此後股價將再次攀升,該產業未來6至12個月的升值幅度一般在20至30%左右。該行表示,預計聯準會將在6月首次降息,2024年總共降息4次,每次25個基點。從歷史上看,較低的利率也伴隨著併購活動的增加。去年全球生技併購案已經開始有加溫現象,由於大型藥商到2030年將面臨「專利斷崖」,市場認為大型公司將持續收購具有前景公司,以補足收入損失。該行表示,除了利率前景之外,認為中小型市值(SMID)生物技術併購仍有需求。由於小型生技公司缺乏現金,且目前估值相對較低廉,也吸引大型企業購入。預估未來併購案可持續帶動生技股股價表現。據摩根士丹利估計,到2030年,2024年營收1820億美元的藥物(佔全年總營收的41%)將失去專利保護。安進(Amgen)面臨的損失最大,佔其2024年營收的68%,其次是必治妥施貴寶(Bristol Myers Squibb)的64%,默沙東(MSD)的56%,嬌生製藥部門51%,以及輝瑞(Pfizer)的40%。同時,摩根士丹利認為該產業的併購能力為4680億美元。嬌生位居潛在併購能力榜單之首,諾和諾德、默沙東、羅氏和諾華製藥位居前五名。該行認為,腫瘤和免疫資產將繼續成為潛在收購者最感興趣的領域,中樞神經系統、神經科學也引起了關注。摩根士丹利也認為,整個產業的公司將繼續專注於價值低於50億美元的交易。

外媒:減肥神藥Wegovy對心臟衰竭患者有效 分析師上調目標價至144.5美元
外媒報導,一份自昨天(6日)發佈在醫學期刊《新英格蘭醫學期刊》(NEJM)上的最新研究報告表明,對於心臟衰竭(HFpEF)患者,特別是那些伴有肥胖的收縮分率保留的患者,接受諾和諾德(Novo Nordisk)旗下的「減肥神藥」Wegovy治療後,體重減輕更明顯,嚴重不良事件發生率更低。丹麥製藥巨頭諾和諾德旗下Wegovy主要成分為司美格魯肽,可用於助肥胖者預防心血管疾病、心臟病、中風等風險。經最新研究證實,該藥對患有糖尿病和心臟衰竭病人的健康也有益處。心臟衰竭的患者通常很容易疲勞、呼吸困難,這種情況可能會導致住院、殘疾和死亡的高風險。目前治療心臟衰竭的方法包括改變生活方式和心臟病藥物,但沒有專門批准治療心臟衰竭的療法,而且患有這種疾病的人數一直在顯著增加。去年秋天,研究人員發佈的研究顯示,Wegovy對患有這種心臟病的人,有顯著的積極健康作用。報導中引述研究人員、心臟病專家Mikhail Kosiborod博士的話表示,最新研究和去年發表的研究的一致結果似乎表明,Wegovy對於廣泛的人群,包括糖尿病患者,是一個有效且安全的治療選擇。Kosiborod還向美國心臟病學會介紹了這項研究,他認為這一發現非常令人興奮,因爲心臟衰竭患者通常難以治療,而且這類患者的數量在不斷增加。但現在Wegovy不僅顯示出了治療效果,而且耐受性良好,這代表患者可以很好地承受這種治療,沒有出現嚴重的副作用。此外,諾和諾德去年全年按本幣和固定匯率計算的營收分別年增31%、36%至2323億丹麥克朗(337.1億美元),這表明營收收入大幅增長;按本幣計算的營利也年增37%至1026億丹麥克朗。並預估,2024年按固定匯率計算的營收成長,將介於18至26%之間;營利成長將介於21至29%之間。分析師近期也對諾和諾德提供了12個月的目標股價,平均目標價為144.5美元,最高估值160美元、最低120美元;目前的平均價格已從之前的125美元上漲了15.6%。諾和諾德股價截至5日收盤,上漲6.9丹麥克朗或0.8%,收在867.5丹麥克朗。

小林製藥紅麴風波延燒!不良通報累計26件 食藥署下架246件產品
日本多名消費者服用小林製藥含紅麴保健食品後,陸續罹患腎臟疾病,甚至有5人死亡,引發軒然大波;台灣部分,有業者曾輸入相關原料,且陸續有民眾通報食用後出現身體不適情形。據食藥署統計,目前累計不良反應通報有26件,已累計下架246件相關產品。截至4月4日,食品藥物管理署已收到使用含日本「小林製薬」公司紅麴原料相關產品之「國內業者主動通報預防性下架資訊」共計246件。另,「全國健康食品、特殊營養食品及膠囊錠狀食品非預期反應通報系統」(下稱非預期反應通報系統),已收到民眾食用含日本「小林製薬」紅麴原料相關產品之通報案件共計26件。食藥署表示,民眾通報時,除填寫基本資訊外,應提供食用產品之批號或效期、病歷、同時所使用之其他藥物、生理檢驗檢查結果及腎臟功能之系列性變化等資料,以利後續評估分析食用產品與非預期反應的相關性。食藥署提醒,民眾買到含有日本「小林製薬」紅麴原料相關產品,如有疑義,可撥打食安專線1919或消保專線1950諮詢,行政院消費者保護處已發函全國消費者保護官協助處理退換貨事宜。此外,食品安全保護基金亦可補助消費者保護團體,協助消費者進行團體訴訟。

國內累計11起小林紅麴通報「9人腎受損」 患者症狀曝
日本發生消費者服用小林製藥含紅麴保健食品後陸續罹患腎臟疾病,甚至有5人死亡,而台灣有業者曾輸入相關原料,且陸續有民眾通報食用後,身體出現不適症狀。據食藥署2日統計,目前收到11件通報,11例通報年齡皆超過40歲,另有2人未確定,其通報症狀,包含全身疲勞、腎絲球過濾率有異常、腎功能受損、急性腎衰竭及慢性腎臟病等。據食藥署2日統計,截至1日,全國健康食品、特殊營養食品及膠囊錠狀食品非預期反應通報系統」,已收到與小林製藥有關紅麴產品案件通報共11件,包括3件健康食品,分別為1件「諾寶紅麴膠囊」及2件「大醫生技紅麴膠囊」,保健功效皆為「調節血脂」。另8件通報的一般食品產品,分別為3件「大研納豆紅麴Q10膠囊」、2件「達摩本草納豆紅麴素食膠囊」、1件「御熹堂日本專利紅麴納豆Q10」、1件「紅景天納豆紅麴膠囊」、1件「小林製薬紅麴膠囊(日本購入)」;至於國內業者主動通報預防性下架資訊方面,目前維持226件主動下架。至於個案通報狀況,目前有11例通報,其患者年齡都大於40歲,其中2人未確定,目前則知年齡最高為73歲,服用最長時間為3至4年、最短6個月。症狀方面,包括感到疲累、腰痠、腰痛、腎絲球過濾率異常、腎功能受損、腎臟些微萎縮、頭暈、血壓高、噁心、想吐、腎功能異常、腎指數下降並合併有蛋白尿、急性腎衰竭和慢性腎臟病等。是否有同時服用其他藥品部分,仍有待確認。