歐洲藥品管理...
」 疫苗 AZ疫苗 歐盟 副作用 血栓
精神醫師提警告!薩滿拿「蘑菇」治療患者 南非地下迷幻產業越禁越旺
在南非當地,迷幻藥雖屬非法,但越來越多自稱薩滿或治療師的人,正於開普敦(Cape Town)周邊公開宣傳以這些藥物進行所謂「靈性療癒」。根據《BBC》報導,這股無監管的地下治療潮流持續擴散;儘管法律明定,若以商業目的販售或使用迷幻藥,最高可面臨25年監禁與罰款。53歲的攝影師道茲(Stuart Dods)是這類「薩滿療程」的參與者之一。他在開普敦郊外一間木屋中準備展開第二次迷幻體驗,目的是治療多年心理創傷。道茲曾接受處方藥治療,但認為迷幻藥才讓他「重新活過來」。他說「媽媽的去世讓我整個崩潰,一年後伴侶又離開我,那時人生像被抽走地毯。」這場為期一天的儀式花費約2,000美元,包含住宿、指導與兩種藥物,分別是裸蓋菇素(psilocybin,魔菇)與搖頭丸(MDMA)。帶領儀式的主持人哈蒂(Megan Hardy)自稱「藥草女人」(medicine woman)。她在開始前也服用少量藥物,稱能與受治者「進入相同頻率」。哈蒂解釋「薩滿的概念是,一腳踏在兩個世界之間。」明知違法,她仍認為這是「正義的公民不服從」。至於劑量掌握,她表示靠多年在自己身上實驗累積經驗。道茲的療程被《BBC世界服務》(BBC World Service)全程拍攝。他躺在地板上,蓋著灰色毯子、戴眼罩,藥效發作後情緒明顯波動。哈蒂與助手佛格森(Kate Ferguson)一邊唱誦、一邊用鳥翼輕拍進行「薰香淨化」(smudging),燃燒藥草以驅除「負能量」。兩人皆無醫學訓練,但都服用少量藥物。當道茲被問是否再服用更多 MDMA 時,他僅回「我不知道」,最終仍服下。事後,《BBC》問他在意識改變狀態下是否仍能同意,他答「這不是強迫,我有機會說要或不要。」然而,南非精神科醫學會(South African Society of Psychiatrists)召集人斯塔斯尼(Dr. Marcelle Stastny)警告「能給出同意必須與現實保持連結。服用迷幻藥後,人是醉的、嗨的,這種情境下同意是不存在的。」近年,隨臨床研究顯示迷幻藥對憂鬱、焦慮與創傷後壓力症候群(PTSD)具潛在療效,全球對此治療的關注暴增。2022年一項涉及233人的研究發現,25毫克合成裸蓋菇素搭配心理支持可改善憂鬱症狀。不過,歐洲藥品管理局(European Medicines Agency)於2025年的回顧分析指出,目前臨床證據仍不足,並提醒迷幻藥會使心率與血壓升高,必須在受控環境施用。在南非,這類「迷幻治療」市場正快速膨脹。斯塔斯尼警告「尤其在開普敦,這已成爆炸性成長。人們迷失、脫節,想找一顆能解決所有問題的藥丸,但那根本不存在。」幾年前,另一位薩滿引導師希爾(Sonette Hill)在給病人服用伊波加鹼(Ibogaine)後,病人突然暴怒掐住她的喉嚨。這種源自非洲雨林的植物萃取物雖能治療成癮,卻屬高危迷幻藥。2024年,一名牙醫吉瓦(Dr. Anwar Jeewa)在未登記診所替26歲男子馬提諾維奇(Milo Martinovic)施用伊波加鹼後導致其死亡,被判過失殺人罪。儘管風險重重,網路仍充斥提供「療癒旅程」的廣告。斯塔斯尼說「有些人只是服過藥覺得被啟發,就自認能幫別人;更糟的是那些覺得自己比精神科醫師更神的人。」回到開普敦的木屋,道茲的藥效逐漸退去。他說自己尚未痊癒,但覺得正「朝治癒的路上」前進「我能感覺到某些東西被打開,也許之後我還會再來一次。」

罕病AADC基因治療「價格近億」納健保採採分期支付 首年估13人受惠
AADC缺乏症是一種遺傳性罕見疾病,通常在嬰兒早期出現症狀。由台大醫院團隊研發的AADC基因治療,2022年獲歐盟上市許可,價格近億元。健保署藥物共擬會今天(21)審查通過健保給付,將和廠商啟動價量協議,預計最慢今年11月開始給付,預估第一年13名患者受惠。芳香族L-胺基酸脫羧基酶缺乏症 (AADC)是先天基因缺損,通常在嬰兒早期出現症狀,導致嚴重的發展遲緩、動眼危象、低張力及四肢運動異常、自律神經系統失調、睡眠問題及情緒障礙等。AADC基因治療是2010年由台大醫院基因醫學部提出「AADC治療計畫」,並陸續獲得AADC缺乏症病友會、罕見疾病基金會、長榮集團張榮發總裁及生技醫藥國家型科技計畫(NRPB)的支持贊助,之後技轉給美國藥廠。歐洲藥品管理局(EMA)於2022年核准這項基因治療藥物上市。健保署副署長龐一鳴證實,今天共擬會通過AADC基因治療納入健保給付,並授權健保署和廠商進行「價量協議」,牌價近億元,實際價格會低一些。共擬會專家認為,由於藥物價格高,採「分期支付」,觀察病人穩定有效才會給付。依據國健署統計至今年7月, AADC罕病通報72人、死亡27人、存活45人。而台灣新生兒發生率約三萬分之一,高於其他國家,如日本約16萬2千分之一、美國約6萬4至9萬分之一、歐盟約11萬6千分之一。龐一鳴表示,此次通過給付的重點不在於價格多貴,這類罕病病童若沒有幫忙就活不久,國家應該盡量照顧,且相對其他國家,台灣病人數較多,早期研發跟技術都是以台灣為基地,再向國際推廣,健保更應該要支持。龐一鳴說明,依照標準流程為2個月,最慢今年11月開始給付,預估給付後第一年使用人數13人。他轉述健保署長石崇良的話,「全台灣每一個人也只付不到5元,可以救一個罕病小朋友,絕對值得!」

「菸」關難解1/加熱菸審查進度延宕兩年 國健署審查機制究竟哪裡卡關?
行政院日前公布院版的立法院下會期優先法案修法,其中包括兩年前修正菸品「一禁一管」政策的《菸害防制法》,然而被納入管制的加熱菸至今卻一直卡在衛福部無法上市,外界多認為係衛福部刻意營造模糊遊戲規則「技術卡關」所致,如今《菸害防制法》再度提出審議,料將引發各方角力。《菸害防制法》於112年3月22日修正上路,對於新型煙品採「一禁一管」方式,法條「一禁」所謂係指全面禁止電子煙之類菸品,「一管」則將加熱菸納入管制,且業者所提資料必須通過「健康風險評估審查機制」才可製造、輸入,而至今近2年時間過去,卻未見一家加熱菸商通過評估。《菸害防制法》修正版於112年3月22日起實施,除全面禁止電子菸外,加熱菸必須通過健康風險評估審查才可上市販售。(圖/報系資料照)衛福部於《菸害防制法》修正版實施同日公告「健康風險評估審查辦法」,規定申請業者應檢附相關資料,並經由國健署邀專家學者開會評估審查才可上市;另訂申請案件處理時間以六個月為最長期限,必要時得予延長六個月,以延長一次為限,而業者補交資料時間不算在其中。根據部份菸商私下抱怨,他們早將相關資料送請福部國健署審查,然而國健署的審查機制卻沒有一套明晰的遊戲規則,導致審查效率奇差,對於加熱菸的上市時間實在不敢樂觀;國健署對外宣稱,因廠商沒有補充要求的資料,因此無法完成審查。民進黨立委陳瑩質疑,若推稱廠商沒有補充資料,國健署迄今開了37場審查會議的開會內容為何?審 查會議內容看似公開透明,遲遲不解決技術性卡關亂象,根本是瀆職。事實上,加熱菸審查辦法確有問題存在,一名知情人士指出,以新藥查驗及指定菸品審查作比較,指定菸品審查補件次數及期限並不明確,導致加熱菸審查完全沒有截止日期。以新藥查驗為例,審查過程中有1次技術補件機會,期限為2個月,得展延1個月;指定菸品補件次數及期間卻沒有明確規範,申請者只得持續補件。《菸害防制法》修法施行滿周年,新北市衛生局已裁處輸入電子煙或加熱菸118件,累計監督銷毀近7000條加熱菸及加熱菸主機、類菸品等違規貨品,國健署遭批延宕加熱菸審議進度,導致稅捐稅收大量流失。(圖/報系資料照)該知情人士續指,指定菸品審查機制也並不精簡,以新藥查驗為例,若得到美國食品藥物管理局(FDA)、歐洲藥品管理局(EMA)或日本厚生勞動省(MHLW)其中兩地區的核准證明,並經評估不具族群差異者,審查時間得從240天縮減至180天,相對指定菸品審查卻未有此機制,對所有菸品採同一程序,不免有浪費行政資源之嫌。至今沒有加熱菸合法上市,也多次遭指造成稅收流失問題。新北市衛生局上月宣布查獲並銷毀6萬多條非法走私入境的加熱菸及電子菸,遭到CLEAN AIR大聯盟發起人彭華幹痛批,政府本可徵收到3108萬元的菸捐和菸稅,卻這樣一把火燒了。依現行有關菸品健康捐及菸稅規定,每包菸的菸捐加上菸稅為51.8元,據推估,加熱菸拖延上市一年的菸捐與菸稅加起來,大約260億到280億元。台酒董事長湯期安日前備詢時坦言,菸防法上路後,很多民眾轉用加熱菸,台灣菸酒遲遲無法銷售加熱菸,已影響到40、50億元的銷量。據了解,國內一年約銷售19億包香菸,如一包紙菸以120元計算,香菸市場一年銷售額約2280億;加熱菸因還未開放,無法推估一年銷售額,依衛福部目前推估,我國人口預估0.5%抽加熱菸。對此,綠營立委表示,加熱菸的市場需求既成事實,拖延上市只會造成走私品流行以及稅收流失,既然加熱菸已合法納管,就應正視政策矛盾,加速加熱菸審查進程,讓其儘快上市,政府才能有效管理產品,確保稅收與消費者安全。◎提醒您:吸菸有害健康、吸菸害人害己。

瘦瘦針增自殺傾向?歐盟本周審查 美國FDA初步認定無關連
在特斯拉執行長馬斯克等名人的帶動下,俗稱「瘦瘦針」、「減肥針」的GLP-1藥物(Glucagon-likepeptide-1 agonists類升糖素胜肽-1受體促效劑)成為炙手可熱的減肥聖物,但從去年起便傳出可能會增加輕生傾向,歐洲藥品管理局 (EMA) 將於本週召開一次會議,審查有關 GLP-1 類減肥藥物與自殺傾向是否有關聯的報告。中國附醫健康醫學中心副院長、台灣肥胖醫學會理事長林文元表示,GLP-1藥物本來是一種降血糖藥,在研發過程中,發現血糖下降的同時,體重也在下降,所以在國外很早就用於減重。瘦瘦針藥物種類相當多,目前台灣大致有Liraglutide、Dulaglutide、Semaglutide等3大類,隨著民眾搶買減肥針,全球都出現短缺狀況。歐洲藥品管理局去年接獲冰島通報,1例使用抑制食慾的胰妥讚(Semaglutide類藥物)後導致出現自殺念頭、1例使用善纖達(Liraglutide類藥物)想自殺、另1例使用善纖達出現自殘想法。Liraglutide、Semaglutide類藥物均由諾和諾德(Novo Nordisk)製造。目前歐盟藥物產品訊息中並未將自殺行為列為副作用,相關產品的安全性將由「藥品監測暨風險評估委員會」(Pharmacovigilance Risk Assessment Committee, PRAC)進行評估,日後將考慮是否將審查範圍擴大到「類升糖素胜肽-1受體促效劑」(GLP-1 receptor agonists)的其他藥物。諾和諾德對此回應,GLP-1受體促效劑應用於治療第2型糖尿病已有超過15年的歷史,用於治療肥胖症也有8年的歷史。從大型臨床試驗項目和上市後監測收集的數據中,並無證據顯示其藥物與自殺自殘傾向存有關聯。諾和諾德強調會持續監測正在進行的臨床試驗和實際使用其產品的數據,並與當局密切合作,以確保患者安全和向醫療保健專業人員提供足夠的信息。美國食品藥物管理局 (FDA) 今年1月的初步審查發現不存在自殺關聯,不過,FDA同時警告,鑑於數據有限,不能完全排除有這種風險的可能性,之後將繼續關注這一問題。

減肥藥市場過熱? 美專家示警:增長趨勢難延續因「這2點」
「減肥神藥」司美格魯肽(semaglutide)是一種類升糖素胜肽-1(GLP-1)受體的促效劑,能達到降糖減重的效果。有研究結果顯示,除了減重外,還可以應對心血管疾病、酒精成癮、癡呆等症狀。摩根大通先前預計GLP-1類藥物年銷售額,到2030年將達1000億美元,不過有專家對此提出質疑,且未來隨著更多人服用該藥物,相關保險的涵蓋範圍將面臨挑戰。內科醫生、曾擔任白宮衛生政策主任的帕特爾(Kavita Patel)博士日前受CNBC採訪時表示,諾和諾德發佈的關於Ozempic延緩慢性腎病能力的最新數據,是該藥物第二種用途的有力支持證據之一,但證實能治療酒精成癮、阿茲海默症等疾病的數據並不完全。更重要的是,帕特爾指出,限制減肥藥市場前景的一大重要因素便是醫療保險。目前基本沒有醫療保險覆蓋此類藥物,因此患者只能靠自費。在沒有保險的情況下,這些藥物每月的花費可能高達1000美元,這顯然不是大多數人能承受的。與此同時,瑞穗(Mizuho)的醫療保健行業策略師霍茲(Jared Holz)認為,諾和諾德和禮來的這種增長趨勢可能不會持續,因為目前的供應限制使患者無法獲得足夠劑量。他補充道,鑒於股票的交易情況,這些公司無法真正提供能夠安撫投資者的收入。更為GLP-1類藥物的未來添加不確定性的則是其本身效果和副作用,目前還需要更多研究數據來證明其有效性和安全性。歐洲藥品管理局此前曾警告,GLP-1類藥物具有引發甲狀腺癌的潛在風險。目前多國醫藥監管機構正在審查這些藥物導致抑鬱和自殺的風險。本月,一項發表於《美國醫學會雜誌》的研究還稱,Wegovy和Ozempic等減重藥物可能會增加非糖尿病患者患胃麻痹、胰腺炎、腸梗阻和膽道疾病的風險。

「瘦瘦筆」疑似引發輕生念頭! 歐盟宣布展開調查
瘦瘦筆近年在減肥圈爆紅,然而歐洲藥品管理局(The European Medicines Agency ,EMA)近期表示,已接獲冰島通報,1例使用抑制食慾的胰妥讚(Ozempic)後導致出現自殺念頭、1例使用善纖達(Saxenda)想自殺、另1例使用善纖達出現自殘想法,將對此展開調查。名人效應 減肥針全球短缺名人在社交媒體上大量分享減肥貼文,吸引民眾跟風。目前善纖達和Wegovy已獲得減肥核准和許可。Ozempic適用於糖尿病患者,有助於控制血糖和體重。隨著民眾購買填充式減肥針,全球都出現短缺狀況。綜合外媒報導,胰妥讚為GLP-1受體促效劑,主要成分為semaglutide(索馬魯肽),核准用於治療第2型糖尿病;而善纖達含有類似的成分liraglutide(利拉魯肽),核准用於長期體重管理。兩者均由諾和諾德(Novo Nordisk)製造,由於許多非糖尿病患買來用於減重,經常處於全球缺貨狀態。EMA表示將針對善纖達、Wegovy、胰妥讚及其他類似減重藥物進行安全評估。目前歐盟藥物產品訊息中並未將自殺行為列為副作用,相關產品的安全性將由「藥品監測暨風險評估委員會」(Pharmacovigilance Risk Assessment Committee, PRAC)進行評估,日後將考慮是否將審查範圍擴大到「類升糖素胜肽-1受體促效劑」(GLP-1 receptor agonists)的其他藥物。諾和諾德對此回應,患者安全是重中之重,非常重視所有不良事件的報告。GLP-1受體促效劑應用於治療第2型糖尿病已有超過15年的歷史,用於治療肥胖症也有8年的歷史。從大型臨床試驗項目和上市後監測收集的數據中,並無證據顯示其藥物與自殺自殘傾向存有關聯。諾和諾德強調會持續監測正在進行的臨床試驗和實際使用其產品的數據,並與當局密切合作,以確保患者安全和向醫療保健專業人員提供足夠的信息。美國的善纖達處方資料包括建議監測患者是否有憂鬱或自殺念頭,若出現症狀時應停止用藥。在成人臨床試驗發現,服用該藥物的在3,300多人中有9人報告有自殺念頭,而服用安慰劑的1,900多人中只有2人有自殺意念;至於兒科臨床試驗中,125名研究對像中有1人因善纖達自殺而死亡。處方資料稱「沒有足夠的信息來確定與善纖達的因果關係。」美國食品和藥物管理局(The Food and Drug Administration ,FDA)2017年核准Ozempic用於治療糖尿病,並於2021年核准Wegovy用於減肥。官方表示,將繼續檢視獲核准藥品後續的安全性,並規劃檢測和風險評估系統,一旦發現新的警訊,將採取相關應對措施。常見減肥藥7大副作用專家提醒,減肥藥應與健康飲食和運動並用,而且所有藥物都有潛在副作用。部分藥品的仿單已將自殺念頭列入可能的副作用,建議使用者注意自己的情緒、行為、想法、感覺是否出現改變,並盡速尋求醫療協助。噁心嘔吐頭痛腹瀉便秘腹痛疲倦健康醫療網提醒您:自殺不能解決問題,你我都是自殺防治守門人。安心專線:0800-788-995(0800-請幫幫-救救我)張老師專線:1980勇敢求救並非弱者,您的痛苦有人願意傾聽,生命線專線:1995原文出處:Weight-loss jabs investigated for suicide riskEuropean regulators probe risks of suicidal thoughts in users of popular weight-loss medications

洗刷慾望城市形象「阿姆斯特丹擬遷紅燈區」 性工作者、居民連歐盟藥管局都怒了
荷蘭阿姆斯特丹的「紅燈區」,讓性產業合法化,每年吸引大批遊客造訪,但也衍生街道嘈雜擁擠、居民反彈等等問題。最近當局正討論讓合法性工作者從這個紅燈區遷至市郊的「色情中心」,但光是選擇地點就引發各界爭議,除了居民與市長意見相左,就連歐盟轄下的歐洲藥品管理局(European Medicines Agency)都跳出來反對。阿姆斯特丹紅燈區。沿著阿姆斯特丹的運河兩側行走,可以見到打扮性感的女子站在櫥窗前,搖擺妖嬌身軀,這裡就是全球最早合法性工作的指定區,然而阿姆斯特丹的紅燈區聞名全球,卻也衍伸出不少問題,像是遊客太多和酒醉鬧事,這些問疑也讓阿姆斯特丹政府計畫把紅燈區遷到市郊,蓋一棟「色情中心」。根據英國廣播電台(BBC)和《荷蘭新聞》(DutchNews)報導,阿姆斯特丹市政府計畫建造一棟5千平方公尺、5層樓高的「色情中心」,包括2座酒吧、100間小包廂以及一個脫衣舞廳,據市長哈爾塞馬(Femke Halsema)表示,這是因為電影《紅磨坊》帶來的啟發,為了改變阿姆斯特丹的形象以及減緩觀光帶來的衝擊,「性工作必須從市區消失」,擺脫紅燈區是罪犯與受害女子聚集地的傳統形象。阿姆斯特丹市長哈爾塞馬位處風暴核心。阿姆斯特丹市政府上個月公布的其中一處興建地點,就是商務會議中心林立的「南阿姆斯特丹」,不過這項計畫一出,立刻引起附近民眾反彈,他們認為一旦色情中心進駐,遊客就會大量湧入,嚴重破壞當地的居住品質,民眾擔心原本存在舊紅燈區的犯罪、酗酒鬧事問題可能蔓延到新大樓。除此之外,這連總部位在該區的歐洲藥品管理局也發布聲明,「色情中心可能對附近街區造成負面影響」,希望阿姆斯特丹政府能重新考慮。其實更不想搬遷的就是紅燈區業者,由於規畫中的色情中心只有100個包廂,連目前紅燈區的250間一半都不到,業者控訴市府完全不考慮性工作者的生計。紅燈區搬遷計畫預計要好幾年才會通過,但市府打算在2023年底前選定地點,哈爾塞馬試圖與市民對話卻頻遭砲轟,由於她堅持這項計畫更被外界封為「妓院夫人」,位處於風暴核心的阿姆斯特丹市長要如何化解這場紛爭,看來仍要持續的看下去。紅燈區搬遷計畫預計要好幾年才會通過,但市府打算在2023年底前選定地點。(圖/翻攝自推特)

減肥新革命1/馬斯克瘦9公斤成活招牌 瘦瘦針藥廠市值飆升3260億美元「成全球第二」
特斯拉執行長馬斯克日前現身瘦了一大圈,全球網友驚訝不已,他回覆「靠著禁食與減肥藥Wegovy,30天減少9公斤」,這款「瘦瘦針」瞬間爆紅,研發藥廠丹麥諾和諾德(Novo Nordisk)股價大漲近一成,市值衝上3260億美元為全球第二大藥廠。專家預言瘦瘦針將主宰未來減重市場,其他藥廠也紛紛搶進馬斯克使用的瘦瘦針,尚未在台灣上市。「就我了解,Wegovy已經拿到台灣減重的適應症執照,但可能是全球缺藥、或是一些程序還沒走完,所以目前還沒上市,推測應該在今年底或明年初就能在台灣合法用於減肥。」中國附醫健康醫學中心副院長、台灣肥胖醫學會理事長林文元表示。Wegovy是藥廠研發的減肥針劑藥物,屬於GLP-1藥物的一種,研究顯示可減去體重的17%,由於大受歡迎,諾和諾德藥廠的成為全球市值第二大藥廠,其他藥廠也紛紛跟進搶市,GLP-1藥物(Glucagon-likepeptide-1 agonists類升糖素胜肽-1受體促效劑),與人類進食後所產生的腸胃荷爾蒙相似,這種腸胃型荷爾蒙在食物進入腸道後便會開始分泌,刺激胰島素產生,同時減少升糖素分泌來調節血糖。「GLP-1藥物本來是一種降血糖藥,在研發過程中,發現血糖下降的同時,體重也在下降,所以在國外很早就用於減重。」林文元向CTWANT記者解釋,GLP-1藥物可活化大腦下視丘的飽食中樞,又能延遲胃排空的速度,所以容易有飽足感、抑制食慾,進而達到減重效果。瘦瘦針藥物種類相當多,目前台灣大致有Liraglutide、Dulaglutide、Semaglutide3大類,其中只有Liraglutide(善纖達)取得減重的適應症執照,Dulaglutide(易週糖)、Semaglutide(胰妥讚)僅有糖尿病的適應症執照。「雖然如此,但醫師還是可以開給患者『非適應症』使用,只是需要自費,大約一支1000元左右,所以很多想減重的人紛紛搶購,才造成現在的缺藥問題,為了不損害糖尿病患的用藥權益,目前衛福部規定只有糖尿病患才能使用,不開放自費。」丹麥藥廠諾和諾德生產的瘦瘦針Wegovy引發搶購風潮,市值瞬間翻倍成長,已經成為全球第二大藥廠。翻攝(圖/翻攝自Novo Nordisk官網)台灣近期出現的瘦瘦針搶購潮,以Semaglutide成分藥物為主。「它的高劑量藥物品牌名稱為Wegovy,每周注射2.4毫克(低劑量約每周0.25毫克),目前的臨床試驗顯示68週可減重17%,是所有瘦瘦針藥物中效果最好的,善纖達減重效果只有8~9%,而易週糖則更低。」由於過去有效的減重似乎難以同時兼顧安全性,因此醫藥界對Wegovy在內的「瘦瘦針」GLP-1藥物充滿期待。根據《經濟學人》報導,GLP-1市場規模可望在2031年達到1500億美元,將與癌症藥物市場相去不遠,普及程度將堪比降血壓或降血脂藥物。Wegovy在美國、丹麥和挪威已可購買,特斯拉執行長馬斯克近來瘦身有成,他回覆網友詢問時,也透露「是靠著禁食跟Wegovy」,正因為效果顯著,Wegovy頓時成為眾人追捧的「減肥神器」,歐洲藥品管理局甚至發出警告,指Wegovy在2023年一整年都將面臨缺藥問題。正因為「瘦瘦針」需求很大,《經濟學人》認為投資人就和剛瘦下來的使用者一樣飄飄然,也讓生產Wegovy的諾和諾德藥廠市值2年翻倍至3260億美元,成為全球市值第2大的上市藥廠。

荷蘭紅燈區改「大樓化經營」遭歐盟藥管局反對 市長反嗆:性工作者永遠不會消失
荷蘭的阿姆斯特丹擁有合法紅燈區世界聞名,吸引不少觀光客到訪一探究竟,但上個月阿姆斯特丹宣布,將計畫性關閉線有紅燈區的酒吧和餐館,並禁止在紅燈區吸食大麻,將這些店家移到新商辦大樓中,成立系統性情色中心,但不只新地點附近居民反對,連歐盟的藥品管理局都站出來說話,讓阿姆斯特丹市長表示,「性工作者屬於阿姆斯特丹,永遠不會消失」。阿姆斯特丹市府公布三個地點做為新紅燈區大樓,但也引發附近居民強烈反對。(示意圖/翻攝自pixabay)據《BBC》、《衛報》報導,荷蘭的阿姆斯特丹上個月宣布,計畫將協助原本紅燈區的酒吧與餐館,移動到新規劃的紅燈區大樓經營,這樣的情色中心計畫可以容納百名性工作者,裡面有酒吧、餐廳、聲色場所等,並公布可能的三個地點。但卻造成三個地點的居民不悅,不想社區附近成為色情集中地,而歐盟的歐洲藥品管理局(European Medicines Agency,EMA)也跳出來反對,認為情色中心設在靠近藥品管理局附近,恐會給附近地區帶來負面影響。但阿姆斯特丹市長表示,哈賽瑪(Femke Halsema)受訪表示,EMA大樓與預計規劃的情色中心至少有一公里,並表示要打造一個「有格調、人人都不會羞於造訪的色情中心」,擺脫紅燈區是罪犯與受害女子聚集地的傳統形象,並表示「性工作者屬於阿姆斯特丹,永遠不會消失」。
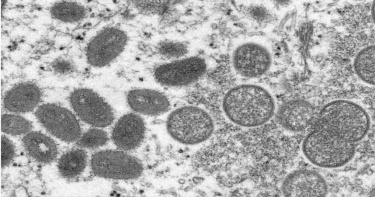
猴痘口服抗病毒藥來了!供重症及免疫低下確診個案使用
疾病管制署(以下稱疾管署)今(28)日表示,我國向國外採購之猴痘口服抗病毒藥物tecovirimat,已於昨(27)日晚間運抵臺灣,將於完成通關及驗收程序後配撥該署各區管制中心。該藥物將由醫師評估治療效益與風險,充分告知病患並獲得同意後提出申請,經審核通過後提供重症及免疫低下確診個案使用。(圖/指揮中心提供)疾管署指出,依據世界衛生組織(WHO)及歐洲疾病管制中心(ECDC)等單位之建議,大多數猴痘患者不需要特殊治療,以輸液治療與維持營養等支持性療法為主,以減輕症狀和併發症。口服抗病毒藥物tecovirimat建議使用於猴痘確診且病情嚴重之病患或免疫低下者。疾管署說明,tecovirimat經歐洲藥品管理局(EMA)核准使用於治療正痘病毒屬之天花、猴痘及牛痘;美國食品藥物管理局(FDA)核准使用於治療天花,美國疾病管制與預防中心(CDC)專案核可使用於治療因猴痘病毒感染惡化為重症或有重症危險因子之高風險患者,以降低死亡機率。我國衛生福利部食品藥物管理署已於今年7月13日同意依據藥事法第48條之2規定,核准其專案輸入。疾管署強調,猴痘已於今年6月23日公告為第二類法定傳染病,目前累計通報13例疑似病例,其中2例境外移入確診病例,感染國家為德國及美國,餘11例已排除;另自 6月30日起,將具有本土或不明感染源猴痘個案之49個國家旅遊疫情提升至「第二級:警示(Alert)」。該署提醒,國人若前往該些國家,應避免可能與不特定人士密切接觸之社交活動等高風險場域,返國入境時如出現發燒、皮膚病灶如紅疹、丘疹、水泡或膿疱等疑似症狀,應主動告知航空公司人員及機場港口檢疫人員,並儘速就醫,告知醫師旅遊史及接觸史。相關資訊可至疾管署全球資訊網( https://www.cdc.gov.tw )或撥打國內免付費防疫專線1922(或0800-001922)洽詢。

台灣做到了!全球第一個腦部基因藥物 歐盟首度核准使用
臺大醫院團隊自2007年開始發展罕見疾病芳香族L-胺基酸脫羧基酶(AADC)缺乏症之基因治療,並技轉給美國PTC Therapeutics藥廠。日前歐洲藥品管理局 同意授予這項基因治療藥物 Upstaza (eladocagene exuparvovec)的上市許可。這項藥物由研發到臨床試驗,都由臺大醫院主導,並在台灣進行,可以說是台灣新藥發展上的一項重要突破。截至目前為止,全世界尚無其他批准的AADC缺乏症治療方式。這是歐盟核准的第一個腦部基因治療藥物;目前歐美核准的基因治療藥物也不過大約十個。 AADC缺乏症是一種遺傳性罕見疾病,通常在嬰兒早期出現症狀,導致嚴重的發展遲緩、動眼危象、低張力及四肢運動異常、自律神經系統失調、睡眠問題、及情緒障礙等。此疾病可能在兒童時期即因併發症導致死亡。它是由於 AADC基因發生變異所引起,該酵素缺乏將導致多巴胺及血清素的缺乏,而這些物質對大腦和神經系統之正常功能至關重要。根據臺大醫院新生兒篩檢統計,在臺灣約每30,000人中有 1 名個案。此基因治療先是於2010年由臺大醫院基因醫學部提出「罕見疾病芳香族L-胺基酸脫羧基酶缺乏症(AADC)治療計畫」,並陸續獲得AADC缺乏症病友會、罕見疾病基金會、長榮集團張榮發總裁、及生技醫藥國家型科技計畫(NRPB)的支持贊助,爾後於2015年和美國Agilis Biotherapeutics簽署產學合作技術轉移計畫完成技轉;該公司於2018年被PTC Therapeutics併購。 此技術是利用病毒載體將帶有功能之AADC基因,透過外科手術及立體定位的方式,注射到人體腦部基底核之核殼位置。這是全球第一個成功的腦部基因療法,我們用該技術在2010年完成全世界第一例的治療後,至今成功進行基因療法共30例個案。患者經過治療後症狀減輕,而且運動功能都有明顯的改善。我們也已經將此項治療成果發表於《Science Translational Medicine》、《The Lancet Child & Adolescent Health》和《Molecular Medicine》等期刊。這項治療成就不只造福台灣及全世界的AADC缺乏症患者,對台灣的生醫製藥產業來說,也是一個重要的里程碑。台灣不僅有能力研發先進的基因治療技術,也擁有嚴謹完善的臨床試驗場域,其成果不僅獲得歐美先進國家的認可,也讓台灣的病友能夠有機會在各項新技術與新藥物臨床試驗期間,及早帶來的治癒的新契機與新希望。
接種Novavax恐出現嚴重過敏 美警告過敏者切勿施打
歐盟藥品審查機構「歐洲藥品管理局(European Medicines Agency,簡稱EMA)」14日證實,施打Novavax疫苗可能出現「嚴重過敏」副作用,該疫苗於13日獲得美國監管機構的授權,其在美國的產品標籤警告,對疫苗成分過敏者,不要施打此疫苗。美國監管機構警告,對疫苗成分過敏者,不要施打Novavax疫苗。(示意圖/unsplash)路透社報導,歐洲藥品管理局(EMA)將更新疫苗的產品訊息,增加皮膚異常及減少知覺的副作用。根據歐洲疾病預防和控制中心(European Centre for Disease Prevention and Control,簡稱ECDC)的數據,自去年12月推出Novavax以來,迄今為止,歐洲僅使用了250,000劑Novavax疫苗(歐洲名為「Nuvaxovid」)。歐盟公布,施打Novavax新冠疫苗有嚴重過敏副作用後,Novavax與其他新冠疫苗製造商的股價,在早盤交易中,下跌20.3%至55.72美元(約新台幣1,668元),其中Novavax的股票波動較大。
變種魔王Omicron來勢洶洶 俄科學家誇自家疫苗最有效
南非出現新冠病毒最新變種「Omicron」,目前全球已有10個國家出現病例,由於其兇猛程度恐怕更勝過往的變種病毒,令不少人憂心忡忡,不過有俄國科學家出面指出,儘管現有的疫苗碰上Omicron後,效力都會下降,但俄羅斯所研發的「史普尼克-V(Sputnik V)」能提供最廣的中和抗體,理論上會比其他疫苗更有效。綜合外媒報導,研發出史普尼克-V疫苗的加馬列亞研究中心(Gamaleya Institute)所長金斯伯格(Alexander Gintsburg)近日指出,史普尼克-V疫苗能夠提供最廣的中和抗體,所以能夠比現有之新冠疫苗提供更好的保護力;不過他也補充,由於目前研究中心尚未收到Omicron的樣本,因此現在尚不需對史普尼克-V疫苗進行升級,中心一旦收到樣本會立刻進行效果測試。根據「俄羅斯通訊社(Sputnik)」報導,美國喬治梅森大學系統生物學家芭拉諾瓦(Ancha Baranova)也同意上述說法,她表示「史普尼克-V疫苗的表現可能會好一些,達到幾個百分點,腺病毒載體疫苗通常會比mRNA疫苗引發更廣泛的免疫反應,但差異可能非常小」。根據了解,俄羅斯衛生部8月也曾宣稱史普尼克-V疫苗是對抗Delta變種的最佳疫苗,對Delta有83%的效力,不過該疫苗遲遲未獲得世界衛生組織(WHO)認證,也尚未獲得歐洲藥品管理局批准。
AZ疫苗新副作用 歐盟增列罕見神經病變「格林巴利症候群」
歐洲藥品管理局(EMA)8日增列一種極為罕見的神經損傷疾病「格林巴利症候群」(Guillain-Barre Syndrome,GBS),作為接種AZ疫苗可能的副作用。根據《路透社》報導,歐洲藥品管理局表示,截止至7月31日,在全球接種的5.92億劑疫苗中,通報了833例「格林巴利症候群」病例,顯示接種AZ疫苗與「格林巴利症候群」之間的因果關係為「至少是合理的可能性」。歐洲藥品管理局將此副作用歸類為,非常罕見。歐洲藥品管理局表示,「格林巴利症候群」是接種AZ疫苗後,出現的副作用中,頻率最低的。歐洲藥品管理局強調,注射疫苗的好處超過可能帶來的風險。而在這之前,美國食品暨藥物管理局(FDA)就曾對嬌生集團(J&J)生產的疫苗,加註警語,稱其疫苗副作用可能出現「格林巴利症候群」的副作用。至於何謂「格林巴利症候群」,專家諮詢小組召集人張上淳曾在記者會中說明,主要是免疫反應造成的周邊神經傷害引起的,症狀為肌肉無力、呼吸衰竭等。

AZ疫苗後遺症再+1! 加拿大11日出現首例個案「建議1種人別接種」
AZ疫苗在世界各國引發不少血栓案例,先前就被不少國家如德國、法國、義大利等宣布停用,後來在歐盟與英國政府為疫苗安全掛保證後,才重新恢復施打。不過加拿大衛生部29日警告,有毛細血管滲漏症候群(CLS)病史的患者,不要接種AZ疫苗。根據「澳聯社」(AAP)報導,加拿大衛生部正在更新阿斯特捷利康(AstraZeneca)COVID-19疫苗與Covishield疫苗(AZ疫苗印度版)的產品專著與標籤,增加毛細血管滲漏症候群(CLS)作為潛在副作用,並警告有CLS病史的患者不要施打AZ疫苗。毛細血管滲漏症候群(CLS)是一種罕見的、可逆性毛細血管病變,血漿迅速從血管滲透到組織間,導致患者出現全身水腫、低蛋白血症、血壓降低情況,嚴重時還會發生多重器官衰竭,常見病發原因包括嚴重創傷、膿毒症、毒蛇咬傷、燒傷等。事實上,歐洲藥品管理局(EMA)在4月份就將CLS列為AZ疫苗潛在安全問題,不過一直到本月11日,才正式增列CLS為AZ疫苗可能副作用之一;加拿大衛生部則表示,直到6月11日,該國才出現第一起CLS病例。英國藥物及保健產品管理局(MHRA)先前也表示,英國正在考慮為有CLS病史的人提供預防建議。

高端疫苗宣布解盲成功!陳培哲:預期中的結果
爭議不斷的高端疫苗宣布解盲成功,並加速第三期臨床實驗,中研院院士陳培哲表示,此為既定的劇本,毫無意外,此為預期中的結果。陳培哲近來提出專業發言,指出三家本土生技公司的疫苗專長都是滅活疫苗,投入新冠疫苗技術卻是蛋白質次單位疫苗,研發與技術都大有問題,甚至更坦言離開食藥署疫苗審查委員,最大的困難點即來自於總統蔡英文,引起一連串政治追殺。不只陳培哲,包含前疾管局局長蘇益仁也認為國產疫苗有問題,即便專家多次拋出相關說法,但有媒體民調顯示,仍有逾5成民眾願意施打國產疫苗。對此,陳培哲則說,如此即在於沒有其他的選擇,這也是很無奈的事情。陳培哲表示,既然高端疫苗已經解盲,建議速向美國食藥署(FDA)、歐洲藥品管理局(EMA)申請緊急使用授權(EUA),如此才能與國際同步。
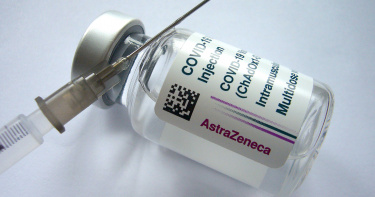
國內採購限制多?歐盟「疫苗護照 」 開放多種疫苗施打核可
在新冠疫情衝擊下,各國政府無不使出洪荒之力,動員企業財團或是民間組織,購買疫苗或者開發疫苗,希望疫苗數量和種類越多越好,讓人民有足夠疫苗可以施打,或是更好的疫苗可以選擇,但台灣不只疫苗不足,還不能選擇打什麼疫苗,更不能自由進口疫苗,顧慮似乎很多。歐盟早就研議對完成新冠肺炎疫苗接種的國際旅客開放邊境。(圖/達志/美聯社)根據《CNBC》的報導,歐盟早就研議對完成新冠肺炎疫苗接種的國際旅客開放邊境,意味著美國與其他非歐洲旅客2021年夏季便能夠前往歐洲旅遊。據歐盟27國的大使19日時透露,歐盟早就做出該項決定,歐盟各國領袖在25日的峰會上批准這項旨在便利旅遊、振興歐洲觀光業的疫苗護照計畫,接下來歐洲議會可望在6月7日到10日間的會議通過,預定7月1日起實施。歐盟對完成疫苗接種的旅客開放邊境。(圖/翻攝自CNBC網頁)根據歐盟執委會主席馮德雷恩25日在會後指出,疫苗護照系統的基礎設施會在6月1日就緒,會員國能在該月中旬起連上系統。報導指出,旅客若是完成接種世界衛生組織(WHO)或歐洲藥品管理局(EMA)批准的疫苗,目前僅包含輝瑞(Pfizer)、莫德納(Moderna)、阿斯特捷利康(AstraZeneca)和嬌生(J&J)目前包含輝瑞、莫德納、阿斯特捷利康和嬌生的疫苗獲歐盟認可。(圖/翻攝自CNBC網頁)完成疫苗接種、能證明病毒核酸檢測(PCR)陰性,或者感染但已經康復的人,都可獲發歐盟疫苗護照,舉例來說,接種疫苗者將在第14天發出,這個時間點被認為患者不再具有傳染力,護照效力維持到第180天,此外,新加坡、以色列等也推出類似概念的證明。不過反觀歐盟對多家疫苗製造商批准,指揮中心對於各界捐贈疫苗,小心再小心,疫苗進口形勢不明,雖說指揮中表示對國內疫苗高端還有聯亞,採購總數至少達到2千萬劑,只不過國產疫苗什麼時候能打到?高端和聯亞的疫苗預計二期實驗結束就拿到緊急授權,相對國外疫苗通常通過三期臨床試驗才會放行,標準好像不太一樣。

王之道/疫苗民粹拖垮台灣
先前因新冠肺炎本土病例不多,民眾接種疫苗意願不高,但近來社區群聚感染大爆發,國人才驚覺疫苗嚴重短缺的問題。國產疫苗雖尚未完成人體試驗,總統蔡英文就宣布七月底開始施打,但對於引進陸製疫苗的呼籲,政府卻扣上紅帽子,認為是幫大陸打「認知戰」,冷回大陸國台辦「假好心」。即使台灣在封閉國境阻斷傳染源上取得成功,但遲遲未能對國人進行疫苗注射,完成群體免疫,現在卻急於操弄「疫苗民粹」,可說是置人民健康與性命於不顧。民眾先前接種疫苗意願不高,與台灣疫情和緩、國際相繼傳出疫苗副作用有關。台灣唯一能使用的疫苗是英國和瑞典跨國公司阿斯特捷利康(AstraZeneca) 所研製的AZ疫苗。但三月起國際間陸續出現該疫苗恐導致血栓的報導,讓人們對其信心大幅下降,十多個國家宣布暫停使用。不過,世界衛生組織(WHO)及歐洲藥品管理局認為,沒有證據說AZ疫苗不安全,其與血栓沒有直接關聯。英國媒體也為AZ疫苗叫屈,認為AZ疫苗在一些國家被叫停,實則與「疫苗政治」有關。由於疫苗投資風險極高、金額龐大,但收穫的政治、經濟利益極高,牽涉國家榮譽與國際權力鬥爭。許多富國在研發初期投入相當大的經費,為了保證回收成本,不惜煽動民粹來保障國產疫苗。例如美國食藥署至今只批准三種疫苗在美國使用,卻不包含在美國生產的AZ疫苗。在AZ疫苗具嚴重副作用的相關報導傳出之前,台灣就已經有緩打疫苗的民粹言論。年初時,許多國家陸續取得疫苗,再加上陸製疫苗研發成功,對遲遲無法取得疫苗的蔡政府產生極大壓力。執政黨民代與側翼網軍、名嘴開始宣傳「拒當白老鼠」、「台灣有等的本錢」、「打疫苗還是會染病」、「你先打,我OK」,延誤接種疫苗速度。根據中央流行疫情指揮中心指揮官陳時中的說法,疫苗覆蓋率至少要達到六成,才會形成集體免疫力,那麼台灣至少需要二千萬劑疫苗。然而,台灣目前施打率不及一%,就算加上近日進口的四十萬劑AZ疫苗,以及預計年中交貨的五百萬劑莫德納疫苗,還是有很大的缺口。蔡英文承諾七月底可施打國產疫苗,或許意在安撫民心,但即使國產疫苗真能上路,其注射證明能否在國外暢行無阻,仍是一大問題。當主要國家恢復往來時,台灣人卻出不去,外國人也進不來,對經貿、旅遊及國家形象傷害甚大。疫苗當然應該自主,但人命關天,實在不宜大行疫苗民粹主義,否則非但解決不了問題,更有可能危及國人健康,甚至延誤疫情的控制。就讓防疫多一點科學,少一點政治吧。

有疫苗打是防疫關鍵 賴正鎰建議由民間採用大陸國藥疫苗
面對國內確診新冠肺炎人數持續增加,造成前線醫護醫療能量緊繃,全國人民更因為等不到疫苗、全國持續三級警戒,現有阿斯特捷利康AZ緩不濟急,下半年的民生經濟表現恐怕問題很大,全國商總主席賴正鎰呼籲,政府應加速採購疫苗,3個月內達到施打1千萬劑確保證國人安全;甚至建議政府應拋棄政治成見,接受使用大陸疫苗,可由民間或地方政府出面採購後捐給政府,再提供給國人使用。賴正鎰面對疫情轉趨嚴峻憂心表示,台灣去年的前期防疫做得很好,但今年出現漏洞,爆發連環疫情,而疫情傳播速度之快,天都增加3、4百人確診,全國上下大家壓力都很大。每天電話被打爆的賴正鎰表示,許多商總會員告訴他,三級警戒疫情實施後,超過五成的店家場所都關閉,無法營業,生存不下去,所有飯店餐廳,旅遊業等服務業只好歇業,疫情若不控制,恐怕7月時就倒光了,建請政府要加快採購疫苗速度,並繼續提供產業紓困補助。賴正鎰表示,世界衛生組織(WHO)已在5月初對大陸國藥疫苗授權緊急使用,若政府為了百姓安全,且大陸也願意提供疫苗一起防疫,建議政府應拋棄政治成見,接受使用大陸疫苗。如果政府不方便出面採購,是否趕緊研議開放變通方式,讓企業或是縣市政府有自行談判及採購的權力,相信民間企業很樂意採購後捐給政府,再提供給國人使用。大陸國藥疫苗在5月7日初獲得WHO授權使用,並加入COVAX配發平台,而歐洲藥品管理局也針對科興疫苗正在快速審查中,最近就會公佈結果。(圖/國藥集團)賴正鎰引用專家數據說明,要達成群體免疫目標,估計至少要全體人口70%以上完成接種第一劑疫苗,以台灣2,300萬人口的七成計算,至少要有1,600萬人注射,若每人要注射2劑,那就要3,200萬劑,但台灣現在才拿到70萬劑,國產疫苗也還在研發階段,要等到七月以後,緩不濟急。台灣第一批31萬劑AZ疫苗,到今天為止,才剛完成30萬人施打,施打率僅1.2%,而第2批的41萬劑AZ疫苗,第2批還要5月28日才要開打,至於後續疫苗還在談判,根本就是遙遙無期。根據大陸統計至5月23日,施打疫苗已達到5.1億劑疫苗,每日施打疫苗數量更高達1,700萬劑,而且正在加快速度,力拚在八月達到注射接種率72.9%,才能達到較理想的80%疫苗保護率,群體免疫的目標。賴正鎰說,在大陸數十萬台商,多數台商朋友早就在打完大陸疫苗,結果都很好,沒有問題,另外,像是鄉林在大陸的台幹及涵碧樓員工,累計上千人都完成疫苗施打,沒有什麼副作用、很健康。
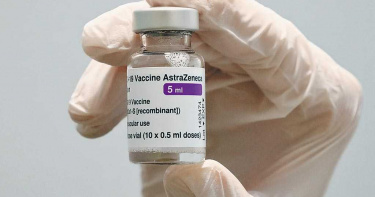
血栓列「極罕見」副作用 AZ疫苗開放旅遊門診!釋出1萬劑自費接種
歐洲藥品管理局(EMA)最新聲明,將血栓列為AZ疫苗接種的「極罕見」副作用後,歐洲已有數國先後暫停或限制特定年齡層打,台灣中央流行疫情指揮中心昨天定調,台灣不會停打,也不會限制年齡,下周一照原訂計畫擴大到第三類順位施打後,還將進一步宣布釋出最多1萬劑疫苗開放自費接種,讓有商務工作、留學等出國需求者,最晚四月底前一定打得到。衛福部傳染病防治諮詢會預防接種組ACIP召集人李秉穎說,從歐盟資料得知,在對照研究看起來,血栓跟打疫苗都沒有相關性;專家評估疫苗帶來的預防效應仍大於不良的反應,利大於弊,所以EMA仍建議繼續接種,國內也將繼續接種。但會進一步提醒、告知接種者有相關潛在風險。根據指揮中心最新統計,前日新增1395人接種AZ疫苗,累績人數終於破2萬人,並新增9件不良反應事件,其中8件為非嚴重事件,1件為其他疑似嚴重事件,發言人莊人祥表示,這名其他疑似嚴重事件,是目前國內首例出現瘀斑個案,為20多歲男性,接種後第5天,肢體多處出現瘀斑到急診就醫,現已經恢復良好,經量測血液中凝血指標都屬正常,未證實是血栓問題。受到國際血栓事件影響,AZ疫苗打氣仍未見回升,莊人祥表示,還需再觀察,4月12日擴大到第二順位中央及地方政府防疫人員,以及第三順位機組員、防疫計程車等高風險接觸者接種後,排在第四順位的自費對象,包含商務人士、有出國工作、留學或就醫等人道因素需求者,也將釋出5千到1萬劑疫苗提供接種,最快下周決定釋出,最慢四月底前一定可以打。台北市長柯文哲允諾「下禮拜我會乖乖去打疫苗」,至於是否呼籲蔡總統一起打疫苗,柯文哲說,除非蔡英文永遠躲在總統府,不然還是要打。