美國食品暨藥...
」 FDA 疫苗 美國 新冠肺炎 輝瑞
廣達攜國軍做電子傷票系統 林百里:智慧醫療不容易
廣達(2382)、國防部軍醫局與國防醫學院17日舉辦產官學合作簽約儀式,宣布共同研發「電子傷票系統」,廣達董事長林百里表示,有許多智慧醫療專案進行中,但打造醫療應用並不容易,「醫生是最聰明的人,我們要滿足最聰明的人不容易。」電子傷票系統,是以科技導入戰場醫療現場,將傷患資訊即時數位化處理,這次的合作是融合AI判讀、無線通訊、生命徵象擷取與即時資訊傳輸功能,透過加密通訊即時傳送至後方指揮與醫療單位。這是由廣達提供核心架構設計與智慧醫療平台支援,搭載自主開發的QOCA遠距照護技術,可用在行動載具、部屬於前線救護設施。國防部軍醫局則提供實戰需求驗證與軍種推廣,國防醫學院衛訓中心則作為學研執行主體,導入多年累積的戰傷評估、戰場醫療流程與醫療資訊系統研究成果。林百里會後接受媒體採訪時表示,廣達布局智慧醫療有3大方向,包括人工智慧(AI)醫療進行診斷、遠距醫療、個人照護醫療等都在進行中,與國防醫學院也合作好幾次,成果都非常好。廣達近期也計畫,要向美國食品暨藥物管理局(FDA)申請醫療器材等相關證照,但必須一步一步來,林百里表示,打造智慧醫療應用並不容易,有關醫生的要求必須好好了解,再進行IT研究。日前在股東會時,也有小股東質疑在智慧醫療項目不容易賺錢,當時林百里提到,要真正「解決醫師需要的問題」才有價值,所以門檻和投入成本很高,且台灣智慧醫療市場規模較小,海外市場則要面對臨床試驗與認證申請等漫長過程,每個新產品的開發都需「十年磨一劍」的精神,「這是最大的挑戰」,但也是機會。

白吐司被踢出「健康食品」 營養師揭關鍵:對心血管健康不利
白吐司是不少台灣民眾早餐的常見選擇,甚至不少民眾認為腸胃炎就該吃白吐司養病,但近日美國食品暨藥物管理局(FDA)重新定義食物「健康」標準,將白吐司、早餐穀片與優格排除在健康食物清單外,改將堅果、部分種子類食材、雞蛋、鮭魚及橄欖油列入清單。對此,營養師吳悦慈表示,這並不令人意外。營養師吳悦慈指出,白吐司主要由精緻澱粉製成,麩皮與胚芽在加工過程中被去除,導致纖維、維生素及礦物質含量大幅下降。此外,市售白吐司還常含有大量添加糖、奶油及加工油脂,這些成分不僅會導致血糖快速升高,也對心血管健康不利。吳悦慈強調,高精緻度的食物進入體內後,容易迅速轉化為葡萄糖,造成血糖快速波動,隨後帶來飢餓感與能量波動,對健康不利。然而對於習慣食用白吐司且一時難以戒除的人,吳悦慈建議可從以下五個方法逐步改善,像是先將白吐司與全麥吐司混合食用。例如早餐可用一片白吐司搭配一片全麥吐司,幫助味蕾逐漸適應全穀類的風味與口感,並逐步增加全麥吐司的比例。吳悦慈說明,白吐司單獨食用容易引起血糖波動,因此建議搭配高纖維、高蛋白質的食物,例如水煮蛋、酪梨泥、生菜或烤雞胸肉。這些搭配不僅能增加飽足感,還能減少單純澱粉對血糖的影響。吳悦慈建議,每餐食用白吐司的份量應限制在一片或半片,並搭配沙拉、湯品或水果等多元食材,減少白吐司在總熱量中的占比,避免營養攝取失衡。此外,吳悦慈也提到,可嘗試將白吐司製作成烤吐司捲、夾餡三明治,或搭配高纖維抹醬(如花生醬、杏仁醬),讓餐點更加多樣化,同時提升營養密度。而對全麥吐司不習慣的人,可以嘗試雜糧麵包、裸麥麵包,甚至以地瓜、燕麥等更天然的碳水化合物來源取代,逐漸減少對白吐司的依賴。

美麥當勞「四盎司牛肉堡」大腸桿菌中毒奪命!13州75人感染「1人死亡」 罪魁禍首找到了
美國連鎖速食巨擘麥當勞(McDonald's)的四盎司牛肉堡爆發民眾食用後感染大腸桿菌的疫情,據美國食品暨藥物管理局(FDA)和疾病管制暨預防中心(CDC)說法,這波疫情造成的住院人數攀升至75人,大部分病例集中在美國西部地區,其中科羅拉多州一名長者死亡,包括一名兒童腎臟出現嚴重併發症,罪魁禍首可能是供應鏈中的切片洋蔥,目前包括其他速食業者塔可鐘(Taco Bell)、必勝客(Pizza Hut)、肯德基(KFC)跟漢堡王(Burger King),也緊急下架洋蔥。連鎖速食店麥當勞的四盎司牛肉堡(Quarter Pounder)可能與大腸桿菌疫情爆發有關。(圖/達志/美聯社)根據多家美媒報導,CDC在22日發布食品安全警報指出,連鎖速食店麥當勞的四盎司牛肉堡(Quarter Pounder)可能與大腸桿菌疫情爆發有關,造成75人中毒,這波疫情已導致22人住院治療,並造成科羅拉多州一名年長患者死亡。值得關注的是,有一名孩童和一名成年人被診斷出溶血性尿毒症候群,這是一種造成腎臟血管受損的嚴重疾病。CDC指出,這些病例由上月27日至本月11日期間發生,多達27例來自科羅拉多州,其餘包括內布拉斯加州、堪薩斯州和猶他州等13州,大腸桿菌是種常見於人類和溫血動物腸道內的細菌。大多數大腸桿菌菌株都不會造成傷害,不過像是如產志賀毒素大腸桿菌,則會產生強烈毒素,恐導致嚴重的食物傳播疾病。調查人員已經將調查重點聚焦在洋蔥絲和牛肉餡上,包括負責供應洋蔥絲的廠商加州薩利納斯(Salinas)的泰勒農場(Taylor Farms)已宣布自主回收黃洋蔥。(圖/達志/美聯社)雖然目前尚未查明導致疫情爆發的具體食材,不過調查人員已經將調查重點聚焦在洋蔥絲和牛肉餡上,包括負責供應洋蔥絲的廠商加州薩利納斯(Salinas)的泰勒農場(Taylor Farms)已宣布自主回收黃洋蔥。有採購相關洋蔥食材業者的塔可鐘(Taco Bell)、必勝客(Pizza Hut)、肯德基(KFC)跟漢堡王(Burger King)等速食餐廳,也紛紛緊急下架洋蔥。(圖/達志/美聯社)對此,美國麥當勞也發聲明表示,受影響的部分地區已停售「四盎司牛肉堡」,強調極度重視食品安全。另外,有採購相關洋蔥食材業者的塔可鐘(Taco Bell)、必勝客(Pizza Hut)、肯德基(KFC)跟漢堡王(Burger King)等速食餐廳,也紛紛緊急下架洋蔥。有採購相關洋蔥食材業者的塔可鐘(Taco Bell)、必勝客(Pizza Hut)、肯德基(KFC)跟漢堡王(Burger King)等速食餐廳,也紛紛緊急下架洋蔥。(圖/達志/美聯社)另據《中時》稍早引述台灣麥當勞回應,「台灣麥當勞四盎司牛肉堡所使用的切絲洋蔥,原料由紐西蘭進口,牛肉餅原料則來自巴拉圭及紐澳,來源皆與美國不同;同時,根據供應商自主檢驗報告,確認原料均符合相關標準,敬請顧客安心食用」。調查人員已經將調查重點聚焦在洋蔥絲和牛肉餡上,包括負責供應洋蔥絲的廠商加州薩利納斯(Salinas)的泰勒農場(Taylor Farms)已宣布自主回收黃洋蔥。(圖/翻攝自X)

首位患者大腦植晶片! 馬斯克喜曝:可用意念「控制滑鼠」
社群X(前身Twitter)創辦人馬斯克(Elon Musk)旗下大腦晶片新創公司「Neuralink」早在2024年1月時已替一名患者植入大腦晶片。而馬斯克在19日時在社群上表示,患者已經康復且狀況良好,現在甚至可以用意念控制滑鼠。綜合外媒報導,馬斯克19日在X上發文表示,今年1月植入大腦晶片的患者目前已康復,且健康狀況良好、狀態正常,且僅透過意念就可以輕鬆控制螢幕中的滑鼠。據悉,目前他的團隊仍在思考如何讓患者多按幾次滑鼠按鍵。不過至今馬斯克尚未提出晶片植入大腦的相關手術成果,因此目前無法得知晶片植入代表多大的科學進步,且Neuralink也並無做出任何回應。去年9月,Neuralink就曾表示已獲得美國食品暨藥物管理局(FDA)的批准,在2024年開始計畫招募人員參加試驗,並利用大腦晶片技術為那些四肢癱瘓或麻痺的人僅用意念就可以輕鬆控制電腦或手機。第一位患者的身份尚未公佈,儘管 Neuralink 去年表示正在尋找因頸脊髓損傷或肌萎縮側索硬化症(ALS)而導致四肢癱瘓的患者進行試驗。另外,馬斯克對Neuralink持續抱有遠見,稱將促進晶片設備快速利用手術植入技術,以治療肥胖、自閉症、憂鬱症和思覺失調等疾病。

250款感冒藥「治鼻塞成分」無效 美FDA專家認定:形同安慰劑
每到感冒及流感季節,美國有數百萬人就會購買添加該成分的成藥,有些人已經服用幾十年,沒想到美國食品暨藥物管理局(FDA)專家近日指出,許多感冒成藥中添加的常見的鼻塞藥劑「去氧腎上腺素」(Phenylephrine)其實並沒有效果,形同安慰劑,民眾若繼續服用,只是在拖延接受有效治療的時間。FDA正考慮是否下架該成分。《紐約郵報》報導,FDA顧問小組11及12日審查幾項現有研究後進行投票,結論是去氧腎上腺素口服藥物無效且不比安慰劑好,根據該小組主席、俄亥俄州立大學藥學系副教授科伊爾(Maria Coyle)表示,「我認為在非處方藥領域,顯然有更好的選擇可以幫助患者」,「研究並不支持這是一種有效的藥物」。佛羅里達大學藥劑師亨德爾斯(Leslie Hendeles)也指出,「如果你有鼻塞,吃了這種藥還是會鼻塞」,他早在2007年就向FDA要求下架這類藥劑。在美國,有數百萬人每到感冒及流感季節就會購買添加該成分的成藥,有些已經服用幾十年,報告顯示,去年至少有250種產品含有這種去鼻塞成分,銷售額將近18億美元,約新台幣575.48億元。報導指出,顧問小組投票結果可能促使FDA決定完全禁止該成分,將導致數百種成藥下架,若FDA決定下架這些藥品,隨著藥廠重新製造、替換成分,恐衝擊民眾無法在市面上買到包括泰諾(Tylenol)、Mucinex、Benadryl等知名廠牌的感冒、流感藥物;報導也指出,若藥廠沒有足夠時間替換產品,FDA的決定可能會嚴重擾亂感冒藥市場。一般來說,FDA通常會遵循顧問小組的建議,但也並非一定,且可能需要數月時間才能做出最終決定,另外,專家也呼籲,消費者無須恐慌,也無須丟掉手邊的藥品,因為儘管該成分被認定無法緩解鼻塞,但對人體無害,且這些藥品其他成分確實可緩解感冒症狀。美FDA專家認定:常見「治鼻塞成分」無效 。(圖/達志/美聯社)
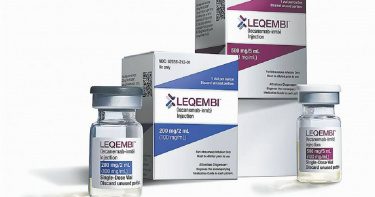
美國准了!首款阿茲海默症藥物納醫保 食藥署:台灣最快2025年上市
美國食品暨藥物管理局(FDA)6日全面批准阿茲海默症(Alzheimer,老人失智症)新藥「Leqembi」,這是首款已證明具有減緩病情發展療效的藥物,有助於阿茲海默症擺脫「不治之症」的印象。因該藥獲批准,美國的公營長者健保「聯邦醫療保險」(Medicare)也把Leqembi選定為保險適用對象。由於患者負擔減輕,估計該藥將普及化。食藥署表示,藥廠已於6月中旬申請銜接性試驗評估,如採加速審查,有望在2025年在台核准上市。Leqembi由日本衛采製藥(Eisai)與美國藥廠百健(Biogen)合作開發。今年1月,該藥獲得相當於臨時許可的「加速批准」,開始在美國國內銷售。Leqembi是一種單株抗體(mAb)藥物,為了去除阿茲海默症患者腦部蓄積的「β-澱粉樣蛋白」而設計,它在臨床試驗中顯示出可使認知功能惡化速度減緩27%的療效。美國約有650萬人罹患阿茲海默症。Leqembi的治療對象是處於發病前期的輕度認知障害(MCI)及早期患者。每2周靜脈注射一次,藥費每年約2萬6500美元(約新台幣82.9萬元),Medicare的被保險人仍需自行負擔20%、約數千美元的醫療費用,其餘費用則由保險支應。Leqembi在臨床試驗中,有1至2成參與者被發現有輕微的腦溢血和腦水腫,尤其是帶有「APOE4」基因的人風險會增加,因此應該在開始用藥前做檢查;此外,使用活血藥物的人也容易發生腦溢血,需加以注意。新光醫院失智症中心主任劉子洋表示,Leqembi適用於早期輕度阿茲海默患者,美國FDA曾核准另一款藥物Aducanumab,但副作用較多,當時引發不少爭議;台北榮民總醫院失智治療及研究中心主任王培寧指出,通常新藥在美國核准後,約2到3年後有機會在台上市,快則1年半,預估最快2025年引進台灣。食藥署副署長陳惠芳回應,一般藥品審查天數為360天,若為國人生命及健康維護有迫切需求,審查天數可縮減為240天;由於國內尚無阿茲海默症藥物,藥廠可提出加速審查申請,如經審查符合條件且資料齊全,將有望在2025年在台核准。

好市多爆A肝莓果早吃進肚 政府下架慢綠委也不爽
好市多熱門商品「科克蘭冷凍三種綜合莓」遭驗出A肝病毒,消費者及立委王鴻薇都批評食藥署反應太慢。食藥署副署長林金富則在立院表示,食藥署在3月19日收到國際警訊後,發現同批號冷凍「草莓」並未輸入台灣,但食藥署加強檢驗,於邊境發現一批智利綜合莓果有病毒,食藥署還同時針對各國輸入莓果加強查驗,一刻都沒有怠慢。至於開罰的問題,他表示,已責成地方衛生署進行調查程序,將給業者陳述意見,目前蒐證已差不多,食安法可開罰6萬到2億,會按照資本額跟違規情形加重處分。王鴻薇昨日在臉書引用消基會資料指出,美國今年3月就已針對相關冷凍莓果發出通報,好市多早該依照食品安全衛生管理法的相關規定進行處理,但最後卻把有問題的產品賣到消費者手上,必須負起相關責任,依法受罰「賠償受害民眾」。食藥署身為主管機關,未依照食品安全衛生管理法和消費者保護法相關法條依法發出消費警訊,也未對企業進行行政查核或封存,導致消費者吃進有風險的產品,相關單位應調查是否有失職疑慮。立委鍾佳濱、陳靜敏、陳培瑜今日也開記者會,批評食藥署動作慢。鍾佳濱說,食藥署拖這麼久在忙什麼?食藥署不是3月就已收到警訊,還說當時抽查沒問題,直到高雄市衛生局抽查才發現問題。迄今為止,也只有高市衛生局根據傳染病防治法裁罰業者,但其實食安法規定,可按次裁罰、從6萬到2億,尤其進口A肝莓有1萬7千公斤,但下架的只有幾百公斤,這麼大的數量流入市面、難道食藥署只坐視業者開放退貨,完全不用開罰嗎?立委陳靜敏批評,食品衛生這麼多年都管不好,A肝雖可能會自行痊癒,但對於年長或者是已經有B肝、C肝的個案來說,造成後續猛爆性肝炎仍然有千分之三的致死率。若食藥署該作為而不作為,會引起民心恐慌,她呼籲,若已購買或食用的問題莓也不用太慌張,但要為自身安全把關,A肝潛伏期就是60天,從食用起60天為限,若發現發燒、全身倦怠、腹痛甚至黃疸,就可能感染,可到感染腸胃科、感染科、家醫科就醫,讓醫生比較好判斷是否罹患A肝,也暫勿生食進口莓類。美國西岸華盛頓州早在今年3月13日陸續傳出5起A型肝炎病例,其中2人住院,5個病例都曾吃過冷凍有機草莓,美國衛生當局研判可能存有關聯,可疑商品在全美其他18州以多種品牌上市,通路包括好市多(Costco)、喬氏(Trader Joe’s)等多家大型零售商,當時國內新聞曾報導,進口商立即全面下架回收,強調進口草莓都未檢出病毒,但美國FDA在事發後曾警告大眾,家中若還有相關品牌草莓,切勿食用。食藥署3月19日曾發布新聞稿指出,美國疾病管制暨預防中心(CDC)評估華盛頓州5起A肝案例疑似與市售冷凍草莓有關,美國食品暨藥物管理局(FDA)已發布警訊下架回收,出問題的草莓與台灣進口批號並不同。但4月28日卻傳出,高雄市衛生局在4月11日接獲食藥署通報,指美國於今年3月通報5起A型肝炎病例,深入調查評估後「推測與市售冷凍草莓有關」,高市衛生局接獲通報後,啟動聯合稽查好市多智利進口「Kirkland Signature科克蘭冷凍三種綜合莓」產品,責令業者預防性下架,查驗、抽樣5批同類產品後,28日接獲通知,其中1批產品驗出A型肝炎病毒陽性,初步疫調結果台灣雖無民眾染疫,但仍提醒民眾注意。由於抽驗不合格產品是在2023年1月19日進口,共367.43公斤,高市衛生局也通令全數銷毀,好市多則同意消費者拿貨退錢,但有網友質疑賣場只退貨太消極、要求應提供消費者賠償。

好市多冷凍草莓疑引A肝遭美下架 「台灣有相同產品」食藥署釋疑
美國疾病管制暨預防中心(CDC)日前表示,華盛頓州有5起A肝案例疑似與市售的冷凍草莓有關,目前美國食品暨藥物管理局(FDA)已經勒令疑似有問題的產品下架回收。而目前也傳出台灣有相同品牌的產品,但食藥署則解釋「出問題的批號與台灣販售的批號不同」。根據媒體報導指出,食藥署表示,從去年1月1日至3月19日這段期間,Kirkland Signature冷凍草莓共進口19批100.57噸,產地來源的確也與發生疑慮的產品相同,均是來自於墨西哥。但是台灣所進口的規格、有效期限與FDA要求下架的批號不同。FDA也特別強調,有疑慮的產品僅運輸到美國特定州銷售。食藥署也表示,A型肝炎通常是由A型肝炎病毒所引發,主要是透過食物來傳播,絕大多數的感染者都有望完全康復。食藥署同時也呼籲民眾應常洗手、不要攝取不乾淨、沒煮熟的食物,外出旅行者可以用瓶裝水、蒸餾水來取代公共飲水,如此不僅可以預防多種疾病,也能預防A型肝炎的發生。
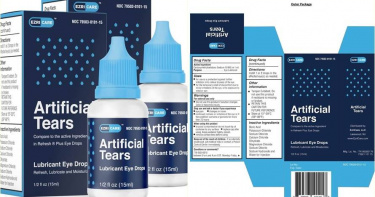
美國知名人工淚液細菌感染釀1死 食藥署回應這樣說
美國食品暨藥物管理局(FDA)近日發出公告,表示由印度藥廠Global Pharma Healthcare推出的人工淚液品牌EzriCare,發現高度抗藥性的綠膿桿菌(Pseudomonas aeruginosa)感染,已影響12州並有55名病患感染,甚至出現首起死亡案例,如今台灣食藥署也對這款人工淚液做出回應。綜合外媒報導,人工淚液品牌EzriCare發現受到細菌感染,當中發現有高度抗藥性的綠膿桿菌(Pseudomonas aeruginosa),雖然還沒有證明細菌感染跟產品有所關聯,但已在美國12州有1死55感染,FDA也以「缺乏測試和適當包裝」為由下架禁售。衛福部食藥署今(4)日也表示,經清查後發現這項產品,並沒有核准輸入台灣,會持續注意國際間警訊。而振興醫院感染科主任兼任感染管制室主任李明政表示,綠膿桿菌是「很惡毒的細菌」,這種細菌擴散快速,一旦感染必須使用特殊抗綠膿桿菌的抗生素才能治療,因此在臨床間常發生延誤就醫,治療的關鍵時間是3日內。
接種疫苗成常態? 美國FDA呼籲:新冠疫苗一年一打
近期由於新冠肺炎疫情趨緩,過去那種緊張「何時可以打疫苗」的日子算是結束了。而美國食品暨藥物管理局(FDA)則在23日表示,呼籲健康的成年人每年應該要接種1劑新冠肺炎疫苗,就像每年接種流感疫苗一樣。根據《路透社》報導指出,美國FDA此舉其實是為了簡化美國當地的疫苗戰略,FDA建議健康的成年人應該每年接受一次更新病毒株的新冠肺炎疫苗,就像是每年接種流感疫苗一樣。而針對幼兒、老年、免疫力低弱的族群,FDA則建議每年應接種2次新版本新冠肺炎疫苗。而除此之外,FDA也建議應該要淘汰最原始的疫苗,全面改以針對Omicron變異株的雙價疫苗作為主要疫苗。目前FDA為此請外部顧問團隊進行評估與研究,雙方預計會於26日進行會議討論。如會議討論結果良好的話,屆時可能最快會在9月推行計畫。報導中也指出,目前美國當地的疫苗接種方針是,在間隔3至4星期這段時間,先接種2劑原始的新冠肺炎疫苗。在接種完2劑疫苗後過幾個月,在開始接種針對各式變異株的加強劑。而如果屆時FDA的專家小組通過這項計畫的話,輝瑞與莫德那最新開發出來的雙價疫苗,就有可能一舉取代傳統的新冠肺炎疫苗。
美時肺癌用藥添生力軍 獲美FDA暫定審查核可搶攻18億美元市場
特殊學名藥廠美時(1795)今(16日)宣布旗下癌症用藥Nintedanib Capsules學名藥證申請,已得到美國食品暨藥物管理局(FDA)暫定審查核可(Tentative Approval),搶攻18億美元(約新台幣545億)市場。該藥品為百靈佳殷格翰OFEV的學名藥,美時將在正式取得藥證後進行上市活動。美時製藥總經理Petar Vazharov表示,繼2022年血癌用藥Lenalidomide在美國成功上市後,公司不斷地追求美時整體在美國藥品市場更高的競爭力,此次再取得肺癌用藥Nintedanib於美國FDA的暫定審查核可,不僅讓美時的肺癌用藥產品線新添生力軍,更展現了其在口服癌症用藥市場愈見精進的實力,並為了提供全球患者可負擔的癌症藥品持續努力。根據國際醫藥專業研調機構IQVIA的數據顯示,2021年度OFEV在美國的銷售金額約為18億美元。目前共有4家學名藥公司,包含Glenmark、Accord、Eugia及美時,且已分別獲得此一產品的暫定審查核可。美時去年12月營收12.7億元,月增18.6%、年增39%;第四季營收31.7億元,季增41.1%、年增13.1%,單月、季營收雙寫三年同期新高;全年合併營收約新台幣146.3億元,年增16%,連續3年實現雙位數的年成長。其中亞洲市場與去年相比增長6%,主要受惠於台灣國內業務的快速擴張。美時在亞洲以外的出口業務增加了28%,主要來自Lenalidomide在全球多個市場上市的成果,其中美國市場成功上市是重要動能。

美國逾250萬青少年吸電子煙 FDA官員:構成嚴重健康風險
美國食品暨藥物管理局(FDA)自2016年以來,致力於打擊青年使用含尼古丁的各種口味電子煙。美國近日一項調查發現,2022年逾250萬美國青少年吸電子煙,推算當時國高中生中約有255萬人使用電子煙。據《路透社》報導,疾病管制暨預防中心(CDC)於1月18日至5月31日對全國青少年進行調查,當中有4分之1的學生表示每天都使用電子煙。而表示使用電子煙的學生中,將近85%的學生吸的是「調味電子煙」,其中有超過半數的學生使用一次性電子煙。FDA煙草產品中心主任布萊恩(Brian King)表示,美國青少年使用電子煙的比例仍處於令人擔憂的水平,且對年輕人構成嚴重的公共健康風險。美國市面上能看到的調味電子煙產品。(圖/達志/路透社)調查發現,美國電子煙公司「Juul Labs Inc」已退出青少年最喜愛電子煙品牌排行榜。目前Puff Bars、英美煙草公司「BATS.L」的電子煙產品最受青少年歡迎。調查結果顯示,電子煙使用量比去年有所上升,但比2019年及2020年有所下降。往年的學生是在課堂中配合完成這項調查,而2021年有將近一半學生是遠程進行調查。因此這項調查結果,與數據收集方式改變有關,CDC提醒不要將2021年調查結果與其他年份的調查結果做比較。CDC吸煙與健康辦公室(OSH)基特納(Deirdre Kittner)表示,這項研究指出「我國愈發多年輕人持續被含有尼古丁的電子煙裝置吸引和迷住。」

聯亞母女撕破臉!員工「薪資銀行」選邊站惹議 金管會將了解
聯亞集團「母女」經營權之爭愈加猛烈,原與創辦人王長怡同一經營團隊的兩名幹部「選邊站」,相繼遭移送法辦及惹上官司,「女兒派」也反擊對王長怡提告,展開激烈法律戰。不過,根據CTWANT調查,兩派攻防之中,就連員工薪資銀行也被扯入而「逕行凍結」資金,最為惹議,這也引起金管會與立委關注,將予以了解。聯亞集團旗下包括國內疫苗大廠聯亞生技、聯亞藥(6562)等,由聯亞創辦人王長怡於2020年研發新冠疫苗UB-612(2019 COVID-19冠狀病毒疾病),當時因台灣募資不易,王長怡還特地回美國與女兒、女婿走訪華爾街生技醫療專業投資機構,三度取得資金,因此聯亞疫苗不只打國產盃,更是打國際盃。聯亞新冠疫苗UB-612先於去年向衛福部申請緊急使用授權(EUA),同年8月食藥署宣布未通過審查;今年3月則再次提出EUA申請,4月即傳出透過UBI分割子公司Vaxxinity獲流行病預防創新聯盟(CEPI)支持贊助925萬美元(約新台幣2.69億元),執行美國食品暨藥物管理局(FDA)核准的「多國多中心臨床三期試驗」。根據CTWANT調查,UB-612從研發、試驗、申請使用核准到開發市場同時,聯亞集團卻傳出王長怡與女兒在公司控股股權等的經營權歧見到互控。目前王長怡仍能掌控位於新竹的聯亞生技,該公司員工約80人,原本至5月底皆如期發放薪水給員工,豈料在6月下旬,卻傳出負責匯薪資的某公股銀行卻「臨時凍結」該帳戶,讓雙方經營權之爭更加浮出檯面。從王長怡及女兒派各自發出的聲明來看,發生該起薪資戶銀行凍結資金之案,起因疑涉及「銀行(行員)如何判斷而決定逕行凍結」的過程,涉及到公司大小章、銀行開戶印鑑章等的掌控權與否。以創辦人王長怡一方的聲明來看,提到「任職聯亞生技20餘年財務處長涉及侵占公司大章,拒絕交還停職移送法辦調查,且大章落入聯亞集團另一家公司」,再對涉案人員提出相關告訴中,可了解王長怡目前掌控的聯亞生技並無大章。但再看「女兒派」聲明所稱,「王長怡透過非財務主管員工不法竊取聯亞公司財務印鑑使用,企圖辦理銀行匯款,造成銀行困擾,才暫停帳戶,銀行同意就無爭議包括員工薪資等款項可逕行放款」,可知聯亞薪資戶印鑑章應由王長怡掌控。王長怡一方所述,聯亞生技員工薪資戶凍結一案,應是股東之一的國發基金居中澄清誤會才解凍該帳戶;但女兒派則說是經由其協調銀行才願放款,雙方皆說是他們的努力成果,但該帳戶會遭凍結,關鍵在於銀行,到底是要看誰能真正代表公司經營者,或是看誰到底擁有該銀行帳戶印鑑章。
美國爆發嬰兒奶粉缺貨潮 外媒分析背後多重因素
美國近期爆發嬰兒奶粉的缺貨潮,雖然表面上看起來原因是美國本土最大的配方奶粉廠宣布閉廠。但《CNN》特別製作專題、抽絲剝繭分析引發這場缺貨潮背後的各種原因。健康方面,先前傳出亞培的配方奶粉疑似受到污染,導致4名嬰兒患病。之後更傳出有2人在飲用亞培於密歇根州的工廠所生產的配方奶粉後死亡。雅培懷疑死亡的因而是感染罕見的阪崎腸桿菌(Cronobacter sakazakii),死因與配方奶粉無關。假新聞方面,美國的父母們正在尋找配方奶粉的替代品,但由於假新聞四處流串,就有專家表示,民眾切勿在家中自行製作配方奶粉。商業方面,雖然出事情的奶粉是亞培特定批號的配方奶粉,但選擇關閉整座生產,直接加劇全國性的短缺,間接造成全美的大缺貨。根據即時數據跟踪機構Datasembly報告顯示,美國有8個州與哥倫比亞特區都發生了市售一半的配方奶粉缺貨的事情。而亞培則表示,只要美國美國食品暨藥物管理局(FDA)同意,目前停工的密歇根工廠能在2周內復工,同時在6至8周內完成配方奶粉的上架。檢舉人方面,一名亞培的前僱員向FDA提出檢舉,內容中表示亞培在召回配方奶粉的數個月前,就知道奶粉出了安全性問題,但卻選擇隱瞞。透明度方面,根據《消費者報告》和其他新聞機構通過《訊息自由法》所獲得的文件,內容中顯示FDA早在2021年9月就收到有關嬰兒配方奶粉的檢舉,但一直到2022年2月時,亞培才宣布召回受汙染的奶粉。FDA也在3月表示,亞培位於密歇根州的工廠其實早在2019年就檢測出一系列的問題,但一直到停工前,該工廠一直沒有採取有效的措施來杜絕產品遭受汙染。商業貿易方面,由於監管原因和美國最近的貿易協定,美國禁止從其他國家進口配方奶粉,這也導致了境內配方奶粉缺貨的加劇。保護方面,美國政府單位一直致力於保護嬰兒,過去對配方奶粉實施遠高於其他國家的監管與審核,如今面臨缺貨潮時,許多美國家庭幾乎不可能適應,或是尋找替代品。

出國者白打高端 沈富雄:政府應向國人致歉
中央疫情指揮中心日前宣布,因應民眾出國需求,曾接種一劑或劑劑高端疫苗者可混打AZ、BNT以及莫德納疫苗。對此,前民進黨立委沈富雄直言,「高端混打」是現代版的指鹿為馬,政府讓國人接種國際不認可的疫苗,應向高端接種者致歉。美國規定自8日起,所有外籍旅客須接種2劑獲美國食品暨藥物管理局(FDA)或世界衛生組織(WHO)核准疫苗才可入境,衛福部長陳時中曾評論「美國祭出這樣入境規定怪怪的。」對此,沈富雄批評,陳時中明明知道「怪怪」的原因在哪裡,卻不坦白告訴國人真相,企圖掩飾錯誤政策的欺騙行為。「如果要出國,政府應誠實地說,兩針高端都是白打。」沈富雄直言,高端疫苗在免疫學上應是「有效」,是認證過程有嚴重瑕疵被國際視為「無效」。沈富雄說,為了出國,高端接種者必須「重打」兩針莫德納或BNT,而不是「混打」或「補打」;他批評政府,臉不紅氣不喘,公然把重打說成混打,陳時中是「今之趙高」,嚴重藐視國人的智慧及分辨能力。沈富雄建議高端接種者「重打」前,應抽血測量抗體的濃度,以示負責,更防萬一;抗體濃度過高或足夠者,重打的劑量應考慮減半或重打時間延後。沈富雄認為政府應向高端接種者致歉,讓國人接種國際不認可的疫苗還如此大言不慚,是不可原諒的失政。對於民進黨立委高嘉瑜稱「打高端者「賺到」,出國可以補打兩劑AZ、BNT或莫德納,沈富雄則批評「欲哭無淚的裝飾型幽默,不假思索、輕佻的政客表演,藍綠都覺噁心。」

開綠燈 美FDA全票通過:5至11歲兒童接種BNT
開綠燈!美國食品暨藥物管理局(FDA)專家小組,26日以全票通過,將為5至11歲兒童接種輝瑞/BNT新冠疫苗,最快11月初可望開始施打,輝瑞/BNT新冠疫苗亦成為全球第一款對12歲以下孩童注射的新冠疫苗。FDA專家委員會當天以17票贊成、0票反對、1票棄權的壓倒性多數,支持向5至11歲孩童提供輝瑞/BNT疫苗,將有2800萬兒童受惠。輝瑞藥廠先前發布臨床數據指出,其疫苗對5至11歲兒童效力達90.7%,且未見嚴重安全問題;5至11歲兒童同樣注射2劑,劑量為成年人的三分之一。另外輝瑞/BNT疫苗也將針對2到4歲幼童進行臨床試驗,預計年底前將有結果。白宮首席防疫專家佛奇24日就已預告,預期11月上旬開放該年齡層兒童施打疫苗,在年底前希望讓大部分兒童打完兩劑。FDA委員會認為,上述年齡層兒童注射疫苗的利益,遠大於罹患心肌炎等副作用的潛在風險。不過也有專家委員認為,雖然支持向5至11歲提供疫苗,但反對強制接種;另外有專家指出,應僅建議該年齡層的高風險案例注射。委員會成員、美國疾病管制暨預防中心(CDC)專家科恩表示,5到11歲兒童應該獲得其他年齡層擁有的接種機會,「我們不希望兒童死於新冠肺炎,不希望他們住進重症病房。」據CDC統計,美國已有8300名5至11歲兒童因感染新冠肺炎住院,其中三分之一在重症病房,死亡人數即將破百。美國FDA數日內就會決定是否批准在緊急授權下,開放5到11歲施打疫苗,依照前例,FDA通常會遵循專家委員會的意見,CDC則將在下周,決定是否作出同樣建議。FDA目前已完全批准輝瑞/BNT疫苗在16歲以上族群的使用,12至15歲則是獲得FDA核可緊急授權使用。

「嬌生單劑型疫苗」抗體較莫德納低 美專家建議政府追打第2劑
為對抗新冠肺炎疫情,各國公衛專家關注如何讓疫苗效力更強、更久,美國食品暨藥物管理局(FDA)外部顧問15日建議FDA批准,所有接種嬌生COVID-19「單劑型疫苗」的人接種第2劑疫苗。綜合「路透社」等外媒報導,食藥局的疫苗和相關生物產品諮詢委員會(Vaccines and Related Biological Products Advisory Committee)支持所有接種嬌生(Johnson & Johnson)疫苗的18歲以上民眾,可在接種第1劑疫苗後,至少2個月後接種追加劑,小組成員指出,相較於莫德納疫苗、BNT疫苗這類mRNA疫苗而言,嬌生疫苗產生的抗體濃度較低,因此給出上述建議,雖然這類建議無強制力,但FDA一般都會遵守。會議主持密西根大學公共衛生學院流行病學者孟多(Arnold Monto)表示,「這是公衛上的當務之急,我們看到一群人整體疫苗效力較低,迫切需要做些什麼」。報導指出,一但美國食藥署批准施打第2劑,疾病管制暨預防中心(CDC)就會因應接種的群體提出具體建議,而美國疾管中心也預定下週開會討論追加劑議題。事實上,為確保脆弱人群有足夠保護力,美國食藥局在上個月就批准65歲以上、重症高風險人群,和工作上易接觸病毒者追加施打輝瑞/BNT疫苗,目前也正在考慮將接種疫苗追加劑的年齡下降到40歲。

拜登接種BNT第3劑「加強針」 捲袖挨針呼籲:符合資格的人,快去打
全球新冠肺炎疫情未歇,日前已經完成BNT兩劑疫苗接種的美國總統拜登,於台灣時間28日凌晨1點左右,完成加強針(第三劑)接種。他日前也出面曾呼籲民眾,加強針是「新武器」,符合接種資格的國民,最好趕快去打針。今年78歲的拜登(JoeBiden),去年12月接種輝瑞第一劑,今年1月接著注射第二劑,時隔將近10個月的時間,他帶頭捲袖在全美民眾面前,接種第3劑輝瑞/BNT疫苗。拜登透露,他自己先前打過兩劑BNT疫苗,身體都沒有出現不適,強調第三劑疫苗的作用是屬於「加強針」,安全有效,呼籲民眾應儘快接種。美國食品暨藥物管理局(FDA)本月22日,已針對65歲以上民眾及高風險族群,開放接種第三劑疫苗來加強防禦效力,但這一針的施打,必須與第二劑至少間隔6個月。而美國目前打完完整兩劑疫苗的接種率約為55.3%,其中55%民眾施打輝瑞/BNT疫苗、37%打的是莫德納疫苗,8%則是嬌生疫苗。
AZ疫苗新副作用 歐盟增列罕見神經病變「格林巴利症候群」
歐洲藥品管理局(EMA)8日增列一種極為罕見的神經損傷疾病「格林巴利症候群」(Guillain-Barre Syndrome,GBS),作為接種AZ疫苗可能的副作用。根據《路透社》報導,歐洲藥品管理局表示,截止至7月31日,在全球接種的5.92億劑疫苗中,通報了833例「格林巴利症候群」病例,顯示接種AZ疫苗與「格林巴利症候群」之間的因果關係為「至少是合理的可能性」。歐洲藥品管理局將此副作用歸類為,非常罕見。歐洲藥品管理局表示,「格林巴利症候群」是接種AZ疫苗後,出現的副作用中,頻率最低的。歐洲藥品管理局強調,注射疫苗的好處超過可能帶來的風險。而在這之前,美國食品暨藥物管理局(FDA)就曾對嬌生集團(J&J)生產的疫苗,加註警語,稱其疫苗副作用可能出現「格林巴利症候群」的副作用。至於何謂「格林巴利症候群」,專家諮詢小組召集人張上淳曾在記者會中說明,主要是免疫反應造成的周邊神經傷害引起的,症狀為肌肉無力、呼吸衰竭等。

最快秋天!5至11歲兒童將有疫苗可打 BNT疫苗可望獲得美國EUA
輝瑞董事會成員、美國食品暨藥物管理局(FDA)前局長哥提列(Scott Gottlieb)接受美國媒體《CNBC》訪問時說,輝瑞計畫在今年9月時,將公布5至11歲孩童的疫苗試驗數據,並提交數據給FDA。哥提列表示,就緊急授權使用的審查時間而言,FDA大約需要4到6周時間,所以預計批准時間將會在秋季末期或初冬。輝瑞BNT疫苗是美國目前唯一獲得完全授權的新冠肺炎疫苗,但此授權只針對16歲以上民眾,12至15歲的人群雖然也能施打,但僅限在緊急授權使用的情況下。如今哥提列的發言也顯示,針對,輝瑞BNT新冠肺炎疫苗可望在今年秋冬獲得美國食品暨藥物管理局緊急授權使用(EUA)。疫情中心指揮官陳時中今天於記者會上表示,未來美國FDA若通過輝瑞BNT疫苗5至11歲兒童的EUA,將於審查藥廠相關資料之後再做決定。