BRCA
」 癌症 乳癌 攝護腺癌 健保 基因
次世代基因定序檢測納健保「申請率10%」 HOPE:癌友面臨3項為難與抉擇
「次世代基因定序檢測(NGS)」自2024年5月1日起納入健保給付,迄今已超過一年又三個月,健保署預估每年約2萬多名癌症病人受惠,挹注經費約3億元,接軌癌症精準醫療趨勢。據悉,目前申請件數超過2千件,約達預估數額的十分之一,CTWANT採訪到HOPE癌症希望基金會,發現許多癌友面臨3項為難與抉擇,可能是讓他們提出申請卻步的原因;對此政策HOPE予以肯定之外,同時也提出4點建議,希望讓每位癌友都能在適當時機受惠。CTWANT記者訪問到HOPE癌症希望基金會副執行長嚴必文,就NGS納健保上路一年多來,癌友使用情況給予一些分享,她表示,「NGS的確帶給癌友的新契機」,透過基因分析找到個人化治療方案,提高存活率與生活品,許多癌症病友也歡欣鼓舞期待這個新政策到來,為治療帶來更多的曙光。「感到遺憾的是,NGS給付上路首年申請量未達當初預期每年2萬名病友受惠的規模(可能因初期制度適應與宣導期所致),實際受惠者僅10分之一左右,但我們相信也希望,未來狀況會逐漸提升。」嚴必文說。嚴必文提到,然而,HOPE的確在一線的病友服務中,發現還是有許多病友對於「NGS健保定額給付政策」不是完全了解,因此當實際想申請時,卻發現因應檢測模組不同,扣掉健保給付費用,個人可能還要支付數萬到十萬元,對於部分經濟狀況較吃緊的病友而言,這筆額外費用就會形成沉重壓力,從而影響病友檢測意願。次世代基因定序檢測(NGS)納入健保給付涵蓋19種癌症,每人每癌別可終生給付一次。圖為基米實驗室人員檢測現場。(示意圖/方萬民攝)CTWANT記者進一步詢問,就「醫生有建議癌友使用NGS,卻未申請」的原因有哪些?嚴必文說,HOPE從病人角度觀察到三個現象,一為「給付額度與自付差額差距大,經濟壓力成為主要阻礙」。如前述所言,健保對NGS採定額給付,但大型或廣泛基因套組實際費用高,自付差額常達數萬至十萬元,對經濟負擔重的病友家屬造成極大壓力。「還有,面臨檢測等待時間與治療時機衝突,急需疾病快速決策」,嚴必文說,NGS檢測需約3-4週出報告。對於病情進展迅速的患者(尤其像急性血液病癌症)而言,等待期間可能錯失標靶治療的黃金時機。另外,醫師通常也可能傾向先做單基因快速檢測(3-4天)以確定常見突變,以儘快展開治療,若陰性再考慮更全面套組。嚴必文接著說,「終身一次給付政策」讓醫師與病友在申請時產生猶豫,影響申請率與治療策略彈性,政策上每人每癌別終身僅健保給付一次,因此醫師在早期階段建議檢測時,常與病友考慮保留給付機會,以備未來復發或抗藥性時用;結果是一些病友即使符合條件,也可能選擇不申請。對此,CTWANT進一步問HOPE,可否就此政策實施以來提出一些建議?嚴必文說,「HOPE肯定政府推動NGS健保給付的政策方向」,但也在此提出四點建議。嚴必文說,第一項建議「提高給付額度,減輕負擔」健保僅補助部分費用,大型套組自付差額可高達數萬元,許多病友因此放棄檢測;建議逐步提升給付額度,尤其照顧經濟弱勢,避免費用成為阻礙。其次,建議「放寬適用條件,增加彈性」嚴必文說,目前每人每癌別終身僅給付一次,導致醫師與病友在檢測時機上猶豫;建議針對復發或抗藥性病友,增設一次檢測機會;並隨醫療證據更新,擴大納入更多癌別,讓更多病友受惠。嚴必文並建議「強化藥物給付」,若找出突變卻無藥可用或用不起,NGS檢測將失去意義;應同步放寬標靶及免疫藥物的健保給付條件,延長療程,確保病友「找得到、用得起」。「持續簡化醫院申請流程,並擴大NGS可近性,讓每位癌友都能在適當時機受惠。」嚴必文就HOPE癌症希望基金會在服務一些癌友時的觀察,提出以上的建議。目前NGS的健保給付將涵蓋19種癌症,包括14種實體腫瘤和5種血液腫瘤,以NGS及單基因檢測提供民眾多元選擇。給付區分為BRCA、小套組、大套組等三種,依檢測基因數支付不同點數,最高支付定額3萬點,另依專家建議各癌別之檢測時機不同,每人每癌別可終生給付一次。
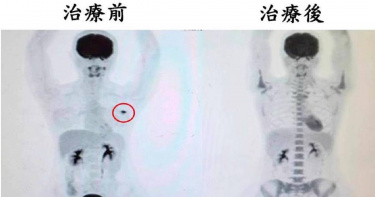
37歲女罹三陰性乳癌 「先期化療再開刀」腫瘤細胞全消失
37歲的吳女士因觸摸到左乳房腫瘤而至乳房外科就醫,經檢查確診為三陰性乳癌。由苗栗縣大千醫院安排接受六次先期性化學治療,待腫瘤明顯縮小後再手術切除。術後的病理化驗顯示,腫瘤細胞已完全消失,亦無淋巴轉移,整體治療非常成功,目前持續門診追蹤。大千綜合醫院乳房外科醫師陳以涵表示,三陰性乳癌是一種乳房惡性腫瘤,約佔所有乳癌的8-15%。其雌激素接受體(ER)、黃體素接受體(PR)以及第二型人類表皮生長因子受體(HER2)均為陰性,且對傳統的荷爾蒙治療或HER2標靶治療無效,故以化療藥物作為主要治療方式。陳以涵醫師建議,女性應定期接受乳房檢查,才能早期發現異常、早期接受治療,及早恢復健康人生。(圖/大千醫院提供)陳以涵說明,三陰性乳癌的特點有:1.發病年齡較輕,多數小於40歲。2.抑癌基因(BRCA1、BRCA2)突變機率較高,大約占25%(一般乳癌病人約為2%)。3.細胞分化惡性度較高。4.容易有淋巴結轉移。5.有較高的機會轉移和復發。陳以涵指出,目前許多臨床研究顯示,三陰性乳癌病人若接受先期性化學治療(亦即在手術前先做化學治療)的效果會比其他類型的乳癌較好,特別能達到病理完全反應。透過先期性化療,將原本在手術後做的輔助性化療提早至術前執行,在化療的同時觀察腫瘤大小的變化,可確認腫瘤對藥物的反應。若能在先期性化療後達到病理完全反應,其預後比較好,反之則容易發生癌細胞復發和轉移,建議要再追加化療或標靶藥物作為輔助性治療。先期性化學治療能幫助醫師掌握病人的治療成效,不僅有較高的機會保留乳房,還有助減少復發、轉移的風險,提高三陰性乳癌病人的治癒率及存活率。但要注意的是,接受先期性化療的病人,較可能因為免疫力下降,容易有術後傷口感染或是癒合不良的風險。陳以涵示,一般乳癌在腫瘤切除手術後再接受輔助性化療,是無法立即觀察藥物的成效,而是在一段時間(2-3年)後再追蹤是否有復發轉移,才能知道藥物有無效果。對於容易復發及轉移的三陰性乳癌,若能透過先期性化療,了解藥物治療對癌細胞的效果,就能提高治癒率及存活率,進而恢復健康的人生。
一家四口一年半內「全罹癌」 醫示警:親屬中兩人罹癌應立即基因檢測
居住在中國湖南武漢的李姓女子,近日在短影音平台分享自己一家在一年半內陸續確診癌症的經歷,迅速在網路上引發廣泛討論。她表示,自己與母親都罹患甲狀腺癌,公公被診斷出口腔癌,而婆婆則確診乳癌,四人皆有癌症家族史。根據《快科技》報導,這起病例不僅凸顯遺傳風險的重要性,也喚起社會對癌症早期篩檢的關注。從公開資訊來看,李女與母親的病情有高度遺傳傾向,醫師研判可能與RET或BRAF基因突變有關;這類遺傳性甲狀腺癌約佔整體病例的5%至10%。李女的公公過去曾有家族成員罹患口腔癌,婆婆則有乳癌家族病史,醫學界普遍認為,BRCA1或BRCA2基因突變可能導致乳癌遺傳風險升高。研究顯示,約10%的癌症與特定基因突變密切相關,若直系親屬中兩人以上罹患相同癌症,或不同類型的癌症頻繁出現在家族內,便需提高對家族性癌症症候群的警覺,例如李奇症候群或遺傳性乳癌-卵巢癌症候群。雖然李女與其他三位家庭成員並未同住,但各自的生活習慣與環境因素仍可能成為致癌的加速器。特別是口腔癌方面,長期抽菸、嚼食檳榔與口腔衛生不佳等因素都被視為高危險因子。乳癌則與荷爾蒙變化、肥胖與壓力水準密切相關。由於家人相繼罹癌,心理壓力加劇,也可能對免疫系統造成潛在衝擊。截至目前,這個家庭的癌症治療費用已超過人民幣30萬元,其中公公因接受放射治療後身體出現較嚴重損傷。醫界建議,高風險家族應盡早建立家族癌症圖譜,並透過遺傳諮詢與基因檢測來掌握風險,常見如BRCA與RET基因等。對於有甲狀腺癌傾向者,每年應接受一次頸部超音波與甲狀腺功能檢測;乳癌則建議40歲以上女性每年安排乳房攝影與超音波;口腔癌患者可每半年做一次黏膜檢查與病理切片檢查,搭配低劑量電腦斷層與腫瘤標記檢測做全方位追蹤。此外,李女的經歷也點出一般民眾對癌症遺傳的常見誤解。有些人誤認為癌症具傳染性,但事實上,癌細胞無法在人與人之間傳播。即使攜帶致癌基因,也不代表必然會發病,只要及早介入,風險可大幅降低。好萊塢女星安潔莉娜裘莉(Angelina Jolie)曾因家族病史選擇預防性切除乳房,即是一例。

早期三陰性乳癌治療迎曙光! 6月起「2類藥」納健保給付
53歲的Amanda,2年前確診早期三陰性乳癌,讓定期做健檢、沒有不良嗜好的她感到晴天霹靂。在商保支持下,她自費逾200萬接受免疫藥物輔助治療。現在的Amanda病情獲控制、預後良好,希望能繼續陪伴雙胞胎孩子長大,不再錯過他們人生的重要時刻。今(2024)年6月,健保將免疫藥物輔助治療與PARP抑制劑正式納入早期三陰性乳癌給付。看到原先無法負擔高昂藥費的病友姐妹可受惠,Amanda也為她們感到開心。健保署龐一鳴副署長指出,台灣隨著乳癌篩檢的推廣,使得早期發現率很高,但標準化死亡率未見改善,與疾病易復發、年輕化趨勢以及過去缺乏治療方法有關。雖然難以阻止乳癌的發生,但死亡率有望透過治療降低,龐副署長表示,健保署將根據科學實證數據提供更多好的治療工具,呼籲病友積極面對治療,期待接下來的兩三年能看到死亡率數字的改善,從而實現「健康台灣」願景。早期三陰性乳癌過去僅化療納健保 新藥給付可用於術前術後台灣乳房醫學會陳芳銘理事長表示,台灣逾8成乳癌病友確診時為早期。在乳癌亞型中,三陰性乳癌大約佔10%至15%,惡性度較高,五年內復發風險近3成,尤其是「腫瘤介於1-2公分且合併淋巴轉移」或「腫瘤大於2公分」的高風險早期三陰性乳癌族群,更易復發、存活率偏低。針對高風險性早期三陰性乳癌,過去的健保給付以化療為主。陳芳銘理事長指出,從去年開始,健保加速接軌國際,陸續新增和擴大乳癌用藥給付,而此次新增的PARP抑制劑與免疫檢查點抑制劑,可用於早期三陰性乳癌術前和術後治療,預計嘉惠近800位病友。患者多認為一旦確診早期乳癌,就應立即手術。陳芳銘理事長說明,術前採用輔助治療,可先讓腫瘤縮小,保留更多乳房。研究顯示,高風險早期三陰性乳癌病友,接受完整術前、術後免疫藥物輔助治療,5年疾病惡化與腫瘤復發風險降低近4成,整體死亡率下降約3成5,對於亞洲族群的效果更顯著。另外,具BRCA1/2基因變異、合併高復發風險的早期三陰性乳癌病友,術後接受PARP抑制劑治療,侵襲性疾病及遠端疾病的發生風險則可降低約4成。三陰性乳癌年輕患者多 早期治療有望達完全緩解中華民國乳癌病友協會黃淑芳理事長表示,三陰性乳癌常發生在年輕女性身上,職場衝刺、婚育計劃都因為罹癌而被迫中斷,令人感到惋惜。陳芳銘理事長表示,本次給付讓早期三陰性乳癌有機會在「手術前」就獲得免疫藥物的輔助治療。陳芳銘理事長表示,研究顯示,三陰性乳癌患者在術前接受免疫藥物搭配化療,有6成達到腫瘤完全消失(pCR),其餘4成患者持續接受合併療法,也有助降低復發風險、延長存活。陳芳銘理事長也提醒,化學治療和免疫治療都會產生相應的副作用,化療最常見的副作用是白血球過低,目前健保也有給付白血球生成素,助改善副作用。免疫治療最大的副作用則是影響內分泌功能,例如甲狀腺功能和血糖,醫師會定期監測並透過藥物調整。治療過程中發高燒的狀況可能是白血球降得太低,引發感染所致,或是少數情況下免疫治療造成甲狀腺素升高,導致代謝性發燒。他指出,過去患者多因為害怕副作用而對治療卻步,不過目前多數副作用都有應對策略,患者都可及時與醫師反映處理。乳房篩檢持續推廣中 醫:望篩檢率與國際比肩黃淑芳理事長指出,中華民國乳癌病友協會提出了「極早的篩檢、極早的發現、極早治療」口號,持續推動乳房篩檢,國健署的數據也顯示,目前篩檢人數已達到6萬多人。高雄市乳癌防治衛教學會侯明鋒理事長則表示,台灣的篩檢推廣表現良好,但篩檢率與其他國家相比仍有提升空間,因此提升篩檢率與國際比肩,仍是未來需要共同努力的方向。【延伸閱讀】沒症狀=沒問題?乳癌早期無聲息 醫曝自篩1最佳時機不是過了5年就沒事! 醫籲「3族群」當心荷爾蒙陽性乳癌復發風險https://www.healthnews.com.tw/readnews.php?id=65510

2抑制劑擴增給付5癌 健保署:6月上路
衛福部統計,國人卵巢癌、輸卵管癌、原發性腹膜癌,以及早期乳癌,為2022年女性發生率前十名,攝護腺癌為男性發生率前三名。為提升癌症病人的治療權益,健保署宣布通過2項PARP抑制劑擴增給付5癌,6月上路,每年約775人受惠,新增9.79億元健保支出。如與拜登同為攝護腺癌,且符合轉移性、基因突變,在台灣就可符合健保用藥,有助增加1年存活率。健保署醫審及藥材組組長黃育文表示,本次擴增給付的藥品為olaparib及niraparib。在卵巢癌、輸卵管癌及腹膜癌的治療上,擴增給付於「具HRD陽性且含致病性BRCA突變或基因不穩定」者。使用olaparib於合併治療,可延長整體存活期中位數17.9個月,費用約147萬元。使用niraparib,則可延長無惡化存活期11.4個月,約140萬元。在早期乳癌治療上,此次擴增olaparib的給付於「具germline BRCA1/2突變併HER2陰性高復發風險的早期乳癌」,可降低42%侵襲性疾病、43%遠端疾病的發生風險,費用約75萬元。至於攝護腺癌,則給付olaparib於「具germline或somatic BRCA1/2致病性或疑似致病性突變」患者,合併治療費用約204萬元。台灣泌尿腫瘤醫學會理事長王弘仁說,約十分之一的晚期攝護腺癌患者有BRCA1/2基因突變,過去的治療方式包含荷爾蒙治療、化學治療,如今則多了新選項。比起未使用者,約增加1年的存活率,可維持病情不惡化。王弘仁建議患者先接受次世代基因定序(NGS)檢測,了解基因突變。若與拜登病情類似,即攝護腺癌轉移,又有BRCA1/2突變,即可符合健保用藥條件。

「這癌症」是男性晚年隱形殺手? 醫籲:熟男應定期檢查
攝護腺癌是專屬男性的癌症,台灣男性發生率第三名,連退休醫師都可能疏忽,險危害健康!該名男醫師現年73歲,因朋友確診攝護腺癌,才主動前往醫院進行檢查,從抽血報告中看到,雖攝護腺特異抗原(PSA)指數並未明顯偏高,但因攝護腺健康指數(PHI)異常升高,主動要求進行攝護腺切片檢查,並進一步確診為攝護腺癌。所幸發現得早,也馬上接受根除性攝護腺切除手術,術後恢復良好,目前僅須持續追蹤,可以好好享受退休生活。高風險族群勿輕忽 攝護腺癌恐危及生活品質攝護腺癌為台灣男性常見癌症之一,童綜合醫院研發創新中心院長、泌尿科歐宴泉醫師指出,該疾病在早期通常無明顯症狀,極易被忽視,根據臨床統計,台灣約有三成攝護腺癌患者出現下背痛、骨骼疼痛、骨折、體重異常減輕、貧血、腎功能異常,甚至下半身麻痺等症狀後才就醫,延誤治療時機,使後續治療更具挑戰,對生活造成重大影響。歐院長進一步指出,攝護腺癌好發於60歲以上族群,特別是有家族病史者,或帶有特定遺傳基因突變(如BRCA1、BRCA2、HOXB13),以及長期高脂飲食、缺乏運動、肥胖,或因荷爾蒙失衡導致前列腺異常增生的男性,也都屬於潛在高風險族群。歐院長強調,年過半百的男性,尤其具有遺傳背景或不良生活習慣者,務必定期進行泌尿系統健康評估。抽血就能檢測! 早期發現根治有望隨著男性健康意識抬頭,攝護腺癌的早期篩檢方式也趨向多元。歐宴泉院長指出,過去檢查方式以檢測血液中的攝護腺特異性抗原(Prostate Specific Antigen, PSA)搭配肛門指診。雖然是最普及與常見的篩檢方法,但其結果容易受到年齡、攝護腺體積大小、是否發炎等多種因素影響,不具高度專一性,加上PSA本身並無明確的正常值,僅具參考性質,部分良性疾病也可能導致PSA指數升高,增加誤判風險。因此,為提升診斷準確性,現今臨床上常結合「攝護腺健康指數」(Prostate Health Index, PHI)進行評估。歐院長強調,若能在早期階段發現攝護腺癌,經過妥善治療,患者有機會實現根治,並可保持良好的生活品質。PHI提升篩檢精準度 有效協助診斷與治療建議攝護腺健康指數(PHI)作為一項新興的檢測工具,已在臨床診斷中發揮著重要作用。歐宴泉院長指出,PHI由三項與PSA相關的指標組成,數值的高低與攝護腺癌(PCa)的風險密切相關,根據PHI的數值,醫師可以將患者分為不同的低、中、高風險等級。藉由這項指標能夠更精確地評估男性罹患攝護腺癌的風險,有助於醫師在篩檢過程中判斷是否需要進一步進行切片檢查,從而有效減少不必要的侵入性檢查。歐院長補充,PHI檢測是一項簡便且可靠的血液檢查,對於早期發現攝護腺癌具有極大意義。PHI能補強PSA的盲點,比單獨使用PSA檢測更為準確,尤其在區分良性攝護腺疾病(如攝護腺良性肥大)和攝護腺癌時,具有明顯優勢,亦能更精確地預測惡性癌症的風險。推動男性健康意識 醫籲「熟男」應定期檢查歐宴泉院長多年來積極守護男性的健康,致力於推動攝護腺癌的篩檢普及。雖然目前攝護腺癌尚未列入篩檢補助計畫,歐院長仍強烈建議,50歲以上的一般男性,或是40歲以上且有攝護腺癌家族病史的高風險族群民眾,應養成定期檢查的習慣,透過積極的健康管理,男性可在早期發現疾病,及時介入治療,從而有效把握治療的黃金時機,降低晚期併發症的風險,提高生活品質和整體存活率。歐院長也提到,抽血檢查只需三分鐘,提倡「三分鐘護一家」的觀念,呼籲政府應積極推動男性癌症篩檢,保障男性健康。【延伸閱讀】攝護腺癌治療選擇需考量「這些」 海福刀助患者快速回歸工作崗健保延長新一代口服荷爾蒙治療年限!高風險轉移性攝護腺癌患者治療更有保障https://www.healthnews.com.tw/readnews.php?id=65140

4大「致癌原因」你中幾個? 醫:吸菸罹癌風險飆30倍
癌症為我國10大死因第1位,根據衛福部在去年底發布的民國111年癌症登記報告資料顯示,約有13萬人新發現罹癌、5.3萬人死於癌症。醫師黃軒提醒,癌症不是無緣無故找上門,遺傳、生活方式、環境、感染都可能是幕後推手。醫師黃軒在臉書粉專發文,表示癌症就是細胞叛變的結果,人體細胞如同城市裡的小工人,平時各司其職,生長、分裂、死亡,但一旦DNA出錯,這些細胞不受控制地增生,就會形成腫瘤,再進一步擴散、攻擊身體其他器官,就是惡性腫瘤,也就是癌症。黃軒指出,這些狀況並不是憑空發生,他舉出4大造成癌症的主因:遺傳有些人天生就帶著「高危基因」,像是BRCA1、BRCA2等基因突變,會增加罹患乳癌、卵巢癌風險,研究發現,攜帶這些突變的女性,得乳腺癌的機率高達85%。不過這類遺傳因素只占癌症的少數,大部分人並不需要過分擔心。生活方式癌症界的頭號通緝犯就是吸菸,吸菸者得肺癌的風險比不吸煙的人高15到30倍,每一口菸都是在給細胞叛軍送武器。飲食方面,愛吃炸雞、漢堡,不碰青菜,以及過多的高脂、紅肉、加工食品,也會讓大腸癌有機可乘。另外,缺乏運動也會提升罹患乳癌、大腸癌的風險。環境長期在X光或放射性物質旁,像是白血病、甲狀腺癌的風險會悄悄上升。此外,工廠裡的石棉、空氣中的苯,甚至土壤裡的砷,都是潛在的致癌魔頭,可能引發肺癌或皮膚癌。感染有些癌症居然是「傳染病」惹的禍,像是人類乳突病毒(HPV)幾乎與所有子宮頸癌息息相關,而B型、C型肝炎病毒(HBV、HCV)也是肝癌的主要推手。不過黃軒表示「既然有原因,就有對策」,他建議可以靠「6行動」降低罹癌風險,像是戒菸、健康飲食(少碰燒烤、培根)、每週快走150分鐘、遠離毒物(石棉、輻射等)、並接種疫苗與定期健檢,就能把癌症的威脅甩得遠遠的。

壓力大就狂吃高熱量! 醫曝罹癌風險恐增加
壓力會讓大腦啟動「獎勵系統」,讓我們更容易渴望高糖、高脂肪的食物,因為它們能瞬間帶來愉悅感。基因醫師張家銘透露,這是一種演化上的生存機制,當人類還在遠古時代時,遇到壓力往往意味著危機,例如食物短缺或天敵威脅,此時高熱量食物是最好的能量儲備來源,問題是,這種本能在現代社會變成了一種隱形陷阱。張家銘在粉專《基因醫師張家銘》表示,壓力大可能影響免疫系統,導致睡眠品質下降,讓身體更容易出現發炎反應,而壓力與高熱量飲食的組合,竟然能攜手改變體內的分子機制,讓癌細胞的生長環境變得更有利。他提出,2025年發表在期刊《Molecular Cancer Research》的一項研究發現,當身體處於壓力狀態時,會釋放大量腎上腺素,進而活化一種叫做 CREB(cAMP 反應元件結合蛋白) 的分子,而這個分子正好能促進癌細胞的生長;同時,如果這時候攝取高糖、高脂肪食物,體內的 神經降壓素濃度也會升高,而這種物質不僅與肥胖有關,還會進一步加強 CREB 的活性,等於是幫助癌細胞加速繁殖,換句話說,單單壓力或高熱量飲食,可能還不足以讓癌細胞大舉擴張,但當兩者結合時,就像在乾燥的木柴上點燃火苗,讓癌細胞有了最佳的生長條件,如果再加上遺傳基因的影響,那麼癌變的風險將大幅提高。張家銘提到,癌症幾乎都不是單一因素造成的,而是「基因+環境+生活習慣」長期交織的結果,如果家族中有人曾罹患癌症,或是基因檢測發現自己帶有BRCA1、BRCA2、TP53、KRAS這類與乳癌、胰臟癌、肺癌相關的變異,那麼就需要更加謹慎,因為壓力與飲食可能成為觸發癌細胞增長的關鍵因素。拆解這場隱形風險該怎麼做?張家銘說,首先要學會察覺壓力帶來的飲食衝動,其次,可以準備更健康的舒壓食物,另外,如果家族中有癌症病史,或者擔心自己是否有遺傳風險,基因檢測會是一個值得考慮的選項,最後,建立長期的抗壓習慣是關鍵,當壓力來臨時,可以嘗試喝杯溫熱的花草茶、做幾分鐘的深呼吸、到戶外透透氣、閉上眼睛冥想、短暫放下工作做點簡單的伸展運動,只要這些行為變成習慣,大腦在面對壓力時就不會自動聯想到「吃垃圾食物」作為紓壓方式。他也直言,癌症的紅毯,不是命中注定,而是我們的選擇鋪出來的,這項研究提醒大家,癌症並非單純的「運氣問題」,而是基因+環境+生活方式的綜合作用,壓力與高熱量食物的組合,看似毫無關聯,卻能在不知不覺中,為癌細胞鋪路,如果剛好帶有癌症基因,那麼這種影響就更值得警惕。

胃癌公費篩檢明年上路 醫示警「這年齡」染病風險高
衛福部國健署宣布,明年起胃癌篩檢將正式納入公費項目,成為第6項免費癌症篩檢,預計每年投入2至3億元經費,嘉惠45到79歲約60萬民眾,每人享有一次幽門螺旋桿菌檢測。幽門螺旋桿菌感染是胃癌的主要元兇,而20歲以上國人的幽門螺旋桿菌盛行率高達30%,建議要提高檢測意識。癌症長達42年霸榜國人死因第一,其中胃癌排名第7,成為國人健康的隱形殺手。為降低胃癌的發生率與死亡率,國健署將胃癌篩檢全面納入公費,力拚2030年前降低癌症死亡率三分之一。重症、內科醫學專科(指導)醫師暨琺洋醫學診所蕭榮隆醫師指出,胃癌早期難察覺,幾乎沒有症狀,患者一旦出現不適,往往已進展到較晚期,早期發現與治療,對提高存活率極為關鍵。蕭榮隆醫師表示,胃癌男性發生率為女性的2倍,高達9成的胃癌患者曾感染幽門螺旋桿菌,建議20歲以上民眾應及早進行檢測,及早預防,大大降低胃癌的患病風險。目前胃癌篩檢分為侵入性與非侵入性檢測。侵入性檢測以胃鏡檢查為主,適用於高風險族群;非侵入性檢測則包含糞便抗原檢測、碳13尿素吹氣法,以及利用次世代基因定序技術(NGS)的「癌知因」檢測服務。美國國衛院(NIH)網站收錄的日本研究指出(註),幽門螺旋桿菌感染且同時帶有高風險基因,罹患胃癌的風險顯著提高。訊聯基因的癌症基因風險檢測(癌知因),可針對遺傳性胃癌相關的MLH1、MSH2、MSH6、BRCA1、BRCA2、PALB2、APC、STK11、TP53等9大高風險基因進行檢測,提供胃癌早期篩檢與精準評估,協助受檢者在疾病發生前及早預防,且一生只需要檢測一次。蕭榮隆醫師提醒,幽門螺旋桿菌的傳染途徑包含受污染的水、食物和唾液,家庭成員間的相互傳染是重要來源。日常應注意飲食衛生,避免共用餐具,並定期進行檢測。即便是未納入胃癌公費篩檢的部分族群,也可以早一步檢測與預防,防範癌症悄然來襲,有效捍「胃」健康。

了解卵巢癌基因檢測重要性! 醫建議應檢測「這2項目」助治療方案制定
【健康醫療網/記者吳儀文報導】基因檢測在癌症治療策略中扮演著至關重要的角色,卵巢癌亦不例外。北醫附醫婦產部教授邱德生醫師指出,目前臨床上建議卵巢癌患者進行 BRCA 1/2 基因檢測以及 HRD(同源重組修復缺失)基因檢測,以協助制定個人化治療策略。這些檢測有助於選擇適合的標靶藥物(例如 PARP 抑制劑和血管新生抑制劑),作為術後維持性療法,從而降低復發風險並延長患者存活期。卵巢癌術後維持治療:兩項基因檢測助力標靶藥物選擇卵巢癌以手術治療為主,但若病情較重而無法立即手術,可先進行術前輔助化療,然後再進行手術,術後通常搭配化學治療。然而,邱德生教授指出,多數卵巢癌患者在確診時已進展至第三或第四期,即便經過手術與化療,仍有 70% 的患者於術後兩年內復發。幸運的是,現有治療策略中包含 PARP 抑制劑和血管新生抑制劑,這些標靶藥物能夠有效減少復發風險。邱德生教授強調,基因檢測在卵巢癌治療中的重要性,正是因為透過基因檢測可以確認癌細胞的分子特徵,從而針對其弱點精準對症下藥。基因檢測重點:BRCA 與 HRD 的功能與應用針對基因檢測的具體應用,臨床建議所有卵巢癌患者進行 BRCA 基因檢測與 HRD 基因檢測。邱德生教授進一步說明:BRCA 基因檢測 聚焦於檢查 BRCA 1 與 BRCA 2 基因 是否發生突變,這兩個基因負責修復 DNA 並維持細胞穩定性。若基因突變,可能導致 DNA 修復能力下降,進而增加癌症風險。HRD 基因檢測則評估參與 DNA 修復功能的多種基因 是否異常,從而提供更全面的基因資訊。標靶藥物選擇:PARP 抑制劑與血管新生抑制劑的應用策略目前,健保提供部分 BRCA 基因檢測的給付,並根據測試範圍劃分為小套組(檢測 100 個基因以下)和大套組(檢測 100 個以上基因)。此外,台灣癌症基金會也提供善款補助,幫助卵巢癌患者進行 BRCA 或 HRD 基因檢測。BRCA 基因突變患者:健保已納入 PARP 抑制劑作為維持性治療的給付範圍。根據臨床試驗結果與實務經驗,PARP 抑制劑可顯著降低復發風險。此外,這是一種口服標靶藥物,患者可在家服用,無需住院,從而兼顧治療效果與生活品質。HRD 陽性患者:可考慮使用 PARP 抑制劑合併血管新生抑制劑進行雙標靶治療,以進一步提升療效。基因檢測結果為陰性患者:雖然目前健保未給付,但仍可選擇單獨使用上述標靶藥物作為治療選項。邱德生教授提醒,PARP抑制劑容易出現疲倦、貧血,及血小板低下等副作用,不同PARP抑制劑副作用程度不同,而血管新生抑制劑常見副作用為高血壓及腹瀉等,每個人的身體狀況對藥品的反應及副作用不同,治療期間患者需配合醫療團隊,定期監測療效及注意副作用。若疑似有副作用發生,應立即聯繫醫療團隊以調整治療計畫。政策與基因檢測品質把關:未來展望基因檢測和標靶藥物的應用已成為卵巢癌治療的重要組成部分。政府通過健保部分給付以及修訂《特管法》,對基因檢測實驗室進行規範,以確保檢測的準確性與安全性。然而,邱德生教授指出,政策雖然立意良善,但相關配套措施尚未完全落實,導致部分檢測機構在等待審查時無法順利執行檢測。邱德生教授建議,政府若能加速 LDTs(實驗室開發檢測)的審查進程,將能更有效推動基因檢測的普及,進一步提升卵巢癌治療的效率。隨著科技進步與治療方式的多樣化,邱德生教授鼓勵所有癌症病友保持希望,與醫療團隊共同討論,選擇最適合的治療策略,攜手對抗癌症。

2024諾貝爾獎將揭曉! AI、減肥藥受關注
2024年諾貝爾獎將自7日起,依序揭曉生醫、物理、化學、文學、和平等5座獎。根據外媒盤點,其中至少5項是諾貝爾可能的獲獎領域。根據CNN報導,人類基因體圖譜是在諾貝爾獎預測中,經常被討論到的,這是一項大膽的項目,於1990年啟動,並於2003年達成,由美國、英國、法國、德國、日本和中國等,數千名研究人員組成的國際聯盟。這項努力對生物學、醫學和許多其他領域產生了深遠的影響,但該項目可能無法獲得諾貝爾獎的原因之一是參與這項壯舉的人數太多,依據規則,每個獎項只能授予最多3人。第二是,模仿人體激素胰高血糖素樣肽-1(GLP-1)的減肥藥物,其震撼了醫療保健界,這種降低血糖和抑制食慾的藥物有可能開創肥胖症治療和相關疾病的新時代,例如第2型糖尿病。洛克斐勒大學生物化學家莫依索夫(Svetlana Mojsov)、哈佛大學醫學院內分泌學家哈本能(Joel Habener)、丹麥藥廠諾和諾德研究與初期開發部門首席顧問克努森(Lotte Bjerre Knudsen)等3名科學家,在將其轉變為當今數百萬人服用的有效減肥藥物方面發揮了關鍵作用。第三,變革性人工智慧。人工智慧(AI)正在以前所未有的速度改變人們的生活,Google DeepMind AlphaFold蛋白質結構資料庫的開發人員哈薩比斯(Demis Hassabis)、強普(John Jumper),與華盛頓大學醫學院蛋白質設計研究所所長貝克(David Baker)被看好未來可能會獲得諾貝爾化學獎。第四,「腸道菌相」(gut microbiome)領域。細菌、病毒和真菌,生活在人體表面和體內,統稱為人體微生物組,隨著過去20年基因定序的進步,科學家們能夠更了解這些微生物的作用,它們如何與人類細胞,尤其是腸道細胞相互作用。美國聖路易華盛頓大學教授、生物學家高登(Jeffrey Gordon)是該領域的先驅,呼聲相當高。第五,致癌基因檢測。擁有研究人類和黑猩猩之間遺傳差異的背景,現任華盛頓大學醫學院教授金恩(Mary-Claire King)採取了一種全新的方法,早在科學家繪製出人類基因組圖譜之前,其就花了17年的時間來檢測和確定BRCA1基因突變在乳癌和卵巢癌中的作用,這項發現使得基因檢測能夠識別出乳癌風險增加的女性,以及採取哪些措施來降低風險,例如額外的篩檢和預防性手術。

啟動精準治療!NGS納健保含括19癌 台灣第一個本土基因庫誕生
癌症長期位居臺灣十大死因之首,2023年的相關醫療支出近1,400億元,占國家總醫療預算近兩成,反映出癌症治療對健保資源的巨大需求。面對這一挑戰,次世代基因定序檢測(Next Generation Sequencing,NGS)作為精準醫療的重要一環,衛生福利部於5月1日將19種癌症的NGS納入健保給付,透過檢測生物標記尋找基因突變,進而評估標靶藥物精準投藥,預計每年約2萬多名癌症病人受惠。由國家衛生研究院主辦,羅氏大藥廠協辦的「示範計畫領航、健保給付接棒—開創癌症精準醫療新紀元記者會」於今(14)日舉行。會中邀請到衛生福利部中央健康保險署石崇良署長、臺灣癌症基金會賴基銘董事、國家衛生研究院司徒惠康院長、國立臺灣大學醫學院附設醫院癌醫中心分院楊志新院長等多位重量級人物,以及前衛福部部長陳時中,共同見證臺灣癌症精準治療進入新紀元,接軌國際醫療趨勢。司徒惠康院長特別指出,「癌症精準醫療及生物資料庫整合平台合作示範計畫」是一項跨領域合作的典範,包含國衛院,衛福部、五家國際大藥廠及17家醫院。這一跨部門、跨機構的合作,透過全方位的基因檢測和智慧化分析為醫師提供精準的臨床醫療決策支持,收案癌別包含肺癌以及五大消化道癌症。計畫同時成功建立臺灣首個本土臨床基因組數據庫(Clinical-Genomic Database,CGDB),期能累積真實世界數據加速未來藥物的開發和核准流程。截至2024年5月已收錄近兩千筆珍貴真實世界臨床與癌症基因資料,為未來研究和臨床應用提供寶貴資源。司徒院長表示,此計畫不僅促進了臺灣精準醫療體系的發展,也推動了醫療大數據的建立和應用,進一步加速了新藥的研發和核准,為臺灣癌症病人帶來了新的治療希望。針對NGS納入健保給付,健保署石崇良署長說明NGS的健保給付將涵蓋19種癌症,包括14種實體腫瘤和5種血液腫瘤,以NGS及單基因檢測提供民眾多元選擇。給付區分為BRCA、小套組、大套組等三種,依檢測基因數支付不同點數,最高支付定額3萬點,另依專家建議各癌別之檢測時機不同,每人每癌別可終生給付一次。石署長強調,為確保檢測品質並評估後續健保治療藥物的反應與療效,醫事服務機構申報醫療費用須併同上傳檢測結果,以確保能夠在評估給付效益和調整政策時有足夠的實證數據支持。未來若有新的標靶藥物納入健保給付時,醫療機構可以通過資料庫即時查詢藥物的適用條件,避免病人重複接受檢測,從而提升治療效益並降低經濟負擔。此外,健保署亦將致力於促進更多的臨床試驗和新藥的媒合,期許為民眾提供更多及早的治療機會。臺大醫院癌醫中心分院楊志新院長分享了從臨床醫師的視角對NGS檢測和健保給付政策的看法,指出這些進展將使臺灣在全球癌症治療領域保持領先地位。臺灣推動個人化精準醫療已多年,透過基因檢測和智慧化分析,使醫師能做出更精確的臨床決策。期望能大幅改善病人的治療效果和生活品質,同時降低無效用藥,使健保預算更有效地被利用。臺灣癌症基金會賴基銘董事認為,將NGS納入健保給付是一項重大突破,不僅大幅減輕了癌症病人的經濟負擔,也為他們帶來了實質的希望。

每人每癌終生給付一次 次世代基因定序(NGS)5月納健保
次世代基因定序(NGS)價格高昂,不少癌友無法自行負擔,難以找到合適標靶藥。健保署19日帶來好消息,確定5月1日起將NGS納入給付,涵蓋的癌症包括非小細胞肺癌、三陰性乳癌、胰臟癌、血癌等,預估每年約2萬多名癌症病人受惠,經費則需約3億元。此次的給付,象徵著接軌癌症精準醫療趨勢。健保提供3種定額給付方式,分別為BRCA基因檢測支付1萬點、小套組(≦100個基因)支付2萬點、大套組(>100個基因)支付3萬點。NGS涵蓋的實體腫瘤包含:非小細胞肺癌、三陰性乳癌、卵巢癌/輸卵管癌/原發性腹膜癌、攝護腺癌、胰臟癌、NTRK基因融合實體腫瘤、肝內膽管癌、甲狀腺癌、甲狀腺髓質癌等9癌;至於大腸直腸癌、泌尿道上皮癌、黑色素瘤、腸胃道間質瘤及胃癌,將採單基因檢測,近期醫學會已提出申請。針對血癌患者,基因檢測有助於規劃是否適合骨髓移植等治療計畫,本次NGS新增小套組(≦100個基因)及大套組(>100個基因)給付。5大類血液腫瘤包含:急性骨髓性白血病(AML)、高風險之骨髓分化不良症狀群(MDS)、急性淋巴芽細胞白血病(B-ALL及T-ALL)等3癌;另B細胞淋巴癌(BCL)及T或NK細胞血癌與淋巴癌(NKTL)則規劃採單基因檢測,相關醫學會已提出申請。考量各癌別檢測時機不同,健保公告的支付規範依癌別訂有適應症及必要檢測基因,每人每癌別終生給付一次。另為確保檢測品質,限「區域級以上醫院」或「癌症診療品質認證醫院」申報,且必須為衛福部核定的實驗室開發檢測(LDTs)施行計畫表列醫療機構。醫院須自行設立或跨院聯合組成分子腫瘤委員會(MTB),以促進臨床跨領域合作,為不同適應症之癌友提供精準、個人化的治療策略。健保署表示,為確保檢測品質、評估健保治療藥物的反應及療效,醫事服務機構須上傳檢測結果,未來若有新的標靶藥物納入健保給付時,得以資料庫比對查詢適用條件、即時用藥,病人免重複受檢。另健保署研議委託國家級人體生物資料庫平台,促進後續臨床試驗及新藥的媒合,為民眾提供及早治療機會。

基因突變「密密麻麻息肉」!照胃鏡圖曝光 醫嚇呆:跟她媽媽一個模子刻出來
基因檢測真的好準!禾馨民權健康管理診所院長林相宏近日分享,有母親基因異常,造成她的胃和大腸有密密麻麻、數以千計的息肉,結果有女兒又好死不死遺傳到她的基因突變,於是林相宏幫這位女兒做腸胃鏡篩檢,「我真的嚇到了,我眼前胃鏡的畫面,真的跟她媽媽一模模一樣樣,胃裡面有數以千計的息肉」,連息肉的位置、大小、長相、顏色也如同一個模子刻出來的。林相宏也說明,這疾病叫「家族性腺瘤性瘜肉症」,子女約有一半機會遺傳。林相宏昨(15日)在臉書粉專《胰臟醫師 林相宏 禾馨民權內科診所》發文表示,「今天來說一個鬼故事,如果跟你說一個抽血檢測,能預知你的未來,而且很準,你願意嘗試來做嗎?因為有些事情,其實是命中已注定。」林相宏表示,故事中的母親,其實已知道自己有遺傳基因問題,她的基因異常,造成她的胃和大腸有密密麻麻、數以千計的息肉,所以每年都會定期來做息肉切除,「我告訴她,這個疾病是會遺傳給子女的,建議她把子女都帶來做基因檢測。」結果不幸中的大幸,所有子女中只有一位真的遺傳到媽媽的基因突變,媽媽還開玩笑說,「這個小孩真的從小跟我比較像」,於是林相宏也建議小孩要做胃腸鏡篩檢。「胃鏡做下去的那刻,我真的嚇到了!」林相宏形容,「我眼前胃鏡的畫面,真的跟她媽媽一模模一樣樣,胃裡面有數以千計的息肉,連最大顆胃息肉的位置、大小、長相、顏色,也跟她媽媽一模一樣,我真的心中發麻,驚嘆小孩真的是跟媽媽是一個模子刻出來的。」林相宏也驚呼,他對基因檢測的準確感到莫名害怕,他也接著補充說明,這種疾病叫「家族性腺瘤性瘜肉症」,簡稱「FAP」,是一種顯性的遺傳性疾病,子女約有一半機會遺傳,且患者一生中得到大腸癌的機率高達70%。林相宏續稱,突變的基因稱為APC gene,好在病患基因突變的點位,還不是最嚴重那種,從20歲開始全身上下都很容易長出腺瘤,尤其是胃部、大腸、12指腸,平均55歲得到大腸癌。其他癌症的機率也會上升,包括胃癌、胰臟癌、乳癌、小腸癌、甲狀腺癌、肝癌、神經系統癌症,因此建議從18歲開始,每1至2年都要做胃腸鏡篩檢。婦產科名醫蘇怡寧也在貼文底下留言補充,「這些癌症基因就跟大家熟知的乳癌BRCA基因一樣,都是顯性遺傳,不分男女,下一代遺傳機率都是1/2。」有網友也好奇,「比較驚訝的是,這麼多怎麼清!」林相宏則回應,「其實這種疾病得胃癌機率不高,只要先處理大顆胃息肉,反倒是大腸息肉切除會比較辛苦一點,需要斬草除根。」
男30歲竟罹胃癌!一查家中3人有乳癌 醫揪出原因:有關聯
癌症一直是台灣10大死因排名的首位,導致許多人聞「癌症」色變,且家族史中若有癌症的病史,其他家族成員罹患的風險也會相對增加。外科醫師陳榮堅近日也在臉書發文,分享1名30歲男子罹患胃癌的案例,表示實際上乳癌與胃癌有共病基因,有這樣基因的患者,其後代會比一般人罹患胃癌的機率高。外科醫師陳榮堅近日在臉書粉專「外科陳榮堅醫師——不藏私的漸健美園地」發文,指出先前有1名年約30歲的男子,經常覺得胃不舒服而就醫,檢查後發現罹患胃癌,雖然經手術治療,男子已無大礙,癌症也都切得很乾淨,但醫師仍疑惑「怎麼會這麼年輕就罹患胃癌」,結果過沒多久,該男子另1名年約40歲的親戚,也被診斷出罹患胃癌。接連2個案例,不僅同個家族、還都在很年輕時檢查出胃癌,讓醫師們察覺到不對勁,經過詢問後得知,他們的家族中有3名女性得過乳癌,進一步檢驗後更發現,他們家族中帶有BRCA1、BRCA2的基因。陳榮堅醫師解釋,乳癌和胃癌看起來沒什麼關聯,實際上乳癌與胃癌有共病基因,「有一個族群的乳癌患者帶有BRCA1或BRCA2的基因,有這樣基因的病人的後代,會比一般人罹患胃癌的機率還要高」。因此陳榮堅醫師也提醒,若家中出現2位以上的乳癌患者,無論是男性還是女性,都要特別注意胃癌相關的問題,並建議定期安排胃鏡檢查。

共擬會通過次世代基因定序給付!19類癌、2萬人適用 最快5月上路
健保署21日公布,共擬會議通過健保署提案,開放次世代基因定序(NGS)給付。健保署長石崇良表示,NGS將分為3種類別定額給付,包括BRCA-1及BRCA-2、小套組、大套組,分別給付1萬、2萬、3萬點,最快下周預告、5月上路,每年2萬人受惠。石崇良表示,基因檢測適用19種癌,包含非小細胞肺癌、三陰性乳癌、卵巢癌/輸卵管癌/原發性腹膜癌、大腸直腸癌、攝護腺癌、泌尿道上皮癌、肝內膽管癌、黑色素瘤、腸胃道間質瘤、甲狀腺癌、甲狀腺髓質癌、胰臟癌、NTRK基因融合實體腫瘤、胃癌、及5種血液腫瘤。其中包含黑色素瘤、大腸癌在內的4~5種癌症,不需要做到NGS,只需採取單基因檢測即可。NGS採定額方式支付,其中BRCA-1及BRCA-2給付1萬點,100個基因位點以下的小套組給付2萬點,100以上的大套組則是3萬點,依指引執行,各種癌症都有自己的支付標準和條件。石崇良表示,原則上,僅有區域級以上、通過癌症品質認證的醫院才可以申報NGS,必須是通過衛福部核准列冊的機構才可以執行。共擬會議通過後,最快下周預告、5月1日實施,每年2萬人受惠,新增健保支出3億元。

從基因找適合用藥!NGS檢測最快今年五月上路 每癌友每癌症終身用一次
癌症若能精準知道體內突變基因,找到最適合的對應用藥,就能大幅提升藥物治療效果,現可透過「次世代基因定序」(NGS)檢測得知。健保署規劃,將給付19種癌別檢測,署長石崇良今天宣布,最快今年五月上路,每名癌友、每種癌別,終身可以使用健保給付1次,也就是說,若第一次罹患乳癌、第二次罹患不同癌症如卵巢癌,就可再使用。預計每年編列6~10億元預算。癌症治療時,病患常花費時間在嘗試適合的標靶藥物,如今精準醫療成國際趨勢,次世代基因定序(NGS)一次檢測多個癌症基因,有助於精準用藥,但是價格昂貴。衛福部健保署署長石崇良今天上午出席研討會時,宣布健保NGS給付政策方向,除了盤點19種癌別外,政策也確定,「每人每種癌終生給付1次」,但不包含癌症轉移,只有確診第2種癌症才可再使用。石崇良以2022年健保數據分析,當年癌症就診病患達83萬人,藥費支出392億點,其中標靶藥物占率最高,約占整體61.7%。目前健保給付26種標靶藥品,對應11個基因位點,治療10種癌症,但給付方式沒有包含NGS,僅有單一位點檢測,一年約2億,或PCR檢驗,一年約4億元。健保署目前共盤點19種癌別,未來皆納入NGS給付,包含非小細胞肺癌、三陰性乳癌、卵巢癌/輸卵管癌/原發性腹膜癌、肝內膽管癌、攝護腺癌、黑色素瘤癌、腸胃道間質癌、泌尿道上皮癌、甲狀腺癌/甲狀腺髓質癌、大腸直腸癌、NTRK基因融合實體腫瘤、胰臟癌等。除了癌症型別,石崇良表示,檢測時機也是重點,在效益考量及健保經費有限等前提下,研擬健保給付NGS檢測時機為癌症確診時或二、三線治療失敗後,各癌別適用時機不一,仍待依專家共識決定,訂定各癌別檢驗時機指引。至於支付方式規劃3大模式,第一種BRCA1與BRCA2基因,基因片段較長,採獨立給付;第二種是各癌別最基本基因位點小於100個基因的小套組;第三種100個以上基因位點大套組。不採統一定價的全額給付,透過定額給付留下市場彈性,患者可差額自費。石崇良表示,2月6日開完將開最後一次會議,訂出給付NGS規範,待三月共擬會議通過後、還會開一個專家會議、共擬會議,再經預告 期,預估最快五月就能上路。未來也會持續擴大給付項目。
男性「家族史有這病」別輕忽!醫曝易得4種癌:恐比別人早發病
罹患乳癌竟會增加甲狀腺癌的發生率!基隆長庚醫院肝病防治中心主任錢政弘分享一份研究報告,指媽媽或姐妹患有乳癌的成年男性,有較高機率罹患胰臟癌、甲狀腺癌、攝護腺癌及乳癌,且發病時間恐比其他人來得早。錢政弘在臉書粉專發文表示,乳癌為我國女性好發癌症排行第一名,「遺傳性」乳癌機率約15至20%,因此有乳癌家族史的女性需定期接受乳癌篩檢,不過值得注意的是,如果媽媽或姐妹患有乳癌,那麼家中的男性成員則容易罹患4種癌症。錢政弘說明,今年8月一份韓國研究針對6萬9千名有乳癌家族史的成年男性(其母親或姐妹有乳癌)進行追蹤,結果發現相較普通男性,有乳癌家族史的男性罹患「胰臟癌」的風險多1.4倍、「甲狀腺癌」的風險多1.3倍、「攝護腺癌」的風險多1.3倍、「男性乳癌」的風險多3倍;且若母親和姐妹均罹患乳癌,那麼男性發生甲狀腺癌的機率高達3.4倍。對此,錢政弘指出,目前文獻已經知道胰臟癌、攝護腺癌和乳癌都跟「BRCA1/2」基因異常有關,所以一旦媽媽或姐妹有乳癌,男性成員也很有可能因為基因異常得到這3種癌症。錢政弘透露,雖然尚未發現甲狀腺癌與基因異常有關,但觀察發現有乳癌的女性也容易得到甲狀腺癌,推測2者之間有包括甲狀腺荷爾蒙、雌激素和環境因素等共同的致病原因,提醒家中有乳癌病史的男性族群需特別留意。

中年男血尿確診攝護腺癌晚期 搭配精準治療重拾人生
6旬鄭先生因血尿、半夜頻尿至泌尿科就診,一診斷竟是攝護腺癌第四期,且癌細胞轉移到淋巴系統及骨頭,恐活不到2年!由於有癌症家族病史,患者接受基因檢測,找出BRCA致病性基因缺陷,從化療改用PARP抑制劑治療,不僅穩定存活4年多,打球、游泳、跑步都沒問題。台灣泌尿科醫學會呼籲轉移性攝護腺癌患者,11月起健保擴大給付標靶新藥,及早基因檢測搭配第一線精準治療,仍有機會重拾人生。攝護腺癌是年長男性殺手,美國影集《六人行》男星詹姆斯邁克爾泰勒(James Michael Tyler)、名媛孫芸芸父親、前太平洋董座孫道存皆因攝護腺癌過世。台灣泌尿科醫學會馮思中理事長表示,根據衛生福利部110年癌症登記報告,攝護腺癌高居男性十大好發癌症第5名,死亡第6名,發生人數7481位,年新增個案以4%速度成長,相當可怕。多數患者常在排尿異常、雙腿無力,甚至是背痛才求醫,此時可能已為晚期骨轉移,臨床約有3成患者被診斷為轉移性攝護腺癌,若家中親人曾罹患癌症、有家族病史,罹癌風險更高,應小心預防。及早基因檢測 掌握前「腺」治療關鍵攝護腺癌藥物治療選項多,不同的治療策略對於後續疾病發展及病友存活期影響甚鉅。臨床治療大多是給予荷爾蒙藥物以抑制雄性激素,但病友通常治療幾年後會產生抗藥性,發展為「轉移性去勢抗性攝護腺癌」,疾病惡化程度及死亡率高。台灣泌尿科醫學會泌尿腫瘤委員會健保擴大給付標靶新藥黃昭淵分享,具有BRCA基因突變的人罹患攝護腺癌後,死亡率則為一般人的2.5倍,主要因為病程進展較快、對傳統治療的反應比較差,因此預後也比較不好;在轉移性攝護腺癌患者中,約12%具有BRCA基因突變,若使用標靶藥物PARP抑制劑,可讓具有受損BRCA基因的癌細胞無法被修復,導致癌細胞死亡進而可延緩或停止腫瘤生長。荷爾蒙治療產生抗藥性! 健保擴大給付標靶新藥根據研究,標靶藥物PARP抑制劑針對BRCA基因突變轉移性去勢抗性攝護腺癌治療上,可降低近8成疾病惡化風險,今年11月也獲得健保給付,成為有BRCA1/2基因突變且曾使用過新型荷爾蒙治療惡化病友的治療新選擇。高雄榮民總醫院泌尿科郭威廷醫師指出,以往自費使用PARP抑制劑在轉移性去勢抗性攝護腺癌的治療,每月約需耗費10萬元,擴大給付後估計每年約有296位患者受惠。曾使用荷爾蒙療法仍惡化的去勢抗性攝護腺癌患者,經BRCA基因檢測後,具有BRCA1/2或與DNA修復相關基因的基因突變皆受惠,可在第一線治療就獲得較佳的成效,大幅減輕經濟負擔。郭威廷進一步說明,現今轉移性攝護腺癌邁入精準治療,一線治療會影響預後。根據研究,與新一代的荷爾蒙療法相比,若使用PARP抑制劑可以減少近8成的疾病惡化風險,以及死亡風險降低近4成。相較單用新一代荷爾蒙藥物,PARP抑制劑亦可與新一代荷爾蒙療法合併使用,可延長無惡化存活期近1年以上,有效縮小腫瘤、降低PSA指數,四期攝護腺癌雖無法治癒,但穩定控制症狀,有望和疾病和平共處,維持生活品質。馮思中呼籲,進入轉移性去勢抗性攝護腺癌的病友們,可及早進行基因檢測、掌握精準治療,現健保擴大給付PARP抑制劑在轉移性去勢抗性攝護腺癌的治療,讓患者獲得最好的治療成效。男性朋友也應更加注意自我的健康,50歲以上的男性應定期進行PSA篩檢,若家族中有癌症病史者應格外注意,及早篩檢不僅有助於發現潛在的健康問題,也有助於提前預防、及早應對,增加早期發現治療的機會,掌握前「腺」才是掌握人生自由關鍵。

攝護腺癌標靶新藥獲健保給付 一線治療可降近8成惡化風險
根據衛生福利部110年癌症登記報告,攝護腺癌已高居男性十大好發癌症第五名,像是美國經典電視影集《六人行》中的男星詹姆斯邁克爾泰勒(James Michael Tyler)以及名媛孫芸芸父親、前太平洋董座孫道存皆因攝護腺癌過世。台灣泌尿科醫學會馮思中理事長表示,攝護腺癌多數患者常在排尿異常、雙腿無力,甚至是背痛後才進行診斷,而此時可能已為晚期骨轉移,臨床觀察病患進入診間約有三成患者被診斷為轉移性攝護腺癌,若家中有親人曾罹患癌症、有家族病史,罹癌風險更高應小心預防。攝護腺癌藥物治療選項多,但不同的治療策略對於後續疾病發展及病友存活期影響重大。臨床治療,大多是給予荷爾蒙藥物以抑制雄性激素,但病友通常在治療幾年後會產生抗藥性,而發展為「轉移性去勢抗性攝護腺癌」,疾病惡化程度及死亡率高。根據研究,標靶藥物PARP抑制劑針對BRCA基因突變轉移性去勢抗性攝護腺癌治療上,可降低近八成疾病惡化風險,今年11月也獲得健保給付,成為有BRCA1/2基因突變且曾使用過新型荷爾蒙治療惡化病友的治療新選擇!台灣泌尿科醫學會泌尿腫瘤委員會黃昭淵主委分享,具有BRCA基因突變的人罹患攝護腺癌後,死亡率則為一般人的2.5倍,主要因為病程進展較快、對傳統治療的反應比較差,因此預後也比較不好;在轉移性攝護腺癌患者中,約12%具有BRCA基因突變,若使用標靶藥物PARP抑制劑,則可讓具有受損BRCA基因的癌細胞無法被修復,導致癌細胞死亡進而可延緩或停止腫瘤生長,因此PARP抑制劑是精準對抗BRCA基因突變相關癌症的利器。高雄榮民總醫院泌尿科郭威廷醫師指出,今年11月起健保署擴大給付PARP抑制劑在轉移性去勢抗性攝護腺癌的治療上,曾使用過賀爾蒙療法且惡化的去勢抗性攝護腺癌患者,經BRCA基因檢測後,具有BRCA1/2或與DNA修復相關基因的基因突變皆受惠,可在第一線治療就獲得較佳的成效,也大幅減輕患者經濟上的負擔,而轉移性攝護腺癌惡性程度高,年長患者多體力不足接受二線治療,故一線藥物選擇相當重要,可以延長整體存活時間。郭威廷醫師進一步說明,現今轉移性攝護腺癌已邁入精準治療,一線治療也會影響預後。根據研究,與新一代的荷爾蒙療法相比,若使用PARP抑制劑可以減少近八成的疾病惡化風險,以及死亡風險降低近四成。相較單用新一代荷爾蒙藥物,PARP抑制劑亦可與新一代賀爾蒙療法合併使用,可延長無惡化存活期近一年以上,有效縮小腫瘤、降低PSA指數,提升患者生活品質。與攝護腺癌抗戰將近四年的鄭先生也現身分享,當初因為血尿、半夜頻尿而至泌尿科就診,卻被醫師診斷時已是攝護腺癌第四期,且癌細胞已轉移到淋巴系統及骨頭,可能僅剩不到兩年的存活期。因鄭先生也有癌症家族病史,父親因肺癌過世,二哥及爺爺皆為胃癌,在接受過攝護腺癌的標準治療後,也跟從醫師建議進行基因檢測,找出BRCA致病性的基因缺陷,並調整使用PARP抑制劑進行治療。鄭先生現已60歲,穩定跟攝護腺癌共處4年多,早已突破一開始被宣告的存活期,也讓他更珍惜生病後的每一天。比起初期化療讓他體力迅速下滑像是80歲老爺爺,精準化的治療下能保持良好的生活品質,不論是打高爾夫還是游泳、慢跑都可正常的進行。台灣泌尿科醫學會馮思中理事長更再次呼籲進入轉移性去勢抗性攝護腺癌的病友們,第一線治療選擇相當重要!可及早進行基因檢測掌握精準治療關鍵,現健保擴大給付PARP抑制劑在轉移性去勢抗性攝護腺癌的治療後,讓患者可以獲得最好的治療成效。男性朋友也應更加注意自我的健康,50歲以上的男性應定期進行PSA篩檢,若家族中有癌症病史者應格外注意,及早篩檢不僅有助於發現潛在的健康問題,也有助於提前預防、及早應對。